2.有下列几种说法:①含同元素的微粒的化学性质不一定相同;②相对分子质量相同的物质如果结构不同则互为同分异构体;③同分异构体的化学性质一定相同;④同系物具有相同的通式;⑤同系物的化学性质相似;⑥互为同系物的物质间不可能互为同分异构体;⑦两相邻同系物的相对分子质量相差14;⑧化学式相同,各元素质量分数也相同的物质一定是同种物质;以上说法中不正确的是( )
| A. | ②③④ | B. | ②③⑧ | C. | ③④⑤⑦⑧ | D. | ②⑥⑦⑧ |
1.下列物质命名中肯定正确的是( )
| A. | 2,2-二甲基丁烷 | B. | 3,3-二甲基丁烷 | ||
| C. | 2-甲基-3-乙基丁烷 | D. | 4-甲基-3-乙基己烷 |
20.下列说法正确的是( )
| A. | 有机化合物都是从有机体中提炼出来的 | |
| B. | 有机物和无机物的性质完全不同 | |
| C. | 所有有机物均含有碳元素 | |
| D. | 所有有机物均含有氢元素 |
18.有A、B、C、D、E五种短周期元素,已知A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如右图所示.E的单质可与酸反应,1mol E单质与足量酸反应能产生22.4L H2(标准状况);E的阳离子与A的阴离子核外电子排布完全相同.回答下列问题:
(1)B在周期表中的位置为第三周期第VA族.
(2)元素A在化合物中一般显负(填正或负)价,但在与F(填元素符号)形成化合物时,所显示的价态正好相反.
(3)比较C、D元素简单离子半径的大小S2->Cl-(填离子符号).
(4)向D与E形成的化合物的水溶液中加入过量氨水,有关反应的离子方程式为Mg2++2 NH3.H2O═Mg (OH)2↓+2 NH4+.
(5)D的最高价氧化物对应的水化物与E的最高价氧化物对应的水化物反应的化学方程式为Mg(OH)2+2HClO4═Mg(ClO4)2+2H2O.
| A | ||
| B | C | D |
(2)元素A在化合物中一般显负(填正或负)价,但在与F(填元素符号)形成化合物时,所显示的价态正好相反.
(3)比较C、D元素简单离子半径的大小S2->Cl-(填离子符号).
(4)向D与E形成的化合物的水溶液中加入过量氨水,有关反应的离子方程式为Mg2++2 NH3.H2O═Mg (OH)2↓+2 NH4+.
(5)D的最高价氧化物对应的水化物与E的最高价氧化物对应的水化物反应的化学方程式为Mg(OH)2+2HClO4═Mg(ClO4)2+2H2O.
17.下列离子方程式书写正确的是( )
| A. | Fe2(SO4)3和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ | |
| B. | 等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| C. | 浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+$\frac{\underline{\;\;△\;\;}}{\;}$Fe3++3NO2↑+3H2O | |
| D. | 0.01 mol•L-1 NH4Al(SO4)2溶液与0.02 mol•L-1 Ba(OH)2溶液等体积混合:NH4++Al3++2 SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O |
16.现有下列几组粒子:①N2、CO;②NH4+、OH-;③O22-、CN-;④PO43-、ClO4-.对上述四组粒子归类正确的是( )
| A. | 质子数相等、电子数和原子数不相等:① | |
| B. | 质子数和电子数相等、原子数不相等:② | |
| C. | 电子数相等、质子数和原子数不相等:③ | |
| D. | 原子数和电子数相等、质子数不相等:④ |
15.下列电池工作时,O2在正极放电的是( )
| A. |  锌锰电池 | B. |  氢燃料电池 | ||
| C. |  铅蓄电池 | D. |  镍镉电池 |
14.H、C、N、O、都属于自然界中常见非金属元素.
(1)O、C、N三种元素的第一电离能由小到大顺序是C O N;NH4+中氮原子轨道的杂化类型为sp3杂化.
(2)CO、N2的结构可表示为:C≡O、N≡N两者的键能数据:(单位kJ/mol)
结合数据说明CO比N2活泼的原因CO的第一个π键的键能为273kJ/mol,N2中的第一个π键的键能为523.3kJ/mol,所以CO的第一个键比N2更容易断裂.
(3)乙二胺(H2N-CH2-CH2-NH2)和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键.
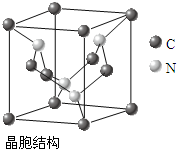
(4)C、N元素形成的新材料具有如右图所示结构,该晶体硬度将超过目前世界上最硬的金刚石,成为首屈一指的超硬新材料.该物质的化学式为:C3N4.
0 168900 168908 168914 168918 168924 168926 168930 168936 168938 168944 168950 168954 168956 168960 168966 168968 168974 168978 168980 168984 168986 168990 168992 168994 168995 168996 168998 168999 169000 169002 169004 169008 169010 169014 169016 169020 169026 169028 169034 169038 169040 169044 169050 169056 169058 169064 169068 169070 169076 169080 169086 169094 203614
(1)O、C、N三种元素的第一电离能由小到大顺序是C O N;NH4+中氮原子轨道的杂化类型为sp3杂化.
(2)CO、N2的结构可表示为:C≡O、N≡N两者的键能数据:(单位kJ/mol)
| A-B | A=B | A≡B | |
| CO | 357.7 | 798.9 | 1071.9 |
| N2 | 154.8 | 418.4 | 941.7 |
(3)乙二胺(H2N-CH2-CH2-NH2)和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键.
(4)C、N元素形成的新材料具有如右图所示结构,该晶体硬度将超过目前世界上最硬的金刚石,成为首屈一指的超硬新材料.该物质的化学式为:C3N4.

 、
、 、
、 、
、 、
、 .
.