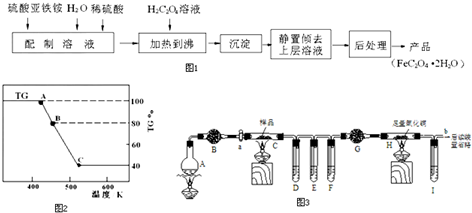
题目内容
17.下列离子方程式书写正确的是( )| A. | Fe2(SO4)3和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ | |
| B. | 等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| C. | 浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+$\frac{\underline{\;\;△\;\;}}{\;}$Fe3++3NO2↑+3H2O | |
| D. | 0.01 mol•L-1 NH4Al(SO4)2溶液与0.02 mol•L-1 Ba(OH)2溶液等体积混合:NH4++Al3++2 SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O |
分析 A.离子个数配比不符合物质的结构;
B.漏掉氢离子与氢氧根离子的反应;
C.加入过量铁粉,生成亚铁离子;
D.NH4Al(SO4)2与Ba(OH)2按照物质的量之比为1:2反应,生成硫酸钡、氢氧化铝和一水合氨.
解答 解:A.Fe2(SO4)3和Ba(OH)2溶液反应的离子方程式,2Fe3++3SO42-+3Ba2++6OH-=2Fe(OH)3↓+3BaSO4↓,故A错误;
B.等物质的量的MgCl2、Ba(OH)2 和 HC1 溶液混合:Mg2++2H++4OH-=Mg(OH)2↓+2H2O,故B错误;
C.加入过量铁粉,生成亚铁离子和二氧化氮,随着反应进行硝酸浓度变稀,反应生成一氧化氮,离子反应为Fe+2NO3-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Fe2++2NO2↑+2H2O,3Fe+2NO3-+8H+$\frac{\underline{\;\;△\;\;}}{\;}$3Fe2++2NO↑+4H2O,故C错误;
D.0.01 mol•L-1 NH4Al(SO4)2溶液与0.02 mol•L-1 Ba(OH)2溶液等体积混合:NH4++Al3++2 SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意反应物用量对反应的影响,选项CD为易错选项.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 标准状况下,B2H6和C2H4的混合气体22.4L,所含的电子数约为16NA | |
| B. | 1mol甲基(-CH3)所含电子数为9NA | |
| C. | 标准状况下,1L庚烷所含有的分子数为$\frac{{N}_{A}}{22.4}$ | |
| D. | 26g C2H2和苯蒸气的混合气体中所含的C原子数为2NA |
2.有下列几种说法:①含同元素的微粒的化学性质不一定相同;②相对分子质量相同的物质如果结构不同则互为同分异构体;③同分异构体的化学性质一定相同;④同系物具有相同的通式;⑤同系物的化学性质相似;⑥互为同系物的物质间不可能互为同分异构体;⑦两相邻同系物的相对分子质量相差14;⑧化学式相同,各元素质量分数也相同的物质一定是同种物质;以上说法中不正确的是( )
| A. | ②③④ | B. | ②③⑧ | C. | ③④⑤⑦⑧ | D. | ②⑥⑦⑧ |
9.某反应方程式为 ,下列说法错误的是( )
,下列说法错误的是( )
 ,下列说法错误的是( )
,下列说法错误的是( )| A. | 反应物的分子式为C10H10O4 | |
| B. | X的结构简式为CH3OH | |
| C. | 生成物中带“※”号的C原子来自“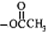 ”中的甲基 ”中的甲基 | |
| D. | 反应物和生成物具有相同的不饱和度 |
7.下列只含极性键的共价化合物为( )
| A. | KCl | B. | Na2O2 | C. | H2O2 | D. | CH4 |
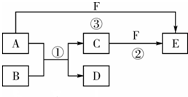 A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应.
A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应. ,反应③的化学方程式是4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
,反应③的化学方程式是4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.