3.工业上回收利用某合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)的工艺流程如下:
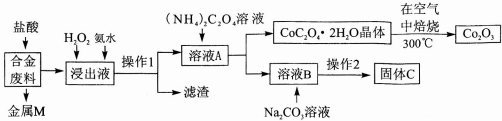
(1)金属M为Cu,操作1为过滤.
(2)加入H2O2的作用是(用离子方程式表示)2Fe2++H2O2+2H+=2Fe3++2H2O,加入氨水的作用是调节溶液的pH使Fe3+转化为Fe(OH)3沉淀.
(3)充分焙烧的化学方程式为4CoC2O4?2H2O+3O2$\frac{\underline{\;焙烧\;}}{\;}$2Co2O3+8 H2O+8CO2.
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表.操作2中,蒸发浓缩后必须趁热过滤,其原因是减少Li2CO3的溶解损失,90℃时Ksp(Li2CO3)的值为4.0×10-3.
(5)用惰性电极电解熔融Li2CO3制取锂,阳极生成两种气体,则阳极的电极反应式为2CO32--4e-=O2↑+2CO2↑.

(1)金属M为Cu,操作1为过滤.
(2)加入H2O2的作用是(用离子方程式表示)2Fe2++H2O2+2H+=2Fe3++2H2O,加入氨水的作用是调节溶液的pH使Fe3+转化为Fe(OH)3沉淀.
(3)充分焙烧的化学方程式为4CoC2O4?2H2O+3O2$\frac{\underline{\;焙烧\;}}{\;}$2Co2O3+8 H2O+8CO2.
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表.操作2中,蒸发浓缩后必须趁热过滤,其原因是减少Li2CO3的溶解损失,90℃时Ksp(Li2CO3)的值为4.0×10-3.
| 温度/℃ | 10 | 30 | 60 | 90 |
| 浓度/mol•L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
2.过氧化尿素是一种新型漂白、消毒剂,广泛应用于农业、医药、日用化工等领域.湿法工艺制取过氧化尿素是用低浓度的双氧水和饱和尿素溶液在一定条件下合成过氧化尿素.反应的方程式为:CO(NH2)2+H2O2 $\frac{\underline{\;30℃\;}}{\;}$CO(NH2)2•H2O2△H<0.过氧化尿素的部分性质如下:
湿法合成过氧化尿素的流程图如下:

请回答下列问题:
(1)反应器的加热方式是水浴加热;反应温度需控制在适当温度下进行,温度不能过高的原因是温度过高,产品易分解,致使活性氧含量降低,温度也不能过低的原因是温度过低,反应速率太慢,且反应体系制冷需要消耗大量能量.
(2)若欲从母液中分离出H2O2和尿素,可采用的操作是减压蒸馏、结晶.
(3)干法工艺制取过氧化尿素的方法是:采用高浓度双氧水水溶液喷雾到无水尿素固体上进行反应,水和反应热通过流态床移去而得到干燥的过氧化尿素产品.
比较干法与湿法两种工艺,你认为干法工艺的优点是:流程短,工艺简单(答出一点即可),干法工艺的缺点是:双氧水浓度高经济效益低,设备复杂等(答出两点即可),湿法工艺的优点是:低浓度双氧水,经济效益高,设备简单易于达到,母液可循环使用等(答出两点即可).
(4)准确称取0.6000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加1mL 6mol•L-1H2SO4,用0.1000mol•L-1KMnO4标准溶液滴定至终点时消耗20.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2•H2O2的质量分数为78.3%(结果保留到小数点后一位).
| 分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
| CO(NH2)2•H2O2 | 白色晶体 | 45℃ | 75-85℃ | 易溶于水、有机溶剂 |

请回答下列问题:
(1)反应器的加热方式是水浴加热;反应温度需控制在适当温度下进行,温度不能过高的原因是温度过高,产品易分解,致使活性氧含量降低,温度也不能过低的原因是温度过低,反应速率太慢,且反应体系制冷需要消耗大量能量.
(2)若欲从母液中分离出H2O2和尿素,可采用的操作是减压蒸馏、结晶.
(3)干法工艺制取过氧化尿素的方法是:采用高浓度双氧水水溶液喷雾到无水尿素固体上进行反应,水和反应热通过流态床移去而得到干燥的过氧化尿素产品.
比较干法与湿法两种工艺,你认为干法工艺的优点是:流程短,工艺简单(答出一点即可),干法工艺的缺点是:双氧水浓度高经济效益低,设备复杂等(答出两点即可),湿法工艺的优点是:低浓度双氧水,经济效益高,设备简单易于达到,母液可循环使用等(答出两点即可).
(4)准确称取0.6000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加1mL 6mol•L-1H2SO4,用0.1000mol•L-1KMnO4标准溶液滴定至终点时消耗20.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2•H2O2的质量分数为78.3%(结果保留到小数点后一位).
16.在一定条件下,既能发生酯化反应,又能发生消去反应的是( )
| A. | CH3CH2OH | B. | CH3OH | C. | CH3CHO | D. | CH3COOH |
15.在有机物的学习中,有机物的式子书写、模型的使用非常重要,下列说法正确的是( )
| A. | 分子式表明了分子中各原子的个数和连接方式 | |
| B. | 结构式、结构简式可表示分子中各原子的连接方式和相对位置 | |
| C. | 球棍模型可表示分子的真实形态 | |
| D. | 比例模型较真实反映分子空间构型 |
14. 磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )
磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )
 磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )
磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )| A. | 该系统中不只存在化学能和电能的相互转化 | |
| B. | 在移位反应器中,反应CO(g)+H2O(g)?CO2(g)+H2(g)(△H>0),若温度越高,则v(CO)越大 | |
| C. | 改质器和移位反应器的作用是将CxHy转化为H2和CO2 | |
| D. | 该电池正极的电极反应为O2+4H+-4e-═2H2O |
13.同温同体积同质量的CO2、CO、H2、O2的压强,按从大到小的顺序排列正确的是( )
| A. | H2>O2>CO>CO2 | B. | H2>CO>O2>CO2 | C. | CO2>O2>CO>H2 | D. | CO2>H2>O2>CO |
12.反应3NO2+H2O=2HNO3+NO中,当有4mol电子发生转移时,被氧化的物质与被还原的物质的物质的量之比是( )
| A. | 1:1 | B. | 1:2 | C. | 2:1 | D. | 3:1 |
11.下列说法正确的是( )
| A. | 任何状态下,1molCO2和18克水所含的分子数和原子数都相等 | |
| B. | 22.4L的任何气体的物质的量为1mol | |
| C. | 非标准状况下,1mol任何气体的体积必定不是22.4L | |
| D. | 标准状况下,1molSO3的体积是22.4L |
10.下列有关电解质叙述正确的是( )
0 168872 168880 168886 168890 168896 168898 168902 168908 168910 168916 168922 168926 168928 168932 168938 168940 168946 168950 168952 168956 168958 168962 168964 168966 168967 168968 168970 168971 168972 168974 168976 168980 168982 168986 168988 168992 168998 169000 169006 169010 169012 169016 169022 169028 169030 169036 169040 169042 169048 169052 169058 169066 203614
| A. | 熔融状态下能导电的物质是电解质 | |
| B. | BaSO4虽然难溶,但是强电解质 | |
| C. | NH3的水溶液能导电,所以NH3是电解质 | |
| D. | 弱电解质溶液的导电性比强电解质溶液弱 |