17. 下表为周期表中短周期的一部分.已知a原子的最外层电子数是电子总数的三分之一,下列说法中正确的是( )
下表为周期表中短周期的一部分.已知a原子的最外层电子数是电子总数的三分之一,下列说法中正确的是( )
 下表为周期表中短周期的一部分.已知a原子的最外层电子数是电子总数的三分之一,下列说法中正确的是( )
下表为周期表中短周期的一部分.已知a原子的最外层电子数是电子总数的三分之一,下列说法中正确的是( )| A. | a的最高价氧化物对应水化物有两性 | |
| B. | b与d组成的化合物不能与水反应 | |
| C. | c的单质能与强碱反应生成两种盐 | |
| D. | c与d能形成共价化合物和离子化合物 |
16.下列化学反应的离子方程式正确的是( )
| A. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- | |
| B. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| C. | 用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| D. | 等体积、等物质的量浓度的氢氧化钙溶液与稀硫酸混合:Ca2++OH-+H++SO42-═CaSO4↓+H2O |
15.在短周期主族元素中,族序数与原子的核电荷数、电子层数均为奇数的有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
14.下列排列顺序不正确的是( )
| A. | 离子半径:Mg2+>O2->F- | B. | 原子半径:Na>S>O | ||
| C. | 热稳定性:HF>HCl>HBr | D. | 酸性:HClO4>H2SO4>H3PO4 |
13.下列实验不能达到相应的实验目的是( )
| 选项 | 实验 | 实验目的 |
| A | 钠和镁分别投入冷水中 | 判断钠和镁金属性强弱 |
| B | 在MgCl2与AlCl3溶液中分别加入过量的氨水 | 判断镁与铝的金属性强弱 |
| C | 向硅酸钠溶液中通入CO2 | 判断碳酸与硅酸的酸性强弱 |
| D | Br2与I2分别与足量的H2反应 | 判断溴与碘的非金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
12.对于化学反应中的能量变化,表述正确的是( )
| A. | 氧化还原反应均为放热反应 | B. | 放热反应中,反应后体系能量降低 | ||
| C. | 断开化学键的过程会放出能量 | D. | 加热才能发生的反应均为吸热反应 |
11.下列有关周期表的说法中,正确的是( )
| A. | 每个主族都含有非金属元素 | B. | 构成半导体的元素都是非金属元素 | ||
| C. | 过渡元素都属于金属元素 | D. | 非金属元素都位于短周期 |
10.下列热化学方程式或离子方程式中,正确的是( )
| A. | 0.01mol•L-1NH4Al(SO4)2溶液与0.02mol•L-1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| B. | 一定条件下,将0.5mol N2(g)和1.5molH2(g)置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 如图表示H2与O2发生反应过程中的能量变化,H2的燃烧热为571.6 kJ•mol-1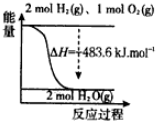 | |
| D. | CO(g)的燃烧热是283.0 kJ•mol-1,则CO2分解的热化学方程式为:2CO2(g)=2CO(g)+O2(g)△H=+283.0 kJ•mol-1 |
9.下列含氧酸中酸性最强的是( )
0 168439 168447 168453 168457 168463 168465 168469 168475 168477 168483 168489 168493 168495 168499 168505 168507 168513 168517 168519 168523 168525 168529 168531 168533 168534 168535 168537 168538 168539 168541 168543 168547 168549 168553 168555 168559 168565 168567 168573 168577 168579 168583 168589 168595 168597 168603 168607 168609 168615 168619 168625 168633 203614
| A. | H2SO4 | B. | HClO4 | C. | H3PO4 | D. | H2SeO4 |
 ,而不排布成
,而不排布成 ,其直接的根据是洪特规则.
,其直接的根据是洪特规则.