8.中国的锰矿石和锌矿石产地在云南、广东、青海等.软锰矿是一种常见的锰矿石,其主要成分是MnO2,含少量Al2O3和SiO2.闪锌矿主要成分是ZnS,含少量FeS、CuS、CdS等杂质,晶体属于六方晶系.现以软锰矿和闪锌矿为原料制备MnO2和Zn,其简化流程如图.

已知:Ⅰ.矿石中所有金属元素在滤液A中均以离子形式存在.
Ⅱ.各种金属离子完全沉淀的pH如表:
回答下列问题:
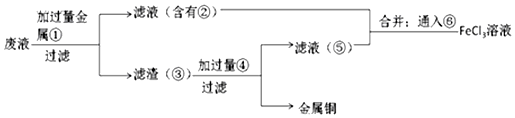
(1)步骤①中MnO2、CuS与硫酸共热时有淡黄色物质析出,请写出该反应的化学方程式CuS+MnO2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+MnSO4+S+2H2O.
(2)步骤②加入适量金属锌是为了回收金属,回收金属的主要成分是Cu、Cd.
(3)步骤③中MnO2的作用是将Fe2+氧化为Fe3+,另外一种物质X可以是AD.
A.ZnO B.MgO C.Cu2(OH)2CO3 D.MnCO3
(4)锂离子电池的正极材料有多种,其中MnO2与Li构成LiMnO2是一种常见的正极材料.电池反应方程式为:Li1-xMnO2+LixC6═LiMnO2+6C,写出该锂离子电池的正极电极反应式Li1-xMnO2+xLi++xe-=LiMnO2.
(5)已知:HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10-7,K2=7.0×10-15,向NaCN溶液中通入少量的H2S气体,反应的离子方程式为CN-+H2S=HCN+HS-.
在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020mol•L-1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS-浓度为1.0×10-4 mol•L-1时,Mn2+开始沉淀,则a=5.[已知:Ksp(MnS)=1.4×10-15].

已知:Ⅰ.矿石中所有金属元素在滤液A中均以离子形式存在.
Ⅱ.各种金属离子完全沉淀的pH如表:
| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
(1)步骤①中MnO2、CuS与硫酸共热时有淡黄色物质析出,请写出该反应的化学方程式CuS+MnO2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+MnSO4+S+2H2O.
(2)步骤②加入适量金属锌是为了回收金属,回收金属的主要成分是Cu、Cd.
(3)步骤③中MnO2的作用是将Fe2+氧化为Fe3+,另外一种物质X可以是AD.
A.ZnO B.MgO C.Cu2(OH)2CO3 D.MnCO3
(4)锂离子电池的正极材料有多种,其中MnO2与Li构成LiMnO2是一种常见的正极材料.电池反应方程式为:Li1-xMnO2+LixC6═LiMnO2+6C,写出该锂离子电池的正极电极反应式Li1-xMnO2+xLi++xe-=LiMnO2.
(5)已知:HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10-7,K2=7.0×10-15,向NaCN溶液中通入少量的H2S气体,反应的离子方程式为CN-+H2S=HCN+HS-.
在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020mol•L-1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS-浓度为1.0×10-4 mol•L-1时,Mn2+开始沉淀,则a=5.[已知:Ksp(MnS)=1.4×10-15].
7.草酸钴是制作氧化钴和金属钴的原料.一种利用含钴废料(主要成分Co2O3),含少量Fe2O3、MnO2、Al2O3、CaO、MgO、碳及有机物等)制取草酸钴(CoC2O3)的工艺流程如图1:

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等.
②部分阳离子一氢氧化物形式沉淀时溶液的pH见表:
③Kap(MgF2)=7.35×10-11,Kap(CaF2)=1.05×10-10
回答下列问题:
(1)焙烧的目的是除去碳和有机物;浸钴过程中Co3+转化为Co2+,反应的离子方程式为2Co3++SO32-+H2O=2Co2++SO42-+2H+.
(2)加入H2O2的目的是将 Fe2+氧化为 Fe3+,加入Na2CO3溶液,调pH至5.2,滤渣Ⅰ主要成分为Al(OH)3、Fe(OH)3.
(3)加入过量NaF溶液,可将Ca2+、Mg2+除去,若所得滤液中c(Ca2+)=1.0×10-3mol•L-1,则滤液中c(Mg2+)为7.0×10-4 mol•L-1.
(4)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是除去Mn2+;萃取时,溶液的pH需要控制在一定范围内才比较适宜,其pH范围约为3.0~3.5.
(5)已知含钴废料中含Co2O3质量分数为a%,若取mg该含钴废料按照上述流程,理论上最多能制得CoC2O4的质量为$\frac{147ma%}{83}$ 或 1.77×10-2mag(列出计算式即可).

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等.
②部分阳离子一氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀时的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
回答下列问题:
(1)焙烧的目的是除去碳和有机物;浸钴过程中Co3+转化为Co2+,反应的离子方程式为2Co3++SO32-+H2O=2Co2++SO42-+2H+.
(2)加入H2O2的目的是将 Fe2+氧化为 Fe3+,加入Na2CO3溶液,调pH至5.2,滤渣Ⅰ主要成分为Al(OH)3、Fe(OH)3.
(3)加入过量NaF溶液,可将Ca2+、Mg2+除去,若所得滤液中c(Ca2+)=1.0×10-3mol•L-1,则滤液中c(Mg2+)为7.0×10-4 mol•L-1.
(4)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是除去Mn2+;萃取时,溶液的pH需要控制在一定范围内才比较适宜,其pH范围约为3.0~3.5.
(5)已知含钴废料中含Co2O3质量分数为a%,若取mg该含钴废料按照上述流程,理论上最多能制得CoC2O4的质量为$\frac{147ma%}{83}$ 或 1.77×10-2mag(列出计算式即可).
5.下列属于加成反应的是( )
0 163942 163950 163956 163960 163966 163968 163972 163978 163980 163986 163992 163996 163998 164002 164008 164010 164016 164020 164022 164026 164028 164032 164034 164036 164037 164038 164040 164041 164042 164044 164046 164050 164052 164056 164058 164062 164068 164070 164076 164080 164082 164086 164092 164098 164100 164106 164110 164112 164118 164122 164128 164136 203614
| A. | CCl4+H2$→_{△}^{催化剂}$ CHCl3+HCl | B. | 2CH2=CH2+O2$→_{△}^{催化剂}$2CH3CHO | ||
| C. |  +HNO3$→_{50℃-60℃}^{浓H_{2}SO_{4}}$+H2O+ +HNO3$→_{50℃-60℃}^{浓H_{2}SO_{4}}$+H2O+ | D. |  +3H2$→_{△}^{Ni}$ +3H2$→_{△}^{Ni}$ |




 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: