��Ŀ����
1�������Ṥҵ��SO2β��������ʯ��ʯ����̿��̼����狀��Ȼ��ص�Ϊԭ�ϣ����Ժϳ�����ҪӦ�ü�ֵ���ơ�����ء������ᰱ�����ʣ��ϳ�·�����£�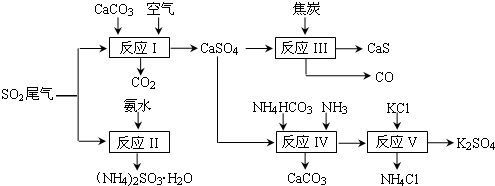
��1�������У���ӦII�е���Һ�м���������ԭ�Ժ�ǿ�ĶԱ����ӵ����ʣ���Ŀ���Ƿ�ֹ������隣�������
��2�������й�˵����ȷ����ABCD��
A����ӦI����������������Ա�֤�����������������������
B����Ӧ�Ļ�ѧ����ʽΪCaSO4+4C$\frac{\underline{\;����\;}}{\;}$CaS+4CO��
C����ӦIV������¶���60��70�棬Ŀ��֮һ�Ǽ���̼���ⰱ�ķֽ�
D����ӦV�еĸ������Ȼ�刺��������ʣ�
���� ��1�������ᰱ�е���Ϊ+4�ۣ��ױ������е�����������
��2��A����������ͼ��Ϸ�Ӧ����������������Ŀ����������������Ϊ����ƣ�
B����Ӧ��ѧ����ʽΪ��CaSO4+4C=CaS+4CO����
C����ֹ̼��������¶ȹ���ʱ�ֽ⣻
D���Ȼ����һ�ֵ��ʣ�
��� �⣺��1���Ա����Ӿ��л�ԭ�ԣ������е��������������ԣ������ᰱ��+4�۵�����л�ԭ�ԣ�
�ʴ�Ϊ����ֹ������隣�������
��2��A�������Ŀ����������������Ϊ����ƣ���A��ȷ��
B����Ӧ��ѧ����ʽΪ��CaSO4+4C=CaS+4CO������B��ȷ��
C����ֹ̼��������¶ȹ���ʱ�ֽ�ò�����Ҫ��Ŀ������C��ȷ��
D���Ȼ�狀�NԪ�أ���һ�ֵ��ʣ���D��ȷ��
�ʴ�Ϊ��ABCD��
���� ���⿼�������������ʼ����ʵ��Ʊ���Ϊ��Ƶ���㣬����ϰ���е���Ϣ�������ķ�ӦΪ���Ĺؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
17����1��ͼa�Ǹ��ݷ�ӦZn+CuSO4=Cu+ZnSO4��Ƴɵ�пͭԭ��أ��������Һ����ZnSO4���ZnSO4����CuSO4������Һ��Cu���ĵ缫��Ӧʽ��Cu2++2e-=Cu��

��2��ͼb�У����Ǽ���ȼ�ϵ�أ��������ҺΪKOH��Һ���Ľṹʾ��ͼ����ͬѧ���ڢ���ʵ�����϶�ͭ��
��a���缫�Ϸ����ĵ缫��Ӧ��CH4-8e-+10OH-=CO32-+7H2O��
����ʵ������Т��е�ͭƬ����������6.4g�����������������CH4���������״����0.56L��
����ͼ���еĢ��Ϊ�ö��Ե缫���200mL 0.05mol/L��CuSO4��Һ��һ��ʱ�����Һ�е�Cu2+ǡ����ȫ�������ָ������£���ҺpH=1�����Ե���������Һ����仯�������������������Һ�ָ�Ϊ����ǰ����Һ��ͬ�����Լ���һ��������b������ţ���
a��Cu b��CuO C��Cu��OH��2 d��CuSO4
��3����FeCl3������ӡˢ��·ͭ��ĸ�ʴ����
д��FeCl3��Һ��ʴӡˢ��·ͭ������ӷ���ʽ2Fe3++Cu=Cu2++2Fe2+��
�����˷�Ӧ��Ƴ�ԭ��أ���ԭ��صĸ�������ΪCu�������ϵĵ缫��ӦʽΪFe3++e-=Fe2+��
�ڸ�ʴͭ���Ļ����Һ�к�Cu2+��Fe3+��Fe2+��Ũ�Ⱦ�Ϊ0.10mol/L��������±����������ݺ�ҩƷ��������ȥCuCl2��Һ��Fe3+��Fe2+��ʵ�鲽�裺��ͨ������������Fe2+������Fe3+���ڼ���CuO������Һ��pH��3.2-4.7���۹��ˣ���ȥFe��OH��3����

��2��ͼb�У����Ǽ���ȼ�ϵ�أ��������ҺΪKOH��Һ���Ľṹʾ��ͼ����ͬѧ���ڢ���ʵ�����϶�ͭ��
��a���缫�Ϸ����ĵ缫��Ӧ��CH4-8e-+10OH-=CO32-+7H2O��
����ʵ������Т��е�ͭƬ����������6.4g�����������������CH4���������״����0.56L��
����ͼ���еĢ��Ϊ�ö��Ե缫���200mL 0.05mol/L��CuSO4��Һ��һ��ʱ�����Һ�е�Cu2+ǡ����ȫ�������ָ������£���ҺpH=1�����Ե���������Һ����仯�������������������Һ�ָ�Ϊ����ǰ����Һ��ͬ�����Լ���һ��������b������ţ���
a��Cu b��CuO C��Cu��OH��2 d��CuSO4
��3����FeCl3������ӡˢ��·ͭ��ĸ�ʴ����
д��FeCl3��Һ��ʴӡˢ��·ͭ������ӷ���ʽ2Fe3++Cu=Cu2++2Fe2+��
�����˷�Ӧ��Ƴ�ԭ��أ���ԭ��صĸ�������ΪCu�������ϵĵ缫��ӦʽΪFe3++e-=Fe2+��
�ڸ�ʴͭ���Ļ����Һ�к�Cu2+��Fe3+��Fe2+��Ũ�Ⱦ�Ϊ0.10mol/L��������±����������ݺ�ҩƷ��������ȥCuCl2��Һ��Fe3+��Fe2+��ʵ�鲽�裺��ͨ������������Fe2+������Fe3+���ڼ���CuO������Һ��pH��3.2-4.7���۹��ˣ���ȥFe��OH��3����
| ���ӣ�0.1mol/L�� | Cu2+ | Fe2+ | Fe3+ | �ṩ��ҩƷ��������Ҫѡ��ʹ�ã� |
| �������↑ʼ����pH | 4.7 | 7.0 | 1.9 | Cl2��NaOH��Һ��CuO��Cu |
| �������������ȫpH | 6.7 | 9.0 | 3.2 |
14�����и��������У���Ϊͬϵ����ǣ�������
| A�� | CH3-CH=CH2��  | |
| B�� |  �� ��  | |
| C�� | �ױ��Ͷ��ױ� | |
| D�� | CH2=CH-CH=CH2��CH3-CH2-CH2-C��CH |
1����ˮ�̲��ŷḻ����Դ�������йغ�ˮ�ۺ����õ�˵���У���ȷ���ǣ�������
| A�� | �Ӻ�ˮ�п���ȡʳ�� | |
| B�� | ��ˮ����ɵõ�ˮ | |
| C�� | ֱ�ӵ�⺣ˮ�ɵ�þ | |
| D�� | �Ӻ�ˮ�еõ���ˮ�ķ����������������������ӽ����� |
13����ҵ�������̿�[��Ҫ�ɷ�MnCO3����FeCO3��SiO2��Cu2��OH��2CO3����]Ϊԭ����ȡ�������̣�������ʾ��ͼ���£�

��֪ksp��CuS��=1.3��10-36��ksp��MnS��=1.95��10-13�������������������������������pH���
�ش��������⣺
��1��д������1����Ҫ�ɷֵ����ƶ������̣���Ҫ�ɷ�MnCO3��ϡ���ᷴӦ���ӷ���ʽΪMnCO3+2HCl=MnCl2+CO2��+H2O��
��2���Լ�1���ѡ��C ����ѡ����ĸ�����䷴Ӧ�����ӷ���ʽMnO2+2Fe2++4H+=Mn2++2Fe3++2H2O��
A���������� B��Ũ���� C���������� D����ˮ
�����Լ�2Ŀ���ǵ���pHֵ����ʱpHӦ�ÿ�����3.7��pH��4.7��Χ��
��3��д����Һ2�м���MnS������Ӧ�����ӷ���ʽMnS+Cu2+=Mn2++CuS���÷�Ӧ��ƽ�ⳣ��Ϊ1.5��1023��
��4���ö��Ե缫�����������Һ������ȡ�������̣�д�����ʱ�����ĵ缫��ӦʽMn2+-2e-+2H2O=4H++MnO2����ҵ���������ܽ�̼���̶����������ܽ⣬����Ҫ�ŵ�Ϊ�����ӷŵ������ж�������������SO42-���ᣮ

��֪ksp��CuS��=1.3��10-36��ksp��MnS��=1.95��10-13�������������������������������pH���
| Mn��OH��2 | Fe��OH��2 | Fe��OH��3 | Cu��OH��2 | |
| ��ʼ����ʱ | 8.3 | 6.3 | 2.7 | 4.7 |
| ��ȫ����ʱ | 9.8 | 8.3 | 3.7 | 6.7 |
��1��д������1����Ҫ�ɷֵ����ƶ������̣���Ҫ�ɷ�MnCO3��ϡ���ᷴӦ���ӷ���ʽΪMnCO3+2HCl=MnCl2+CO2��+H2O��
��2���Լ�1���ѡ��C ����ѡ����ĸ�����䷴Ӧ�����ӷ���ʽMnO2+2Fe2++4H+=Mn2++2Fe3++2H2O��
A���������� B��Ũ���� C���������� D����ˮ
�����Լ�2Ŀ���ǵ���pHֵ����ʱpHӦ�ÿ�����3.7��pH��4.7��Χ��
��3��д����Һ2�м���MnS������Ӧ�����ӷ���ʽMnS+Cu2+=Mn2++CuS���÷�Ӧ��ƽ�ⳣ��Ϊ1.5��1023��
��4���ö��Ե缫�����������Һ������ȡ�������̣�д�����ʱ�����ĵ缫��ӦʽMn2+-2e-+2H2O=4H++MnO2����ҵ���������ܽ�̼���̶����������ܽ⣬����Ҫ�ŵ�Ϊ�����ӷŵ������ж�������������SO42-���ᣮ
10����ȩ����ȩ����ȩ��ɵĻ�����У���Ԫ�ص�����������9%������Ԫ�ص����������ǣ�������
| A�� | 37% | B�� | 63% | C�� | 54% | D�� | ������ |
11���廯����һ����Ҫ�Ļ���ԭ�ϣ��Ʊ�CaBr2•2H2O ����Ҫ������ͼ������˵������ȷ���ǣ�������


| A�� | �Լ�M ��HBr������HBr��Ŀ���dz�ȥ������Ca��OH��2 | |
| B�� | ����IΪ���ˣ�����ΪFe��Fe��OH��2��Fe��OH��3��������Ϊ�ؽᾧ�������������Ϊ����Ũ������ȴ��Ʒ��ϴ�ӡ����� | |
| C�� | �Ƶõ�CaBr2•2H2O ����ͨ�����·����ⶨ���ȣ���ȡһ��������Ʒ����ˮ����������Na2CO3��Һ����ַ�Ӧ����ˣ�������ϴ�ӡ���ɡ���ȴ�������������ó�CaBr2•2H2O�Ĵ��� | |
| D�� | ��ҵ��Ҳ���Խ�����ͨ��ʯ���飬�������壬��65����з�Ӧ���Ƶ��廯�ƣ��˷�Ӧ�л�������һ����ɫ���壬�÷�Ӧ�Ļ�ѧ����ʽΪ3Ca��OH��2+3Br2+2NH3$\frac{\underline{\;\;��\;\;}}{\;}$3CaBr2+N2+6H2O |

