2. 四氧化三锰(Mn3O4)在电子工业有广泛应用.
四氧化三锰(Mn3O4)在电子工业有广泛应用.
(1)金属锰与氧气在一定条件下反应可以制得Mn3O4,反应原理如图所示.
石墨为正极,该电极反应式为O2+2H2O+4e-=4OH-(或O2+2H2O+4NH4++4e-=4NH3•H2O).
(2)Mn3O4的一种工业制法:在常温下,往硫酸锰溶液中加入氨水,
控制溶液的pH 为10,使Mn2+转化为Mn(OH)2 沉淀,过滤,在NH4Cl 溶液
催化下通入氧气将滤渣氧化为Mn3O4.
①滤液中Mn2+的浓度为1.9×10-5mol/L(Ksp[Mn(OH)2]=1.9×10-13).
②滤渣转化为Mn3O4的化学方程式为6Mn(OH)2+O2$\frac{\underline{\;NH_{4}Cl\;}}{\;}$2Mn3O4+6H2O.
(3)加热MnCO3会同时发生如下三个反应:
①a<0(填“>”、“=”或“<”).
②已知2CO(g)+O2(g)=2CO2(g)△H=d kJ•mol-1,则3MnO2+2CO(g)?Mn3O4(s)+2CO2(g) 的△H=(3c+b-3a)kJ/mol.
③在300℃条件下加热MnCO3 制取Mn3O4 并不合适,理由是:该温度下生成Mn3O4的反应平衡常数小,Mn3O4不是主要产物.800℃时,Mn2O3(s)+$\frac{1}{2}$O2(g)?MnO2(s) 的平衡常数K=$\frac{9}{16}$.
 四氧化三锰(Mn3O4)在电子工业有广泛应用.
四氧化三锰(Mn3O4)在电子工业有广泛应用.(1)金属锰与氧气在一定条件下反应可以制得Mn3O4,反应原理如图所示.
石墨为正极,该电极反应式为O2+2H2O+4e-=4OH-(或O2+2H2O+4NH4++4e-=4NH3•H2O).
(2)Mn3O4的一种工业制法:在常温下,往硫酸锰溶液中加入氨水,
控制溶液的pH 为10,使Mn2+转化为Mn(OH)2 沉淀,过滤,在NH4Cl 溶液
催化下通入氧气将滤渣氧化为Mn3O4.
①滤液中Mn2+的浓度为1.9×10-5mol/L(Ksp[Mn(OH)2]=1.9×10-13).
②滤渣转化为Mn3O4的化学方程式为6Mn(OH)2+O2$\frac{\underline{\;NH_{4}Cl\;}}{\;}$2Mn3O4+6H2O.
(3)加热MnCO3会同时发生如下三个反应:
| 序号 | 反应 | △H(kJ•mol-1) | K | |
| 300°C | 800°C | |||
| Ⅰ | MnCO3(s)+$\frac{1}{2}$O2(g)?MnO2(s)+CO2(g) | a | 3.0×107 | 1.8×105 |
| Ⅱ | MnCO3(s)+$\frac{1}{4}$O2(g)?$\frac{1}{2}$Mn2O3(s)+CO2(g) | b | 1.7×103 | 2.4×105 |
| Ⅲ | MnCO3(s)+$\frac{1}{6}$O2(g)?$\frac{1}{3}$Mn3O4(s)+CO2(g) | c | 9.8 | 9.6×104 |
②已知2CO(g)+O2(g)=2CO2(g)△H=d kJ•mol-1,则3MnO2+2CO(g)?Mn3O4(s)+2CO2(g) 的△H=(3c+b-3a)kJ/mol.
③在300℃条件下加热MnCO3 制取Mn3O4 并不合适,理由是:该温度下生成Mn3O4的反应平衡常数小,Mn3O4不是主要产物.800℃时,Mn2O3(s)+$\frac{1}{2}$O2(g)?MnO2(s) 的平衡常数K=$\frac{9}{16}$.
5. 常温下将NaOH溶液滴入二元弱酸H2X溶液中,混合溶液中的离子浓度与溶液pH的变化关系如图所示,下列叙述正确的是( )
常温下将NaOH溶液滴入二元弱酸H2X溶液中,混合溶液中的离子浓度与溶液pH的变化关系如图所示,下列叙述正确的是( )
 常温下将NaOH溶液滴入二元弱酸H2X溶液中,混合溶液中的离子浓度与溶液pH的变化关系如图所示,下列叙述正确的是( )
常温下将NaOH溶液滴入二元弱酸H2X溶液中,混合溶液中的离子浓度与溶液pH的变化关系如图所示,下列叙述正确的是( )| A. | Ka1(H2X)的数量级为10-7 | |
| B. | 曲线N表示lg$\frac{c(H{X}^{-})}{c({H}_{2}X)}$与pH的变化关系 | |
| C. | NaHX溶液中:c(H+)<c(OH-) | |
| D. | 当混合溶液呈中性时:c(Na+)>c(X2-)>c(HX-)>c(H+)=c(OH-) |
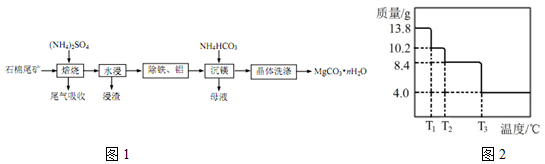
4.用海水制盐工业中的母液来生产金属镁的一种工艺流程如下:

下列说法错误的是( )

下列说法错误的是( )
| A. | 上述工艺流程中未涉及置换反应 | |
| B. | 设计步骤①、②、③的主要目的是富集MgCl2 | |
| C. | 脱水时在HCl气氛中进行可防止MgCl2发生水解 | |
| D. | 电解得到的炽热镁粉可在二氧化碳气氛中冷却 |
3.下列实验操作对应的现象及结论都正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 分别向饱和NaHCO3溶液和饱和NaHSO3溶液中滴加几滴酚酞试剂 | 前者溶液不变色,后者溶液变红 | 非金属:S>C |
| B | 甲烷与氯气的混合气在光照下反应,用湿润的蓝色石蕊试纸检验反应后生成的气体 | 湿润的蓝色石蕊试纸变红 | 甲烷的氯代物呈酸性 |
| C | 向NaAlO2溶液中持续通入气体Y | 先出现白色沉淀,最终沉淀又溶解 | Y可能是HCl |
| D | 向溴水中通入SO2 | 溴水橙黄色褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
1.实验室用H2还原SiHCl3(沸点:31.85℃)制备纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法正确的是( )


| A. | 装置Ⅱ、Ⅲ中依次盛装的是浓H2SO4、冰水 | |
| B. | 实验时,应先加热管式炉,再打开盛装稀硫酸的分液漏斗 | |
| C. | 为鉴定制得的硅中是否含微量铁单质,需要用到的试剂为盐酸、双氧水、硫氰化钾溶液 | |
| D. | 该实验中制备氢气的装置也可用于氢氧化钠稀溶液与氯化铵固体反应制备氨气 |
20.自然界中三种单萜的结构如图所示,下列说法不正确的是( )

0 163794 163802 163808 163812 163818 163820 163824 163830 163832 163838 163844 163848 163850 163854 163860 163862 163868 163872 163874 163878 163880 163884 163886 163888 163889 163890 163892 163893 163894 163896 163898 163902 163904 163908 163910 163914 163920 163922 163928 163932 163934 163938 163944 163950 163952 163958 163962 163964 163970 163974 163980 163988 203614

| A. | ①、③互为同分异构体 | B. | ②的分子式为C10H18O | ||
| C. | ①能使酸性高锰酸钾溶液褪色 | D. | ①、②、③都能与金属钠反应 |
 ,Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为1:1.
,Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为1:1.
 .
. .
. +nCO2$\stackrel{催化剂}{→}$
+nCO2$\stackrel{催化剂}{→}$
