3.室温下,向0.1mol氨水中逐滴加入盐酸,下列描述不正确的是( )
| A. | pH逐渐减小 | B. | $\frac{c(N{{H}_{4}}^{+})}{c(O{H}^{-})}$增大 | ||
| C. | 水的电离程度会不断增大 | D. | Kw不变 |
2.下列选用的仪器和药品能达到实验目的是( )
| A. |  可用于吸收NH3或HCl,并防止倒吸 | |
| B. | 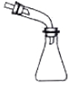 蒸馏时的接收装置 | |
| C. |  除去SO2中的少量HCl | |
| D. |  准确量取一定体积K2Cr2O7标准溶液 |
1.下列物质都能与足量的KI溶液(含少量硫酸)反应生成I2,当生成等量的I2时,消耗物质的量最小的是( )
| A. | H2O2 | B. | FeCl3 | C. | KMnO4 | D. | KIO3 |
20.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 60g丙醇含有的共价键数目为10 NA | |
| B. | 常温常压下,4.4 g CO2与N2O混合气体中含有的原子总数为0.3NA | |
| C. | 在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4 NA | |
| D. | 80 mL 10 mol/L盐酸与足量MnO2加热反应,产生Cl2的分子数为0.2 NA |
19.NA表示阿佛加德罗常数.下列说法中不正确的是( )
| A. | 常温常压下,4.5g${\;}_{7}^{15}$N${\;}_{3}^{+}$所含电子数为2NA个 | |
| B. | 1molFeCl3跟沸水完全反应转化为氢氧化铁胶体,其中胶体粒子的数目是NA | |
| C. | 4.5gSiO2晶体中含有的硅氧键数目为0.3NA | |
| D. | 氧气和臭氧的混合物1.6 g中含有0.1NA氧原子 |
18.设 NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 0.1 mol MnO2与 40 mL 10 mol/L 的浓盐酸充分反应,生成的氯气分子数为 01NA | |
| B. | 0.1mol 铁粉与足量水蒸气反应生成的 H2 分子数目为 0.1NA | |
| C. | 分子数目为 0.1NA的 N2 和 NH3 混合气体,原子间含有的共用电子对数目为 0.3NA | |
| D. | 用惰性电极电解 CuSO4 溶液一段时间后,若加入 0.05mol 的 Cu2(OH)2CO3 固体恰好能使溶液恢复到原来的浓度,则该电解过程中转移电子的数目为 0.2NA |
17. 常温下,向 100mL0.01mol•L-1HA 溶液中逐滴加入0.02mol•L-1MOH 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).下列叙述一定正确的是( )
常温下,向 100mL0.01mol•L-1HA 溶液中逐滴加入0.02mol•L-1MOH 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).下列叙述一定正确的是( )
 常温下,向 100mL0.01mol•L-1HA 溶液中逐滴加入0.02mol•L-1MOH 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).下列叙述一定正确的是( )
常温下,向 100mL0.01mol•L-1HA 溶液中逐滴加入0.02mol•L-1MOH 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).下列叙述一定正确的是( )| A. | 由图中信息可知HA为弱酸 | |
| B. | 在N点pH=7,酸碱恰好完全反应 | |
| C. | 常温时一定浓度的MA稀溶液显中性 | |
| D. | K 点对应的溶液中,c(M+)+c(MOH)=2c (A-) |
15.分子式为C5H12O,分子中含有3个甲基,且能与金属钠反应的有机物共有(不考虑立体异构)( )
0 163655 163663 163669 163673 163679 163681 163685 163691 163693 163699 163705 163709 163711 163715 163721 163723 163729 163733 163735 163739 163741 163745 163747 163749 163750 163751 163753 163754 163755 163757 163759 163763 163765 163769 163771 163775 163781 163783 163789 163793 163795 163799 163805 163811 163813 163819 163823 163825 163831 163835 163841 163849 203614
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
