10.电解Na2SO3溶液,可再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨).下列说法正确的是( )


| A. | 电解过程中若消耗12.6gNa2SO3,则阴极区变化的质量为4.4g (假设该过程中所有液体进出口密闭) | |
| B. | b放电的电极反应式为SO32-+H2O-e-═SO42-+2H+ | |
| C. | 电子由a经内电路流向b电极 | |
| D. | 图中b极连接电源的正极,C 口流出的物质是亚硫酸 |
9.在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2mol A和1mol B,发生反应:2A(g)+B(g)?2D(g)△H=Q kJ•mol-1.相关条件和数据见下表:下列说法正确的是( )
| 实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应温度/℃ | 700 | 700 | 750 |
| 达平衡时间/min | 40 | 5 | 30 |
| n(D)平衡/mol | 1.5 | 1.5 | 1 |
| 化学平衡常数 | K1 | K2 | K3 |
| A. | K3>K2=K1 | |
| B. | 实验Ⅱ可能使用了催化剂 | |
| C. | 实验Ⅲ达平衡后容器内的压强是实验Ⅰ的$\frac{9}{10}$倍 | |
| D. | 实验Ⅲ达平衡后,恒温下再向容器中通入1 mol A和1 mol D,平衡不移动 |
8. 常温下用0.10mol•L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol•L-1CH3COOH(Ka=1.75×10-5)溶液和HCN(Ka=4.9×10-10)溶液所得滴定曲线如图.下列说法正确的是( )
常温下用0.10mol•L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol•L-1CH3COOH(Ka=1.75×10-5)溶液和HCN(Ka=4.9×10-10)溶液所得滴定曲线如图.下列说法正确的是( )
 常温下用0.10mol•L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol•L-1CH3COOH(Ka=1.75×10-5)溶液和HCN(Ka=4.9×10-10)溶液所得滴定曲线如图.下列说法正确的是( )
常温下用0.10mol•L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol•L-1CH3COOH(Ka=1.75×10-5)溶液和HCN(Ka=4.9×10-10)溶液所得滴定曲线如图.下列说法正确的是( )| A. | 曲线I和曲线II分别代表的是CH3COOH和HCN | |
| B. | 点③和点⑤所示溶液中由水电离出的c(H+):⑤>③ | |
| C. | 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH) | |
| D. | 在点②和③之间(不包括端点)存在关系:c(Na+)>c(A-)>c(H+)>c(OH-) (A-代表溶液中的酸根离子) |
7.已知X-离子含a个中子,X元素的质量数为b,则c克X-离子含电子的物质的量为( )mol.
| A. | $\frac{c(b-a)}{b}$ | B. | $\frac{c(b-a+1)}{b}$ | C. | $\frac{b-a+1}{a•b}$ | D. | $\frac{c(b-a-1)}{b}$ |
6.CO2的转换在生产、生活中具有重要的应用.
(1)CO2的低碳转型对抵御气候变化具有重要意义,海洋是地球上碳元素最大的“吸收池”.
①溶于海水中的CO2主要以四种无机碳形式存在,除CO2、H2CO3两种分子外,还有两种离子的化学式为HCO3-、CO32-.
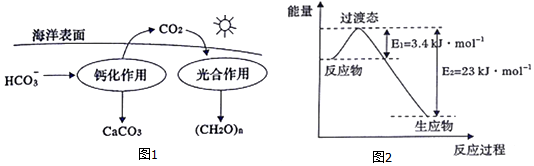
②在海洋碳循环中,可通过图1所示的途径固碳.写出钙化作用的离子方程式:Ca2++2HCO3-═CaCO3↓+CO2↑+H2O.
(2)将CO2与金属钠组合设计成Na-CO2电池,很容易实现可逆的充、放电反应,该电池反应为4Na+3CO2 $?_{放电}^{放电}$2Na2CO3+C.放电时,在正极得电子的物质为CO2;充电时,阳极的反应式为C-4e-+2CO32-═3CO2.
(3)目前工业上有一种方法是用CO2和H2在230℃并有催化剂条件下转化生成甲醇蒸汽和水蒸气.图2表示恒压容器中0.5molCO2和1.5mol H2转化率达80%时的能量变化示意图.能判断该反应达到化学平衡状态的依据B、D(填字母).
A.容器中压强不变 B.H2的体积分数不变
C.c(H2=3c(CH3OH) D.容器中密度不变
E.2个C=O断裂的同时有6个H-H断裂
(4)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表三组数据:
①实验2条件下平衡常数K=$\frac{1}{6}$.
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b的值<1 (填具体值或取值范围).
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时v(正<v(逆)(填“<”、“>”或“=“).
(5)已知在常温常压下:
①2CH3OH(I)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ•mol-1
③H2O(g)=H2O(I)△H=-44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=-442.8kJ/mol.
(1)CO2的低碳转型对抵御气候变化具有重要意义,海洋是地球上碳元素最大的“吸收池”.
①溶于海水中的CO2主要以四种无机碳形式存在,除CO2、H2CO3两种分子外,还有两种离子的化学式为HCO3-、CO32-.
②在海洋碳循环中,可通过图1所示的途径固碳.写出钙化作用的离子方程式:Ca2++2HCO3-═CaCO3↓+CO2↑+H2O.
(2)将CO2与金属钠组合设计成Na-CO2电池,很容易实现可逆的充、放电反应,该电池反应为4Na+3CO2 $?_{放电}^{放电}$2Na2CO3+C.放电时,在正极得电子的物质为CO2;充电时,阳极的反应式为C-4e-+2CO32-═3CO2.
(3)目前工业上有一种方法是用CO2和H2在230℃并有催化剂条件下转化生成甲醇蒸汽和水蒸气.图2表示恒压容器中0.5molCO2和1.5mol H2转化率达80%时的能量变化示意图.能判断该反应达到化学平衡状态的依据B、D(填字母).

A.容器中压强不变 B.H2的体积分数不变
C.c(H2=3c(CH3OH) D.容器中密度不变
E.2个C=O断裂的同时有6个H-H断裂
(4)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b的值<1 (填具体值或取值范围).
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时v(正<v(逆)(填“<”、“>”或“=“).
(5)已知在常温常压下:
①2CH3OH(I)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ•mol-1
③H2O(g)=H2O(I)△H=-44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=-442.8kJ/mol.
4. 某同学设计如图所示装置,用电解法把Na2CrO4溶液转变为Na2Cr2O7溶液(2CrO42-+2H+═Cr2O72-+H2O).下列说法正确的是( )
某同学设计如图所示装置,用电解法把Na2CrO4溶液转变为Na2Cr2O7溶液(2CrO42-+2H+═Cr2O72-+H2O).下列说法正确的是( )
 某同学设计如图所示装置,用电解法把Na2CrO4溶液转变为Na2Cr2O7溶液(2CrO42-+2H+═Cr2O72-+H2O).下列说法正确的是( )
某同学设计如图所示装置,用电解法把Na2CrO4溶液转变为Na2Cr2O7溶液(2CrO42-+2H+═Cr2O72-+H2O).下列说法正确的是( )| A. | A为正极,B为负极 | |
| B. | 电解过程中,电解槽左侧溶液pH增大 | |
| C. | 电解过程中,Na+在电解槽中自左向右迁移 | |
| D. | 当电路中通过lmol电子时,阴极生成0.5mol Na2Cr2O7 |
3.已知常温下反应①、②、③的平衡常数关系为K1>K3>K2,据此所做以下推测合理的是 ( )
①NH3+H+?NH4+ (平衡常数为K1)
②Ag++Cl-?AgCl(平衡常数为K2)
③Ag++2NH3?Ag(NH3)2+(平衡常数为K3)
①NH3+H+?NH4+ (平衡常数为K1)
②Ag++Cl-?AgCl(平衡常数为K2)
③Ag++2NH3?Ag(NH3)2+(平衡常数为K3)
| A. | 氯化银可溶于氨水 | |
| B. | 银氨溶液中加入少量氯化钠有白色沉淀 | |
| C. | 银氨溶液中加入盐酸有白色沉淀 | |
| D. | 银氨溶液可在酸性条件下稳定存在 |
2.向盛有1mL 0.1mol•L-1MgCl2溶液的试管中滴加1mL 0.2mol•L-1氨水,观察到有白色沉淀生成,再滴加1mL 0.1mol•L-1FeCl3溶液,发现白色沉淀转化为红褐色沉淀.由以上现象可以推知,下列叙述不正确的是( )
0 163570 163578 163584 163588 163594 163596 163600 163606 163608 163614 163620 163624 163626 163630 163636 163638 163644 163648 163650 163654 163656 163660 163662 163664 163665 163666 163668 163669 163670 163672 163674 163678 163680 163684 163686 163690 163696 163698 163704 163708 163710 163714 163720 163726 163728 163734 163738 163740 163746 163750 163756 163764 203614
| A. | 白色沉淀转化为红褐色沉淀的离子方程式是:3Mg(OH)2+2Fe3+=3Mg2++2Fe(OH)3 | |
| B. | 上述实验说明:Mg(OH)2的KSP大于Fe(OH)3的KSP | |
| C. | 最后所得溶液中:c (Cl-)=c (NH4+)+2c (Mg2+)+3c (Fe3+) | |
| D. | 最后所得溶液中:c (Cl-)>c (NH4+)>c (Mg2+)>c (Fe3+) |
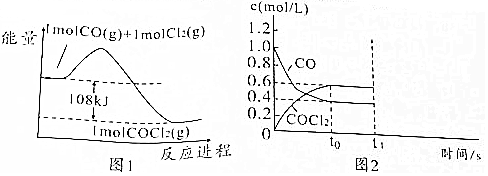
 ;光气遇水后生成两种气体,其中一种气体极易溶于水,反应的化学方程式为COCl2+H2O═2HCl+CO2;
;光气遇水后生成两种气体,其中一种气体极易溶于水,反应的化学方程式为COCl2+H2O═2HCl+CO2;