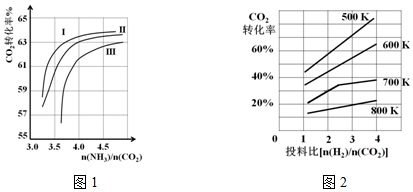
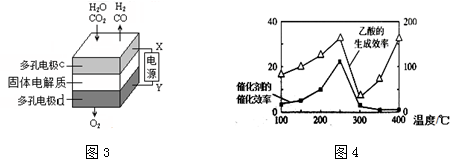
13.25℃时,下列有关说法正确的是( )
| A. | 同浓度、同体积的强酸与强碱溶液混合后,溶液的 pH 一定等于 7 | |
| B. | 0.1 mol•L-1 NH4Cl 溶液与 0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 向 0.10 mol•L-1Na2SO3溶液中通 SO2 气体至溶液 pH=7:c(Na+)═2c(SO32-)+c(HSO3-) | |
| D. | 0.1 mol AgCl 和 0.1 mol AgBr 混合后加入水中,所得溶液 c(Cl-)═c(Br-) |
12.设NA为阿伏加德罗常数.下列说法正确的是( )
| A. | 0.1 molFe和0.1molCu分别与0.1molCl2完全反应,转移的电子数均为0.2NA个 | |
| B. | 4.6g有机物C2H6O的分子结构中含有的C-H键数目一定为0.5NA | |
| C. | 1 mol FeCl3 水解生成的Fe(OH)3胶粒数为NA | |
| D. | 64 g SO2与过量的O2在一定条件下反应生成的SO3分子数为NA |
11.化学与生产、生活、社会发展等息息相关.下列说法正确的是( )
| A. | 为补充土壤中的钾元素,可在田间焚烧秸秆 | |
| B. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 | |
| C. | 石油的分馏、催化裂化、裂解等石油加工方法,其目的均为得到更多的汽油 | |
| D. | 做衣服的棉和麻灼烧有烧焦羽毛的气味 |
10.下列说法不正确的是( )
| A. | 石油裂解的目的是为了获得碳原子数少的轻质油 | |
| B. | lmol葡萄糖与足量的金属钠反应,最多可生成2.5molH2 | |
| C. | C3H8和C5Hl2一定互为同系物 | |
| D. | 油脂是食物中产生能量最高的营养物质 |
9.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温下,3.65gHCl与1.7gNH3混合后,气体分子总数是0.2NA | |
| B. | 100g 98%的浓硫酸中含有的氧原子数目为4 NA | |
| C. | 1mol乙酸(忽略挥发损失)与足量的C2H518OH在浓硫酸作用下加热,充分反应可生成NA个CH3CO18OC2H5分子 | |
| D. | 氯碱工业中,每转移2NA个电子,可以产生标况下44.8L气体 |
8.二氧化碳是引起“温室效应”的主要物质.高效利用能源,能够减少二氧化碳的排放.
I.在一定温度下的2L固定容积的密闭容器中,通入2mol CO2和3mol H2,发生的反应为CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-a kJ•mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
①不能说明该反应已达平衡状态的是D.(填编号)
A.CO2的体积分数在混合气体中保持不变
B.混合气体的平均相对分子质量不随时间的变化而变化
C.单位时间内每消耗1.2mol H2,同时消耗0.4mol H2O
D.反应中H2O与CH3OH的物质的量浓度之比为1:1,且保持不变
②从0min到10min,v(H2)=0.075 mol•L-1•min-1.
③下列措施中不能使$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大的是C(填编号).
A.降低温度 B.将H2O(g)从体系中分离
C.恒温恒容下充入He(g) D.恒温恒容再充入2mol CO2和3mol H2
④计算该温度下此反应的平衡常数K=0.20 L2/mol2_(保留两位有效数字).
II.为进一步探究CO2与NaCN溶液反应的产物,查得数据如下:
①25℃时,测得HCN和NaCN的混合溶液的pH=11,则c(HCN)/c(CN-)=$\frac{1}{49}$(可用分数表示).
②向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:CN-+CO2+H2O=HCN+HCO3-.
III.(1)有一种利用CO2生产甲醇燃料的方法:
已知:CO2(g)+3H2(g)═CH3OH(g)+H2O(l)△H=-a kJ•mol-1;
CH3OH(g)═CH3OH(l)△H=-b kJ•mol-1;
2H2(g)+O2(g)═2H2O(l)△H=-c kJ•mol-1;
则表示CH3OH(l) 燃烧热的热化学方程式为CH3OH(l)+3/2O2(g)═CO2(g)+2H2O(l)△H=-($\frac{3}{2}$c-a-b) kJ•mol-1.
(2)某甲醇燃料电池原理如图2所示.
①M区发生反应的电极反应式为CH3OH-6e-+H2O=CO2+6H+.
②用上述电池做电源,用图3装置电解饱和食盐水(电极均为惰性电极),假设溶液体积为300mL(体积变化忽略),当溶液的pH值变为13时(在常温下测定),理论上消耗甲醇的质量为0.16g.

I.在一定温度下的2L固定容积的密闭容器中,通入2mol CO2和3mol H2,发生的反应为CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-a kJ•mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
①不能说明该反应已达平衡状态的是D.(填编号)
A.CO2的体积分数在混合气体中保持不变
B.混合气体的平均相对分子质量不随时间的变化而变化
C.单位时间内每消耗1.2mol H2,同时消耗0.4mol H2O
D.反应中H2O与CH3OH的物质的量浓度之比为1:1,且保持不变
②从0min到10min,v(H2)=0.075 mol•L-1•min-1.
③下列措施中不能使$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大的是C(填编号).
A.降低温度 B.将H2O(g)从体系中分离
C.恒温恒容下充入He(g) D.恒温恒容再充入2mol CO2和3mol H2
④计算该温度下此反应的平衡常数K=0.20 L2/mol2_(保留两位有效数字).
II.为进一步探究CO2与NaCN溶液反应的产物,查得数据如下:
| 化学式 | 电离平衡常数(25℃) |
| HCN | K=4.9×10-10 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
②向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:CN-+CO2+H2O=HCN+HCO3-.
III.(1)有一种利用CO2生产甲醇燃料的方法:
已知:CO2(g)+3H2(g)═CH3OH(g)+H2O(l)△H=-a kJ•mol-1;
CH3OH(g)═CH3OH(l)△H=-b kJ•mol-1;
2H2(g)+O2(g)═2H2O(l)△H=-c kJ•mol-1;
则表示CH3OH(l) 燃烧热的热化学方程式为CH3OH(l)+3/2O2(g)═CO2(g)+2H2O(l)△H=-($\frac{3}{2}$c-a-b) kJ•mol-1.
(2)某甲醇燃料电池原理如图2所示.
①M区发生反应的电极反应式为CH3OH-6e-+H2O=CO2+6H+.
②用上述电池做电源,用图3装置电解饱和食盐水(电极均为惰性电极),假设溶液体积为300mL(体积变化忽略),当溶液的pH值变为13时(在常温下测定),理论上消耗甲醇的质量为0.16g.

7.能与铝作用放出氢气的溶液中,可能大量共存的离子组是( )
| A. | NH4+、Mg2+、NO3-、Cl- | B. | Cu2+、Na+、HCO3-、Br- | ||
| C. | Na+、Fe2+、SO42-、NO3- | D. | K+、Na+、AlO2-、Cl- |
6.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol CH5+(碳正离子)中含有的电子数为11NA | |
| B. | 6.8g熔融的KHSO4中含有0.1NA个阳离子 | |
| C. | 质量相等、密度不等的N2和C2H4两种气体所含的分子数均为NA | |
| D. | 室温下,42.0g乙烯和丙烯的混合气体中含有的碳原子数为3NA |
5.下列物质间相互发生反应时:①Na+O2②Fe+O2③AgNO3溶液+氨水④HCOOH+Cu(OH)2 ⑤KI溶液+AgNO3溶液 ⑥ ⑦Na2CO3+C6H5COOH ⑧AlCl3+KOH ⑨P+Cl2⑩Cu+HNO3;在不同条件下得到不同产物的是( )
⑦Na2CO3+C6H5COOH ⑧AlCl3+KOH ⑨P+Cl2⑩Cu+HNO3;在不同条件下得到不同产物的是( )
0 163516 163524 163530 163534 163540 163542 163546 163552 163554 163560 163566 163570 163572 163576 163582 163584 163590 163594 163596 163600 163602 163606 163608 163610 163611 163612 163614 163615 163616 163618 163620 163624 163626 163630 163632 163636 163642 163644 163650 163654 163656 163660 163666 163672 163674 163680 163684 163686 163692 163696 163702 163710 203614
 ⑦Na2CO3+C6H5COOH ⑧AlCl3+KOH ⑨P+Cl2⑩Cu+HNO3;在不同条件下得到不同产物的是( )
⑦Na2CO3+C6H5COOH ⑧AlCl3+KOH ⑨P+Cl2⑩Cu+HNO3;在不同条件下得到不同产物的是( )| A. | 除⑤ | B. | 除②⑤ | C. | 除④⑥ | D. | 除④⑤⑥ |