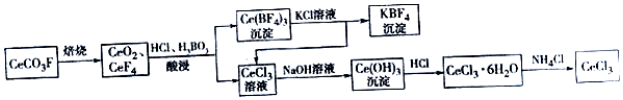
6. 茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素的有关叙述正确的是( )
茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素的有关叙述正确的是( )
 茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素的有关叙述正确的是( )
茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素的有关叙述正确的是( )| A. | 分子式为C15H13O7 | |
| B. | 1 mol儿茶素A在一定条件下最多能与7molH2加成 | |
| C. | 等质量的儿茶素A分别与足量的金属钠和氢氧化钠反应,消耗金属钠和氢氧化钠的物质的量之比为1:1 | |
| D. | 1 mol儿茶素A与足量的浓溴水反应,最多消耗Br24 mol |
5.用惰性电极电解FeSO4溶液制备高纯铁的原理如图所示.下列说法错误的是( )
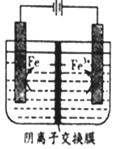

| A. | .阳极主要发生反应:Fe2+-e-═Fe3+ | |
| B. | 可用高纯铁电极作阴扱 | |
| C. | .电解液中的SO42-由右向左通过阴离子交换膜 | |
| D. | .电解法制备髙纯铁总反应:3Fe2+$\frac{\underline{\;通电\;}}{\;}$Fe+2Fe3+ |
4.在Na+浓度为0.5mol•L-1的某澄清溶液中,还可能含有K+、Ag+、Al3+、Ba2+、NO3-、CO32-、SO32-、SiO32-、SO42-等离子,取该溶液100mL进行如图连续实验(所加试剂均过量,气体全部逸出).下列说法不正确的是
( )

( )

| A. | 原溶液中一定不存在Ag+、Al3+、Ba2+、SO42- | |
| B. | 实验中生成沉淀的离子方程式是SiO32-+2H+=H2SiO3↓ | |
| C. | 原溶液一定存在K+、CO32-,可能存在NO3- | |
| D. | 原溶液不存在NO3-时,c(K+)=0.8mol•L-1 |
3.硫酸亚铁常用于制造铁氧体、净水、聚合催化剂、照相制版.某化学兴趣小组在通风环境进行以下探究.回答有关问题:
(1)利用废铁屑(含少量氧化铝、氧化铁等)制取硫酸亚铁晶体用图1所示过程进行实验.

①氧化铝与热烧碱液反应的离子方程式为Al2O3+2OH-+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$2[Al(OH)4]-.
②实验过程中需要用到的玻璃仪器有BC(填标号).
A.分液漏斗B.胶头滴管C.玻璃棒D.坩埚
③FeSO4的溶解度随温度变化的曲线如图2,两次水浴加热的温度均应控制在63℃的原因为为增大FeSO4溶解度,增大产率.
④操作X为趁热过滤.
(2)探究硫酸亚铁分解产物
已知:i 硫酸盐热分解的气体产物可能有SO2、SO3和O2.
ii SO3、SO2的沸点依次为44.8℃、-10℃,S03的熔点为16.8℃.
按图3所示的装置进行实验.
①装置C的作用为安全瓶,防倒吸.
②能证明气体产物仅有SO3和SO2的实验现象为B中有晶体生成,D中不产生白色沉淀,E中溶液颜色变浅.
③探究固体产物中铁的氧化物形式
假设一:只有Fe2O3;假设二:只有Fe3O4;假设三:Fe2O3和Fe3O4均有
为验证上述假设,完成下列定量实验.
(1)利用废铁屑(含少量氧化铝、氧化铁等)制取硫酸亚铁晶体用图1所示过程进行实验.

①氧化铝与热烧碱液反应的离子方程式为Al2O3+2OH-+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$2[Al(OH)4]-.
②实验过程中需要用到的玻璃仪器有BC(填标号).
A.分液漏斗B.胶头滴管C.玻璃棒D.坩埚
③FeSO4的溶解度随温度变化的曲线如图2,两次水浴加热的温度均应控制在63℃的原因为为增大FeSO4溶解度,增大产率.
④操作X为趁热过滤.
(2)探究硫酸亚铁分解产物
已知:i 硫酸盐热分解的气体产物可能有SO2、SO3和O2.
ii SO3、SO2的沸点依次为44.8℃、-10℃,S03的熔点为16.8℃.
按图3所示的装置进行实验.
①装置C的作用为安全瓶,防倒吸.
②能证明气体产物仅有SO3和SO2的实验现象为B中有晶体生成,D中不产生白色沉淀,E中溶液颜色变浅.
③探究固体产物中铁的氧化物形式
假设一:只有Fe2O3;假设二:只有Fe3O4;假设三:Fe2O3和Fe3O4均有
为验证上述假设,完成下列定量实验.
| 步骤 | 操作 | 结论 |
| 1 | 将1.6g固体产物溶于过量稀硫酸 | 假设一成立 |
| 2 | 往步骤1所得溶液中先加入足量双氧水,再加入足量NaOH溶液并充分搅拌 | |
| 3 | 过滤、洗涤、干燥灼烧至恒重 | |
| 4 | 称得最终固体质量为1.6g |
19.环境保护为当今首要的社会问题,下列叙述错误的是( )
| A. | CO2含量增加会导致温室效应 | |
| B. | 为减少木材的使用,使用聚氯乙烯生产包装盒 | |
| C. | 装修材料中的甲醛、芳香烃等会造成污染 | |
| D. | 天然气代替煤作燃料可减少环境污染 |
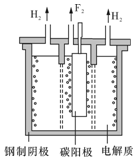
18. 在通电条件下,用如图所示装置由乙二醛(OHC-CHO)反应制备乙二酸(HOOC-COOH).其制备反应为:OHC-CHO+2Cl2+2H2O→HOOC-COOH+4HCl.下列说法正确的是( )
在通电条件下,用如图所示装置由乙二醛(OHC-CHO)反应制备乙二酸(HOOC-COOH).其制备反应为:OHC-CHO+2Cl2+2H2O→HOOC-COOH+4HCl.下列说法正确的是( )
 在通电条件下,用如图所示装置由乙二醛(OHC-CHO)反应制备乙二酸(HOOC-COOH).其制备反应为:OHC-CHO+2Cl2+2H2O→HOOC-COOH+4HCl.下列说法正确的是( )
在通电条件下,用如图所示装置由乙二醛(OHC-CHO)反应制备乙二酸(HOOC-COOH).其制备反应为:OHC-CHO+2Cl2+2H2O→HOOC-COOH+4HCl.下列说法正确的是( )| A. | 每消耗0.lmol乙二醛,在Pt1极放出2.24L气体(标准状况) | |
| B. | Pt1的电极反应为:4OH--4e-=2H2O+O2↑ | |
| C. | 每得到1mol乙二酸将有2molH+从右室迁移到左室 | |
| D. | 盐酸是起提供Cl-和增强导电性的作用 |
17.一些烷烃的燃烧热(kJ/mol)如表:下列表达正确的是( )
0 163126 163134 163140 163144 163150 163152 163156 163162 163164 163170 163176 163180 163182 163186 163192 163194 163200 163204 163206 163210 163212 163216 163218 163220 163221 163222 163224 163225 163226 163228 163230 163234 163236 163240 163242 163246 163252 163254 163260 163264 163266 163270 163276 163282 163284 163290 163294 163296 163302 163306 163312 163320 203614
| 化合物 | 燃烧热 | 化合物 | 燃烧热 |
| 甲烷 | 891.0 | 正丁烷 | 2878.0 |
| 乙烷 | 1560.8 | 异丁烷 | 2869.6 |
| 丙烷 | 2221.5 | 2-甲基丁烷 | 3531.3 |
| A. | 乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g)△H=-1560.8 kJ/mol | |
| B. | 稳定性:正丁烷>异丁烷 | |
| C. | 正戊烷的燃烧热大于3531.3kJ/mol | |
| D. | 相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |

 .
.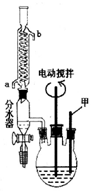 苯甲酸(C6H5COOH式量:122,熔点122.4℃,密度为1.2659g•cm-3)是一种一元有机弱酸,微溶于水易溶于乙醇.实验室中由甲苯(式量:92,密度为0.8669g•cm-3)制备苯甲酸的实验如下:
苯甲酸(C6H5COOH式量:122,熔点122.4℃,密度为1.2659g•cm-3)是一种一元有机弱酸,微溶于水易溶于乙醇.实验室中由甲苯(式量:92,密度为0.8669g•cm-3)制备苯甲酸的实验如下: