2.将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,下列叙述正确的是( )

| A. | 装置甲中铜片表面产生气泡 | |
| B. | 装置甲中正极的电极反应式:2H++2eˉ=H2↑ | |
| C. | 装置乙中电流从铜片经导线流向锌片 | |
| D. | 装置乙溶液中SO42ˉ向铜片做定向移动 |
1.下列说法中正确的是( )
| A. | 任何化学反应都能设计成原电池 | |
| B. | 手机上用的锂离子电池属于一次电池 | |
| C. | 原电池中的阳离子向负极移动 | |
| D. | 把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
20.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 常温常压下,14 g丙烯和环丙烷混合气体中碳原子数为NA | |
| B. | 标准状况下,11.2 L乙烷含有共价键数为3NA | |
| C. | 密闭容器中充入1 mol I2(g)和2 mol H2(g)充分反应,生成HI分子数为2NA | |
| D. | Na2O2与CO2反应时,生成0.5 mol O2转移的电子数为2NA |
19.纵观古今,化学与生活皆有着密切联系.下列有关说法错误的是( )
| A. | “梨花淡自柳深青,柳絮飞时花满城”中柳絮的主要成分和棉花的相同 | |
| B. | 制作烟花的过程中常加入金属发光剂和发色剂使烟花放出五彩缤纷的颜色 | |
| C. | 草莓棚中使用的“吊袋式二氧化碳气肥”的主要成分可以是碳酸钙 | |
| D. | 芒硝晶体(Na2SO4•10H2O)白天在阳光下曝晒后失水、溶解吸热,晚上重新结晶放热,实现了太阳能转化为化学能继而转化为热能 |
18.表是元素周期表的一部分,针对所给的10种元素,完成下列各小题.
(1)第3周期中金属性最强的元素是钙(填元素名称);
(2)S原子结构示意图为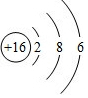 ;
;
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是HClO4(填化学式);
(4)C、N和O原子半径由小到大的顺序的是O<N<C;
(5)第3周期中气态氢化物最稳定的是HCl;
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是SiO2,常用于制造光导纤维(填一种高性能的现代通讯材料的名称);
(7)N元素形成的一种氢化物的化学式是NH3,俗话说“雷雨发庄稼”,请写出二氧化氮溶 于水的反应3NO2+H2O═2HNO3+NO.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
(2)S原子结构示意图为
 ;
;(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是HClO4(填化学式);
(4)C、N和O原子半径由小到大的顺序的是O<N<C;
(5)第3周期中气态氢化物最稳定的是HCl;
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是SiO2,常用于制造光导纤维(填一种高性能的现代通讯材料的名称);
(7)N元素形成的一种氢化物的化学式是NH3,俗话说“雷雨发庄稼”,请写出二氧化氮溶 于水的反应3NO2+H2O═2HNO3+NO.
17.下列属于含共价键的离子化合物是( )
| A. | H2O | B. | CaCl2 | C. | NaOH | D. | CO2 |
16.设NA为阿伏加德罗常数值,下列说法正确的是( )
| A. | 1 L 0.5 mol/L NaHCO3溶液中含有的HCO3-数目小于0.5 NA | |
| B. | 11.2 g 铁粉与硝酸反应失去电子数一定为0.6 NA | |
| C. | 25℃时,pH=13的 Ba(OH)2溶液中含有的OH-数目为0.2 NA | |
| D. | 46 g甲苯含有C=C双键的数目为1.5 NA |
15.设NA为阿伏伽德罗常数的值,则下列说法正确的是( )
0 163043 163051 163057 163061 163067 163069 163073 163079 163081 163087 163093 163097 163099 163103 163109 163111 163117 163121 163123 163127 163129 163133 163135 163137 163138 163139 163141 163142 163143 163145 163147 163151 163153 163157 163159 163163 163169 163171 163177 163181 163183 163187 163193 163199 163201 163207 163211 163213 163219 163223 163229 163237 203614
| A. | 0.4mol AgNO3受热完全分解(2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑),用排水法最终收集到气体的分子数为0.2NA | |
| B. | 6.4g CaC2中含有的离子总数目为0.3NA | |
| C. | 1 mol FeI2与一定量氯气反应时,若已知有1mol Fe2+被氧化则转移的电子数为3NA | |
| D. | 1mol 苯和苯甲酸的混合物完全燃烧时消耗O2的分子数为7.5NA |
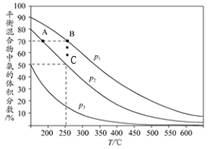 氨在国民经济中占有重要地位.
氨在国民经济中占有重要地位.