题目内容
20.设NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 常温常压下,14 g丙烯和环丙烷混合气体中碳原子数为NA | |
| B. | 标准状况下,11.2 L乙烷含有共价键数为3NA | |
| C. | 密闭容器中充入1 mol I2(g)和2 mol H2(g)充分反应,生成HI分子数为2NA | |
| D. | Na2O2与CO2反应时,生成0.5 mol O2转移的电子数为2NA |
分析 A、丙烯和环丙烷的最简式均为CH2;
B、求出乙烷的物质的量,然后根据乙烷中含7条共价键来分析;
C、碘和氢气的反应为可逆反应;
D、过氧化钠和二氧化碳反应时,氧元素由-1价变为0价从而生成氧气.
解答 解:A、丙烯和环丙烷的最简式均为CH2,故14g混合物中含有的CH2的物质的量为1mol,则含NA个碳原子,故A正确;
B、标况下11.2L乙烷的物质的量为0.5mol,而乙烷中含7条共价键,故0.5mol乙烷中含3.5NA条共价键,故B错误;
C、碘和氢气的反应为可逆反应,故不能进行彻底,则生成的HI分子个数小于2NA个,故C错误;
D、过氧化钠和二氧化碳反应时,氧元素由-1价变为0价从而生成氧气,故当生成0.5mol氧气时反应转移1mol即NA个电子,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
10.1mol下列物质中共用电子对数目最少是( )
| A. | N2 | B. | 金刚石 | C. | HCN | D. | CO2 |
11. 甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
 甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )| A. | 丙与戊的原子序数相差28 | |
| B. | 气态氢化物的稳定性:庚<己<戊 | |
| C. | 常温下,甲和乙的单质均能与水剧烈反应 | |
| D. | 丁元素主要以单质的形态存在于自然界中 |
8. 已知:
已知:
①4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H1=-905.5kJ•molˉ1
②N2(g)+O2(g)?2NO(g)△H2
一定条件下,NO可以与NH3反应转化为无害的物质,反应如下:
③4NH3(g)+4NO(g)+O2(g)?4N2(g)+6H2O(g)△H3=-1625.5 kJ•molˉ1下列说法正确的是( )
 已知:
已知:①4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H1=-905.5kJ•molˉ1
②N2(g)+O2(g)?2NO(g)△H2
一定条件下,NO可以与NH3反应转化为无害的物质,反应如下:
③4NH3(g)+4NO(g)+O2(g)?4N2(g)+6H2O(g)△H3=-1625.5 kJ•molˉ1下列说法正确的是( )
| A. | 反应①使用催化剂,△H1减小 | |
| B. | 反应②生成物总能量低于反应物总能量 | |
| C. | 反应③一定能自发进行 | |
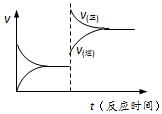
| D. | 反应③达到平衡后升高温度,v(正)、v(逆)的变化如图所示 |
15.设NA为阿伏伽德罗常数的值,则下列说法正确的是( )
| A. | 0.4mol AgNO3受热完全分解(2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑),用排水法最终收集到气体的分子数为0.2NA | |
| B. | 6.4g CaC2中含有的离子总数目为0.3NA | |
| C. | 1 mol FeI2与一定量氯气反应时,若已知有1mol Fe2+被氧化则转移的电子数为3NA | |
| D. | 1mol 苯和苯甲酸的混合物完全燃烧时消耗O2的分子数为7.5NA |
12.2016年12月1日国际纯粹与应用化学联合会宣布,将合成的四种新元素命名为113号 (缩写为Nh)、115号(Mc)、117号(Ts)和118号(Og).则下列说法不正确的是( )
| A. | 113号元素的氧化物为碱性氧化物 | |
| B. | 115号元素位于第七周期VA族 | |
| C. | 含176个中子的Ts原子表示为${\;}_{117}^{176}$Ts | |
| D. | 118号元素的原子最外层有8个电子 |
11.根据下列框图分析,下列说法不正确的是( )


| A. | E3+的氧化性比M2+的氧化性强 | |
| B. | 在反应①中硫酸既表现了酸性、又表现了氧化性 | |
| C. | 我国是世界上最早使用反应②冶炼金属M的国家 | |
| D. | 在③反应中若不加稀硫酸可能看到红褐色沉淀 |
12.a、b、c、d为四种短周期元素,a的原子M电子层有l个电子,b是地壳中含量最多的金属元素,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子半径小于c.关于这四种元素下列叙述错误的是( )
| A. | a、c、d均存在两种以上的氧化物 | |
| B. | b的氧化物与d的最高价氧化物对应水化物反应后的溶液呈酸性 | |
| C. | a是短周期中金属性最强的元素 | |
| D. | 工业上是通过电解b、d形成的化合物制取b单质 |
