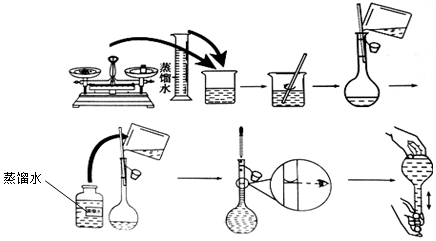
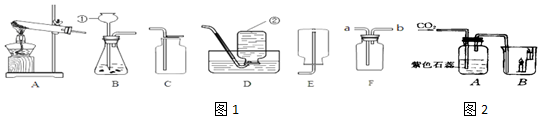
19.某无色溶液与NH4HCO3作用能产生气体,此溶液中可能大量共存的离子组是( )
| A. | Cl-、Mg2+、H+、Zn2+、SO42- | B. | Na+、Ba2+、NO3-、OH-、SO42- | ||
| C. | K+、NO3-、SO42-、OH-、Na+ | D. | MnO4-、K+、Cl-、H+、SO42- |
18.某工厂生产Cu和Zn的主要反应为:①2Cu2O+Cu2S$\frac{\underline{\;高温\;}}{\;}$6Cu+SO2↑ ②MnSO4+ZnSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$MnO2+Zn+2H2SO4下列说法不正确的是( )
| A. | ①中Cu2S、Cu2O只作还原剂 | |
| B. | ①中每生成11.2 L气体(标准状况)转移3 mol原子 | |
| C. | 由反应②可知,在相同条件下的氧化性强弱顺序为:Zn2+>Mn2+>H+ | |
| D. | ②中阳极的电极反应式为:Mn2++2H2O-2e-═MnO2+4H+ |
15.下列微粒中同时具有离子键、共价键和配位键的化合物是( )
| A. | NH4Cl | B. | Na2O2 | C. | H3O+ | D. | MgO |
13.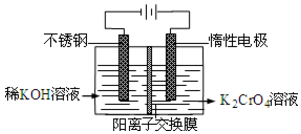 以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:下列说法不正确的是( )
以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:下列说法不正确的是( )
 以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:下列说法不正确的是( )
以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:下列说法不正确的是( )| A. | 在阴极式,发生的电极反应为:2H2O+2e-=2OH-+H2↑ | |
| B. | 在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+?Cr2O72-+H2O向右移动 | |
| C. | 该制备过程总反应的化学方程式为:4K2CrO4+4H2O$\frac{\underline{\;通电\;}}{\;}$2K2Cr2O7+4KOH+2H2↑+2O2↑ | |
| D. | 测定阳极液中K和Cr的含量,若K与Cr的物质的量之比为d,则此时铬酸钾的转化率为α=$\frac{d}{2}$ |
12.用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是( )
0 162952 162960 162966 162970 162976 162978 162982 162988 162990 162996 163002 163006 163008 163012 163018 163020 163026 163030 163032 163036 163038 163042 163044 163046 163047 163048 163050 163051 163052 163054 163056 163060 163062 163066 163068 163072 163078 163080 163086 163090 163092 163096 163102 163108 163110 163116 163120 163122 163128 163132 163138 163146 203614
| A. | NaOH溶液 | B. | HCl溶液 | C. | CuSO4溶液 | D. | NaCl溶液 |