14.T1和T2温度下(T1>T2),BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )
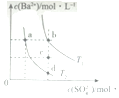

| A. | T1时,c点有沉淀生成 | |
| B. | T2时,蒸发溶剂可能由d点变到b点 | |
| C. | T2时,由a点开始加入BaCl2固体,Ksp增大 | |
| D. | BaSO4的溶解度随温度升高而增大 |
13. 研究CO2转化成有机物实现碳循环对实现社会的可持续发展具有重要的意义.将燃煤废气中的CO2转化为二甲醚的反应原理为2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(1).
研究CO2转化成有机物实现碳循环对实现社会的可持续发展具有重要的意义.将燃煤废气中的CO2转化为二甲醚的反应原理为2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(1).
(1)已知一定压强下,该反应在温度升高时,CH3OCH3(g)的浓度增大,则反应的焓变△H>0,熵变△S<0(分别填“>”、“<”、或“=”).
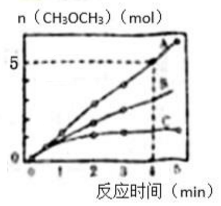
(2)相同条件下,在体积为2L的密闭容器内选用不同的催化剂,生成物二甲醚CH3OCH3的量随时间变化如图所示.
①图中0-4min内的反应速率v(CO2)=1.25mol•(L•min)-1.该温度下平衡常数的表达式为$\frac{{c(C{H_3}OC{H_3})}}{{{c^2}(C{O_2}){c^6}({H_2})}}$.
②下列有关说法正确的是ABC(填字母序号).
A.反应的活化能大小顺序是:Ea(A)<Ea(B)<Ea(C)
B.升高温度能使反应速率加快,是因为活化分子百分数增大
C.单位时间内消耗CO2与生成H2的数目为2:1时,说明反应已经达到平衡
D.增大压强,平衡正向移动,平衡常数K值增大
(3)温度下,在体积可变的密闭容器中,改变起始时各物质的起始投料量,在不同的压强下,平衡时生成物二甲醚CH3OCH3(g)的物质的量如表所示:
①P1>P2(填“>”、“<”或“=”);判断理由为压强增大,平衡向正反应方向移动,从而导致生成物的量增大.
②X1=0.05mol.
③P2下,III中CH3OCH3的平衡转化率为96%.
 研究CO2转化成有机物实现碳循环对实现社会的可持续发展具有重要的意义.将燃煤废气中的CO2转化为二甲醚的反应原理为2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(1).
研究CO2转化成有机物实现碳循环对实现社会的可持续发展具有重要的意义.将燃煤废气中的CO2转化为二甲醚的反应原理为2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(1).(1)已知一定压强下,该反应在温度升高时,CH3OCH3(g)的浓度增大,则反应的焓变△H>0,熵变△S<0(分别填“>”、“<”、或“=”).
(2)相同条件下,在体积为2L的密闭容器内选用不同的催化剂,生成物二甲醚CH3OCH3的量随时间变化如图所示.
①图中0-4min内的反应速率v(CO2)=1.25mol•(L•min)-1.该温度下平衡常数的表达式为$\frac{{c(C{H_3}OC{H_3})}}{{{c^2}(C{O_2}){c^6}({H_2})}}$.
②下列有关说法正确的是ABC(填字母序号).
A.反应的活化能大小顺序是:Ea(A)<Ea(B)<Ea(C)
B.升高温度能使反应速率加快,是因为活化分子百分数增大
C.单位时间内消耗CO2与生成H2的数目为2:1时,说明反应已经达到平衡
D.增大压强,平衡正向移动,平衡常数K值增大
(3)温度下,在体积可变的密闭容器中,改变起始时各物质的起始投料量,在不同的压强下,平衡时生成物二甲醚CH3OCH3(g)的物质的量如表所示:
| 序号 | 起始投料量不同的压强下, 平衡CH3OCH3(g)的量不同的压强 | P1 | P2 | P3 |
| I | 2.0molCO2 6.0molH2 | 0.10mol | 0.04mol | 0.02mol |
| II | 1.0molCO2 3.0molH2 | X1 | Y1 | Z1 |
| III | 1.0mol CH3OCH3 3.0mol H2O | X2 | Y2 | Z2 |
②X1=0.05mol.
③P2下,III中CH3OCH3的平衡转化率为96%.
12.下列化学方程式书写正确的是( )
| A. | 苯酚钠溶液中通入CO2: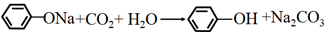 | |
| B. | 常温下CH2=CHCH3与水接触:CH2=CHCH3+H2O→CH3CH(OH)CH3 | |
| C. | 乙醇和金属钠发生反应放出氢气:2CH3CH2OH+2 Na→2CH3CH2ONa+H2↑ | |
| D. | 甲苯与氯气在铁粉催化作用下发生反应: |
11.有X、Y两种元素,原子序数小于等于20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数).下列说法正确的是( )
| A. | 若HnXOm为强酸,则X的氢化物溶于水一定显酸性 | |
| B. | 若X(OH)n为强碱,则Y(OH)n也一定为强碱 | |
| C. | 若X元素形成的单质是X2,则Y元素形成的单质一定是Y2 | |
| D. | 若Y的最高正价为m,则X的最高正价一定为m |
10.下列图象分别表示有关反应的反应过程与能量变化的关系,下列说法中正确的是( )
| A. | 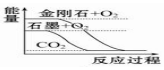 石墨转变为金刚石是吸热反应 | B. | 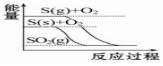 相同条件下等质量S(g)比S(s)的能量低 | ||
| C. | 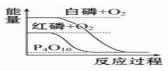 白磷比红磷稳定 | D. | 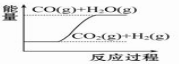 CO(g)+H2O(g)═CO2(g)+H2(g)是吸热反应 |
9.下列微粒中,与OH- 具有相同的质子数和相同的电子数的是( )
| A. | NH2- | B. | Cl | C. | NH3 | D. | Na+ |
8.下列说法中,正确的是( )
| A. | SiO2和CO2常温都是气体分子 | |
| B. | CO2、SiO2均能和氢氟酸反应 | |
| C. | CO2和SiO2都是酸性氧化物,在一定条件下都能和氧化钙反应 | |
| D. | CO2、SiO2分别是H2CO3、H2SiO3的酸酐,因而均可由CO2、SiO2与水反应制得相应酸 |
7.下列各组物质性质的比较中正确的是( )
| A. | 酸性:H3PO4>H2SO4>HClO4 | B. | 碱性:Mg(OH)2>Ca(OH)2>KOH | ||
| C. | 热稳定性:H2S>H2O>HF | D. | 氧化性:F2>Cl2>Br2>I2 |
6.下列互为同位素的是( )
| A. | Na和Na+ | B. | 35Cl和37Cl | ||
| C. | 14N和 14C | D. | ${\;}_{8}^{16}$O2和${\;}_{8}^{18}$O2 |
5.核素${\;}_{92}^{238}$U中子数与质子数之差是( )
0 162885 162893 162899 162903 162909 162911 162915 162921 162923 162929 162935 162939 162941 162945 162951 162953 162959 162963 162965 162969 162971 162975 162977 162979 162980 162981 162983 162984 162985 162987 162989 162993 162995 162999 163001 163005 163011 163013 163019 163023 163025 163029 163035 163041 163043 163049 163053 163055 163061 163065 163071 163079 203614
| A. | 54 | B. | 92 | C. | 146 | D. | 238 |