题目内容
12.下列化学方程式书写正确的是( )| A. | 苯酚钠溶液中通入CO2: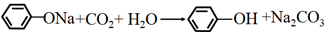 | |
| B. | 常温下CH2=CHCH3与水接触:CH2=CHCH3+H2O→CH3CH(OH)CH3 | |
| C. | 乙醇和金属钠发生反应放出氢气:2CH3CH2OH+2 Na→2CH3CH2ONa+H2↑ | |
| D. | 甲苯与氯气在铁粉催化作用下发生反应: |
分析 A.苯酚的酸性大于碳酸氢根离子,二者反应生成碳酸氢钠;
B.没有催化剂,丙烯与水不发生反应;
C.乙醇与金属钠反应生成CH3CH2ONa和氢气;
D.甲苯与氯气在铁粉催化作用下,应该是苯环氢被取代.
解答 解:A.碳酸的酸性比苯酚的酸性强,所以苯酚钠通入二氧化碳生成苯酚和碳酸氢钠,反应的化学方程式为:C6H5ONa+CO2+H2O→C6H6OH+NaHCO3,故A错误;
B.常温下CH2=CHCH3与水接触,没有催化剂,二者不发生反应,无法书写化学方程式,故B错误;
C.乙醇和金属钠发生反应放出氢气,反应的化学方程式为:2CH3CH2OH+2 Na→2CH3CH2ONa+H2↑,故C正确;
D.甲苯与氯气在铁粉催化作用下发生反应,Cl原子取代的是苯环上的H,如: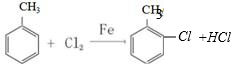 ,故D错误;
,故D错误;
故选C.
点评 本题考查了化学方程式的正误判断,为高考的高频题,题目难度中等,注意掌握化学方程式的书写原则,明确化学方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确等,试题有利于提高学生的规范答题能力.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
2.酸性 KMnO4溶液能与草酸(H2C2O4)溶液反应.某化学探究小组利用反应过程中溶液紫色消失快慢的 方法来研究影响反应速率的因素.
I.实验前首先用浓度为 0.1000mol/L 酸性 KMnO4标准溶液滴定未知浓度的草酸溶液.
(1)写出滴定过程中发生反应的离子方程式 2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
(2)下列有关一定物质的量浓度溶液配制的说法中正确的是 C.
A.把 15.8g KMnO4固体溶于 1L 水中所得溶液物质的量浓度为 0.1mol/L
B.把 0.01mol KMnO4固体投入 100mL 容量瓶中加水至刻度线,充分振荡后,浓度为 0.1mol/L C.需要 90mL 0.1mol/L 的 KMnO4溶液,应准确称量 KMnO4 固体 1 58g
D.定容时仰视容量瓶颈刻度线读数,会使配制的溶液浓度偏高
II.通过滴定实验得到草酸溶液的浓度为 0.2000mol/L.用该草酸溶液按下表进行后续实验(每次实验草酸溶液 的用量均为 8.00mL).
(3)写出表中实验 1 和实验 2 的实验目的: 探究温度不同对反应速率的影响.
(4)该小组同学对实验 1 和实验 3 分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
分析上述数据后得出“其他条件相同时,酸性高锰酸钾溶液的浓度越小,褪色时间就越短,即反应速率就
越快”的结论.甲同学认为该小组“探究反应物浓度对速率影响”的实验方案设计中存在问题,从而得到 了 错 误 的 实 验 结 论,甲 同 学 改 进 了 实 验 方 案,请 简 述 甲 同 学 改 进.
(5)该实验中使用的催化剂应选择 MnSO4并非 MnCl2,原因可用离子方程式表示为 2MnO4-+10Cl-+16H+=5Cl2↑+2Mn2++8H2O.
III.工业上可用软锰矿(主要成分为 MnO2)经下列生产过程制备高锰酸钾.
①由软锰矿提取得到 MnO2,然后在 MnO2、KOH 的熔融混合物中通入空气可制得锰酸钾(K2MnO4);
②向锰酸钾溶液中通入 CO2 可获得高锰酸钾.
(6)第①步生产过程中,在熔融混合物中通入空气时发生反应的化学方程式:2MnO2+4KOH+O2$\frac{\underline{\;高温\;}}{\;}$2K2MnO4+2H2O.
(7)向锰酸钾溶液中通入CO2可获得高锰酸该反应中氧化产物与还原产物的物质的量之比为2:1.
I.实验前首先用浓度为 0.1000mol/L 酸性 KMnO4标准溶液滴定未知浓度的草酸溶液.
(1)写出滴定过程中发生反应的离子方程式 2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
(2)下列有关一定物质的量浓度溶液配制的说法中正确的是 C.
A.把 15.8g KMnO4固体溶于 1L 水中所得溶液物质的量浓度为 0.1mol/L
B.把 0.01mol KMnO4固体投入 100mL 容量瓶中加水至刻度线,充分振荡后,浓度为 0.1mol/L C.需要 90mL 0.1mol/L 的 KMnO4溶液,应准确称量 KMnO4 固体 1 58g
D.定容时仰视容量瓶颈刻度线读数,会使配制的溶液浓度偏高
II.通过滴定实验得到草酸溶液的浓度为 0.2000mol/L.用该草酸溶液按下表进行后续实验(每次实验草酸溶液 的用量均为 8.00mL).
| 实验 编号 | 温度 (℃) | 催化剂 用量(g) | 酸性高锰酸钾溶液 | |
| 体积(mL) | 浓度(mol/L) | |||
| 1 | 25 | 0.5 | 4.00 | 0.1000 |
| 2 | 50 | 0.5 | 4.00 | 0.1000 |
| 3 | 25 | 0.5 | 4.00 | 0.0100 |
| 4 | 25 | 0 | 4.00 | 0.1000 |
(4)该小组同学对实验 1 和实验 3 分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
| 实验 编号 | 溶液褪色所需时间(min) | ||
| 第 1 次 | 第 2 次 | 第 3 次 | |
| 1 | 14.0 | 13.0 | 11.0 |
| 2 | 6.5 | 6.7 | 6.8 |
越快”的结论.甲同学认为该小组“探究反应物浓度对速率影响”的实验方案设计中存在问题,从而得到 了 错 误 的 实 验 结 论,甲 同 学 改 进 了 实 验 方 案,请 简 述 甲 同 学 改 进.
(5)该实验中使用的催化剂应选择 MnSO4并非 MnCl2,原因可用离子方程式表示为 2MnO4-+10Cl-+16H+=5Cl2↑+2Mn2++8H2O.
III.工业上可用软锰矿(主要成分为 MnO2)经下列生产过程制备高锰酸钾.
①由软锰矿提取得到 MnO2,然后在 MnO2、KOH 的熔融混合物中通入空气可制得锰酸钾(K2MnO4);
②向锰酸钾溶液中通入 CO2 可获得高锰酸钾.
(6)第①步生产过程中,在熔融混合物中通入空气时发生反应的化学方程式:2MnO2+4KOH+O2$\frac{\underline{\;高温\;}}{\;}$2K2MnO4+2H2O.
(7)向锰酸钾溶液中通入CO2可获得高锰酸该反应中氧化产物与还原产物的物质的量之比为2:1.
3.为了分离提纯蛋白质,不可在蛋白质溶液中加入下列试剂中的( )
| A. | 甲醛溶液 | B. | 饱和硫酸钠溶液 | C. | 硝酸铅溶液 | D. | 饱和硫酸铜溶液 |
7.下列各组物质性质的比较中正确的是( )
| A. | 酸性:H3PO4>H2SO4>HClO4 | B. | 碱性:Mg(OH)2>Ca(OH)2>KOH | ||
| C. | 热稳定性:H2S>H2O>HF | D. | 氧化性:F2>Cl2>Br2>I2 |
4.下列各组离子中,能大量共存且加入(或通入)X试剂后发生反应的离子方程式对应正确的是( )
| 选项 | 离子组 | 试剂X | 离子方程式 |
| A | Fe3+、Al3+、SiO32-、NO3- | 过量的盐酸 | SiO32-+2H+=H2SiO3↓ |
| B | 透明溶液中:Fe3+、NH4+、SO42-、Cl- | 过量的铜粉 | 2Fe3++Cu=2Fe2++Cu2+ |
| C | Na+、Ba+、HCO3-、Cl- | NaHSO4溶液 | H++HCO3-=CO2↑+H2O |
| D | pH=1的溶液中:Mg2+、Fe2+、NO3-、SO42- | 双氧水 | 2Fe2++H2O2+2H+=2Fe3++2H2O |
| A. | A | B. | B | C. | C | D. | D |
1.将少量高聚物M在氢氧化钠浓溶液中煮沸一段时间后,得到无色透明溶液,将溶液蒸发浓缩,冷却至室温,加入硫酸酸化,得到白色晶体N,同时剩余溶液中还含有一种有机物R,经仪器分析得出,N中含有苯环,N、R分子中均含有两种不同化学环境的氢原子.下列判断正确的是( )
| A. | R可能为乙二酸 | |
| B. | N可能为对苯二甲酸 | |
| C. | 高聚物M为加聚产物 | |
| D. | 含有羧基的物质在常温下均易溶于水 |
 第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量.图是部分元素原子的第一电离能I1随原子序数变化的曲线图.
第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量.图是部分元素原子的第一电离能I1随原子序数变化的曲线图.