16.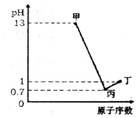 X、Y、Z、W为四种短周期元素,它们的最高价氧化物对应水化物分别为甲、乙、丙、丁,常温下甲、丙、丁均可与乙反应生成盐和水,X、Z、W的原子序数及0.1mol/L甲、丙、丁溶液的pH如图所示(已知lg2=0.3).下列说法正确的是( )
X、Y、Z、W为四种短周期元素,它们的最高价氧化物对应水化物分别为甲、乙、丙、丁,常温下甲、丙、丁均可与乙反应生成盐和水,X、Z、W的原子序数及0.1mol/L甲、丙、丁溶液的pH如图所示(已知lg2=0.3).下列说法正确的是( )
 X、Y、Z、W为四种短周期元素,它们的最高价氧化物对应水化物分别为甲、乙、丙、丁,常温下甲、丙、丁均可与乙反应生成盐和水,X、Z、W的原子序数及0.1mol/L甲、丙、丁溶液的pH如图所示(已知lg2=0.3).下列说法正确的是( )
X、Y、Z、W为四种短周期元素,它们的最高价氧化物对应水化物分别为甲、乙、丙、丁,常温下甲、丙、丁均可与乙反应生成盐和水,X、Z、W的原子序数及0.1mol/L甲、丙、丁溶液的pH如图所示(已知lg2=0.3).下列说法正确的是( )| A. | 简单阴离子的还原性:Z<W | |
| B. | X、Y分别与W形成的化合物皆为离子化合物 | |
| C. | 乙固体中加入甲的溶液或浓氨水,固体都能溶解 | |
| D. | Y、Z的简单离子都会影响水的电离平衡 |
14.下列变化中,属于加成反应的是( )
| A. | 乙炔通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色 | |
| B. | 甲苯在一定条件下与浓硝酸反应生成三硝基甲苯 | |
| C. | 乙醇在一定条件下与氢溴酸反应生成溴乙烷 | |
| D. | 在一定条件下苯与氢气反应制取环己烷 |
13.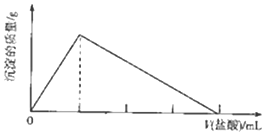 短周期主族元素R、X、Y、Z的原子序数依次增大,R的气态氢化物能使湿润的红色石蕊试纸变蓝色;X原子的核外电子数与价电子数之比为4:3,X和Y组成两种离子化合物,其中一种可作航天器中的供氧剂.向YZX2的溶液中滴加元素,产生沉淀的质量与盐酸体积的关系如图所示.下列说法不正确的是( )
短周期主族元素R、X、Y、Z的原子序数依次增大,R的气态氢化物能使湿润的红色石蕊试纸变蓝色;X原子的核外电子数与价电子数之比为4:3,X和Y组成两种离子化合物,其中一种可作航天器中的供氧剂.向YZX2的溶液中滴加元素,产生沉淀的质量与盐酸体积的关系如图所示.下列说法不正确的是( )
 短周期主族元素R、X、Y、Z的原子序数依次增大,R的气态氢化物能使湿润的红色石蕊试纸变蓝色;X原子的核外电子数与价电子数之比为4:3,X和Y组成两种离子化合物,其中一种可作航天器中的供氧剂.向YZX2的溶液中滴加元素,产生沉淀的质量与盐酸体积的关系如图所示.下列说法不正确的是( )
短周期主族元素R、X、Y、Z的原子序数依次增大,R的气态氢化物能使湿润的红色石蕊试纸变蓝色;X原子的核外电子数与价电子数之比为4:3,X和Y组成两种离子化合物,其中一种可作航天器中的供氧剂.向YZX2的溶液中滴加元素,产生沉淀的质量与盐酸体积的关系如图所示.下列说法不正确的是( )| A. | 气态氢化物的稳定性:X>R | |
| B. | 简单离子半径:X>Y>Z | |
| C. | R的最高价氧化物对应的水化物是一种强酸 | |
| D. | 用Z的单质与Y的氧化物反应可冶炼Y的单质 |
12.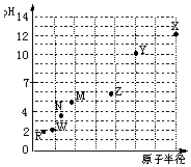 同一短周期元素,浓度均为0.01mol/L的最高价氧化物对应水化物的pH与原子半径的关系如图所示.则下列说法正确的是( )
同一短周期元素,浓度均为0.01mol/L的最高价氧化物对应水化物的pH与原子半径的关系如图所示.则下列说法正确的是( )
 同一短周期元素,浓度均为0.01mol/L的最高价氧化物对应水化物的pH与原子半径的关系如图所示.则下列说法正确的是( )
同一短周期元素,浓度均为0.01mol/L的最高价氧化物对应水化物的pH与原子半径的关系如图所示.则下列说法正确的是( )| A. | 气态氢化物的稳定性:M>N | |
| B. | Z的最高价氧化物能溶于稀氨水 | |
| C. | X和W形成的常见化合物中阴、阳离子个数比为2:1 | |
| D. | Z和R的简单离子半径:Z3+<R- |
10.已知34Se的原子结构示意图为 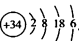 下列说法正确的是( )
下列说法正确的是( )
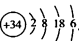 下列说法正确的是( )
下列说法正确的是( )| A. | Se位于第4周期第ⅣA族 | B. | 原子半径:Br>Se>P | ||
| C. | 热稳定性:HCl>H2Se>HBr | D. | 酸性:HClO4>HBrO4>H2SeO4 |
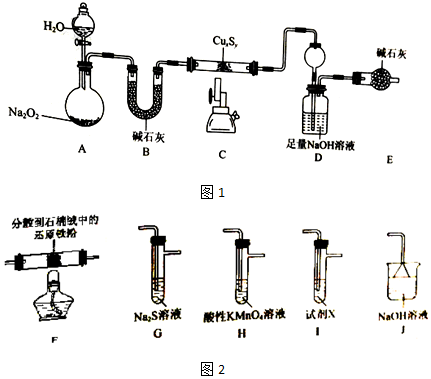
9.某小组同学设计如下实验,研究亚铁盐与H2O2溶液的反应.
【实验Ⅰ】
试剂:酸化的0.5mol•L-1FeSO4溶液(pH=0.2),5% H2O2溶液(pH=5)
(1)上述实验中H2O2溶液与FeSO4溶液反应的离子方程式是2Fe2++2H++H2O2=+2Fe3++2H2O.
(2)产生气泡的原因是Fe3+催化下H2O2分解生成O2.
【实验Ⅱ】
试剂:未酸化的0.5mol•L-1FeSO4溶液(pH=3),5% H2O2溶液(pH=5)
(3)将上述混合物分离,得到棕黄色沉淀和红褐色胶体.取部分棕黄色沉淀洗净,加4mol•L-1盐酸,沉淀溶解得到黄色溶液.初步判断该沉淀中含有Fe2O3,经检验还含有SO42-.检验棕黄色沉淀中SO42-的方法是取加入盐酸后的黄色溶液少许于试管中,加入BaCl2溶液,产生白色沉淀,说明棕黄色沉淀中含有SO42-.
(4)对于生成红褐色胶体的原因,提出两种假设:
i. H2O2溶液氧化Fe2+消耗H+
ii.Fe2+氧化的产物发生了水解
①根据实验II记录否定假设 i,理由是反应后溶液的pH降低.
②实验验证假设 ii:取Fe2(SO4)3溶液,加热,溶液变为红褐色,pH下降,证明假设 ii成立.
(5)将FeSO4溶液加入H2O2溶液后,产生红褐色胶体,反应的离子方程式是2Fe2++4H2O+H2O2=+2Fe(OH)3(胶体)+2H+.
【实验Ⅲ】
若用FeCl2溶液替代FeSO4溶液,其余操作与实验 II相同,除了产生与 II相同的现象外,还生成刺激性气味气体,该气体能使湿润的蓝色石蕊试纸变红但不褪色.
(6)产生刺激性气味气体的原因是H2O2分解反应放热,促进Fe3+的水解平衡正向移动,产生的HCl受热挥发.
(7)由实验Ⅰ、Ⅱ、Ⅲ可知,亚铁盐与H2O2反应的现象与pH、阴离子种类、温度、反应物用量(至少写两点)有关.
【实验Ⅰ】
试剂:酸化的0.5mol•L-1FeSO4溶液(pH=0.2),5% H2O2溶液(pH=5)
| 操作 | 现象 |
| 取2mL上述FeSO4溶液于试管中,加入5滴5% H2O2溶液 | 溶液立即变为棕黄色,稍后,产生气泡.测得反应后溶液pH=0.9 |
| 向反应后的溶液中加入KSCN溶液 | 溶液变红 |
(2)产生气泡的原因是Fe3+催化下H2O2分解生成O2.
【实验Ⅱ】
试剂:未酸化的0.5mol•L-1FeSO4溶液(pH=3),5% H2O2溶液(pH=5)
| 操作 | 现象 |
| 取2mL 5% H2O2溶液于试管中,加入5滴上述FeSO4溶液 | 溶液立即变为棕黄色,产生大量气泡,并放热,反应混合物颜色加深且有浑浊.测得反应后溶液pH=1.4 |
(4)对于生成红褐色胶体的原因,提出两种假设:
i. H2O2溶液氧化Fe2+消耗H+
ii.Fe2+氧化的产物发生了水解
①根据实验II记录否定假设 i,理由是反应后溶液的pH降低.
②实验验证假设 ii:取Fe2(SO4)3溶液,加热,溶液变为红褐色,pH下降,证明假设 ii成立.
(5)将FeSO4溶液加入H2O2溶液后,产生红褐色胶体,反应的离子方程式是2Fe2++4H2O+H2O2=+2Fe(OH)3(胶体)+2H+.
【实验Ⅲ】
若用FeCl2溶液替代FeSO4溶液,其余操作与实验 II相同,除了产生与 II相同的现象外,还生成刺激性气味气体,该气体能使湿润的蓝色石蕊试纸变红但不褪色.
(6)产生刺激性气味气体的原因是H2O2分解反应放热,促进Fe3+的水解平衡正向移动,产生的HCl受热挥发.
(7)由实验Ⅰ、Ⅱ、Ⅲ可知,亚铁盐与H2O2反应的现象与pH、阴离子种类、温度、反应物用量(至少写两点)有关.
8.科技改变生活,充电宝已逐渐成为人们生活中的必需品.某充电宝工作时的总反应式为:V2O3+xLi $?_{充电}^{放电}$ Li4V2O3,下列说法正确的是( )
| A. | 放电时正极上的电极反应为:Li-e-═Li+ | |
| B. | 该充电宝的凝胶介质可用KOH水溶液代替 | |
| C. | 充电时每生成14g Li,凝胶介质中有2mol电子通过 | |
| D. | 充电时电池的正极失电子后Li4V2O3会转化为V2O3 |
7.下列关于元素性质的有关叙述中不正确的是( )
0 162809 162817 162823 162827 162833 162835 162839 162845 162847 162853 162859 162863 162865 162869 162875 162877 162883 162887 162889 162893 162895 162899 162901 162903 162904 162905 162907 162908 162909 162911 162913 162917 162919 162923 162925 162929 162935 162937 162943 162947 162949 162953 162959 162965 162967 162973 162977 162979 162985 162989 162995 163003 203614
| A. | S Cl 的原子半径依次减小 | |
| B. | Na Mg 的失电子能力依次增强 | |
| C. | O F的气态氢化物的稳定性依次增强 | |
| D. | Si P 的最高价含氧酸的酸性依次增强 |
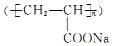 和苯甲酸异丙酯流程如下(部分条件已经略去):
和苯甲酸异丙酯流程如下(部分条件已经略去):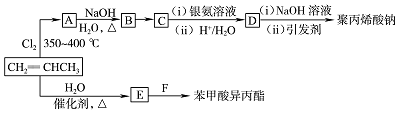
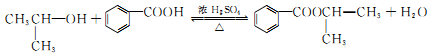 .
.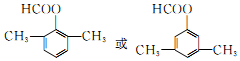 .
.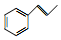 和F为原料(无机试剂任选),设计制备有机物
和F为原料(无机试剂任选),设计制备有机物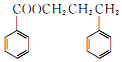 的合成路线.
的合成路线.