2.已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系如图所示.则甲和X不可能是( )

| A. | 甲为C,X为O2 | B. | 甲为SO2,X为NaOH溶液 | ||
| C. | 甲为Fe,X为Cl2 | D. | 甲为硝酸溶液,X为Fe |
1.下列几种类推结论中正确的是( )
| A. | 酸的水溶液呈酸性,故酸性水溶液一定是酸的水溶液 | |
| B. | Fe3O4可写成FeO?Fe2O3;Pb3O4也可写成PbO?Pb2O3 | |
| C. | 工业上通过电解熔融MgCl2来制取金属镁;也可以通过电解熔融AlCl3来制取金属铝 | |
| D. | 第2周期元素氢化物稳定性顺序是HF>H2O>NH3;则第3周期元素氢化物稳定性顺序是HCl>H2S>PH3 |
20.如图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是( )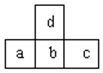

| A. | d的氢化物比b的氢化物稳定 | |
| B. | d与c不能形成化合物 | |
| C. | a、b、c的最高价氧化物对应水化物的酸性强弱的关系是c>b>a | |
| D. | 原子半径的大小顺序是a>b>c>d |
19. 如图表示温度和压强对平衡状态下可逆反应2M(g)+N(g)?2Q(g)△H<0的影响.下列有关说法正确的是(反应容器的体积不变)( )
如图表示温度和压强对平衡状态下可逆反应2M(g)+N(g)?2Q(g)△H<0的影响.下列有关说法正确的是(反应容器的体积不变)( )
 如图表示温度和压强对平衡状态下可逆反应2M(g)+N(g)?2Q(g)△H<0的影响.下列有关说法正确的是(反应容器的体积不变)( )
如图表示温度和压强对平衡状态下可逆反应2M(g)+N(g)?2Q(g)△H<0的影响.下列有关说法正确的是(反应容器的体积不变)( )| A. | x可能表示该反应的平衡常数 | |
| B. | x可能表示平衡混合物的密度 | |
| C. | 当x表示Q的体积分数时,T2<T1 | |
| D. | 当x表示平衡混合物的物质的量时,T2<T1 |
18.为确定下列置于空气中的物质是否变质,所选试剂(括号内的物质)不能达到目的是( )
| A. | 氯水(AgNO3溶液) | B. | NaOH溶液[Ba(OH)2溶液] | ||
| C. | FeSO4溶液(KSCN溶液) | D. | KI溶液(淀粉溶液) |
16.中和滴定中用已知浓度的稀盐酸滴定未知浓度的稀氨水,计算式与滴定氢氧化钠溶液类似:c1V1=c2V2,则( )
| A. | 终点溶液偏碱性 | B. | 终点溶液中c(NH4+)=c(Cl-) | ||
| C. | 终点溶液中氨过量 | D. | 合适的指示剂是甲基橙而非酚酞 |
15.工业上在一定条件下将丙烷脱氢制丙烯.
(1)反应过程中能量变化如图1所示,下列有关叙述正确的是ac.
a.此反应为吸热反应
b.催化剂能改变反应的焓变和活化能
c.E1表示正反应的活化能,E2表示逆反应的活化能
d.有催化剂能加快反应速率,提高丙烷的转化率
(2)上述反应在恒温恒容密闭容器中达到平衡,其平衡常数K的表达式为K=$\frac{c(C{H}_{2}=C{H}_{2})c({H}_{2})}{c(C{H}_{3}C{H}_{2}C{H}_{3})}$.若升温,该反应的平衡常数增大(填“增大”、“减小”或“不变”).若向上述反应达到平衡的容器内再通入少量丙烷,则$\frac{c(C{H}_{2}=CHC{H}_{3})}{c(C{H}_{3}C{H}_{2}C{H}_{3})}$减小(填“增大”、“减小”或“不变”).
(3)在0.1MPa、800K条件下,向恒容密闭容器中通入丙烷和稀有气体,丙烷脱氢反应的转化率随着稀有气体与丙烷比例的变化情况如图2所示,则随着稀有气体与丙烷比例的增加,丙烷转化率逐渐增大的原因是此反应是气体体积和增加的反应,随着稀有气体比例的增加,降低了反应体系各气体的分压,相当于减压,从而促进反应向正反应方向进行,提高了丙烷脱氢的转化率.

(4)上述反应生成物丙烯经多步氧化生成丙酸,已知常温下Ka(CH3CH2COOH)=1.3×10-5.Kb(NH3•H2O)=1.8×10-5.
①用离子方程式表示CH3CH2COONa溶液显碱性的原因CH3CH2COO-+H2O?CH3COOH+OH-.
②常温下,若丙酸与氨水混合后溶液呈中性,则溶液中$\frac{c(C{H}_{3}C{H}_{2}CO{O}^{-})}{c(N{H}_{3}•{H}_{2}O)}$=1.3×109.
(5)已知:
则丙烷脱氢反应的热化学方程式为CH3CH2CH3(g)?CH2=CHCH3(g)+H2(g)△H=+126kJ/mol.
(1)反应过程中能量变化如图1所示,下列有关叙述正确的是ac.
a.此反应为吸热反应
b.催化剂能改变反应的焓变和活化能
c.E1表示正反应的活化能,E2表示逆反应的活化能
d.有催化剂能加快反应速率,提高丙烷的转化率
(2)上述反应在恒温恒容密闭容器中达到平衡,其平衡常数K的表达式为K=$\frac{c(C{H}_{2}=C{H}_{2})c({H}_{2})}{c(C{H}_{3}C{H}_{2}C{H}_{3})}$.若升温,该反应的平衡常数增大(填“增大”、“减小”或“不变”).若向上述反应达到平衡的容器内再通入少量丙烷,则$\frac{c(C{H}_{2}=CHC{H}_{3})}{c(C{H}_{3}C{H}_{2}C{H}_{3})}$减小(填“增大”、“减小”或“不变”).
(3)在0.1MPa、800K条件下,向恒容密闭容器中通入丙烷和稀有气体,丙烷脱氢反应的转化率随着稀有气体与丙烷比例的变化情况如图2所示,则随着稀有气体与丙烷比例的增加,丙烷转化率逐渐增大的原因是此反应是气体体积和增加的反应,随着稀有气体比例的增加,降低了反应体系各气体的分压,相当于减压,从而促进反应向正反应方向进行,提高了丙烷脱氢的转化率.

(4)上述反应生成物丙烯经多步氧化生成丙酸,已知常温下Ka(CH3CH2COOH)=1.3×10-5.Kb(NH3•H2O)=1.8×10-5.
①用离子方程式表示CH3CH2COONa溶液显碱性的原因CH3CH2COO-+H2O?CH3COOH+OH-.
②常温下,若丙酸与氨水混合后溶液呈中性,则溶液中$\frac{c(C{H}_{3}C{H}_{2}CO{O}^{-})}{c(N{H}_{3}•{H}_{2}O)}$=1.3×109.
(5)已知:
| 化学键 | H-H | C-H | C-C | C=C |
| 键能(kJ•mol-1) | 436 | 413 | 348 | 612 |
14.铅蓄电池有广泛的应用,由方铅矿(PbS)制备铅蓄电池电极材料(PbO2)的方法如图1:

査阅资料:①PbCl2(s)+2Cl-(aq)?PbCl42-(aq)△H>0
②Fe3+、Pb2+以氢氧化物形式开始沉淀时的PH值分别为1.9、7.0
③不同温度和浓度的食盐溶液中PbCl2的溶解度(g•L-1):
(1)步骤I中FeCl3溶液与PbS反应生成PbCl2和S的化学方程式为PbS+2FeCl3=PbCl2+2FeCl2+S;
加入盐酸控制pH小于1.0的原因是抑制Fe3+的水解.
(2)步骤II中浸泡溶解时采用95℃和饱和食盐水的目的分别是加快浸泡速率、增大PbCl2在氯化钠溶液中的溶解度.
(3)步骤III中将滤液B蒸发浓缩后再用冰水浴的原因是冰水浴使反应PbCl2(s)+2Cl-(aq)?PbCl42-(aq)平衡逆向移动,使PbCl42-不断转化为PbCl2晶体而析出(请用平衡移动原理解释).
(4)步骤IV需用溶质质量分数为20%、密度为1.22g•cm-3的硫酸溶液,现用溶质质量分数为98.3%、密度为1.84g•cm-3的浓硫酸配制,需用到的玻璃仪器有ABE(填相应的字母).
A.烧杯 B.量筒 C.容量瓶 D.锥形瓶 E.玻璃棒 F.胶头滴管
(5)用铅蓄电池为电源,采用电解法分开处理含有Cr2O72-及含有NO2-的酸性废水(最终Cr2O72-转化为Cr(OH)3,NO2-转化为无毒物质),其装置如图2所示.
①左池中Cr2O72-转化为Cr3+的离子方程式是6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
②当阴极区消耗2mol NO2-时,右池减少的H+的物质的量为2 mol.

査阅资料:①PbCl2(s)+2Cl-(aq)?PbCl42-(aq)△H>0
②Fe3+、Pb2+以氢氧化物形式开始沉淀时的PH值分别为1.9、7.0
③不同温度和浓度的食盐溶液中PbCl2的溶解度(g•L-1):
| NaCl浓度(g.L-1) 温度(℃) | 20 | 40 | 60 | 100 | 180 | 260 | 300 |
| 13 | 3 | 1 | 0 | 0 | 3 | 9 | 13 |
| 50 | 8 | 4 | 3 | 5 | 10 | 21 | 35 |
| 100 | 17 | 11 | 12 | 15 | 30 | 65 | 95 |
加入盐酸控制pH小于1.0的原因是抑制Fe3+的水解.
(2)步骤II中浸泡溶解时采用95℃和饱和食盐水的目的分别是加快浸泡速率、增大PbCl2在氯化钠溶液中的溶解度.
(3)步骤III中将滤液B蒸发浓缩后再用冰水浴的原因是冰水浴使反应PbCl2(s)+2Cl-(aq)?PbCl42-(aq)平衡逆向移动,使PbCl42-不断转化为PbCl2晶体而析出(请用平衡移动原理解释).
(4)步骤IV需用溶质质量分数为20%、密度为1.22g•cm-3的硫酸溶液,现用溶质质量分数为98.3%、密度为1.84g•cm-3的浓硫酸配制,需用到的玻璃仪器有ABE(填相应的字母).
A.烧杯 B.量筒 C.容量瓶 D.锥形瓶 E.玻璃棒 F.胶头滴管
(5)用铅蓄电池为电源,采用电解法分开处理含有Cr2O72-及含有NO2-的酸性废水(最终Cr2O72-转化为Cr(OH)3,NO2-转化为无毒物质),其装置如图2所示.
①左池中Cr2O72-转化为Cr3+的离子方程式是6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
②当阴极区消耗2mol NO2-时,右池减少的H+的物质的量为2 mol.
13.运用化学反应原理研究NH3的性质具有重要意义.请回答下列问题:
(1)已知:
①NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H=-1266.5kJ•mol-1
②N2(g)+O2(g)═2NO(g)△H=+180.5kJ•mol-1
写出氨高温催化氧化生成NO的热化学方程式4NH3(g)+5O2(g)$\frac{\underline{催化剂}}{△}$4NO(g)+6H2O(g)△H=-905.5KJ/mol.
(2)氨气、空气可以构成燃料电池,其电池反应原理为:4NH3+3O2=2N2+6H2O.已知电解质溶液为KOH溶液,则负极的电极反应式为2NH3+6OH--6e-═N2+6H2O.
(3)合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的化学平衡常数K值和温度的关系如表:
①由上表数据可知该反应的△H< 0 填“>”、“<”或“=”);
②理论上,为了增大平衡时H2的转化率,可采取的措施是AD(选填字母);
A.增大压强 B.使用合适的催化剂 C.升高温度 D.及时分离出产物中的NH3
③400℃时,测得某时刻氨气、氮气、氢气的物质的量浓度分别为3mol•L-1、2mol•L-1、l mol•L-1,此时刻该反应的V正(N2)=< V逆(N2).(填“>”、“<”或“=”).
(4)已知25℃时,Ksp[Fe(OH)3]=1.0×l0-38,Ksp[Al(OH)3]=4.0×l0-34,当溶液中的金属离子浓度小于1.0×10-5mol•L-1时,可以认为沉淀完全.在含Fe3+、A13+的浓度均为1.05mol•L-1的溶液中加入氨水,当Fe3+完全沉淀时,A13+沉淀的百分数70%.
0 162796 162804 162810 162814 162820 162822 162826 162832 162834 162840 162846 162850 162852 162856 162862 162864 162870 162874 162876 162880 162882 162886 162888 162890 162891 162892 162894 162895 162896 162898 162900 162904 162906 162910 162912 162916 162922 162924 162930 162934 162936 162940 162946 162952 162954 162960 162964 162966 162972 162976 162982 162990 203614
(1)已知:
①NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H=-1266.5kJ•mol-1
②N2(g)+O2(g)═2NO(g)△H=+180.5kJ•mol-1
写出氨高温催化氧化生成NO的热化学方程式4NH3(g)+5O2(g)$\frac{\underline{催化剂}}{△}$4NO(g)+6H2O(g)△H=-905.5KJ/mol.
(2)氨气、空气可以构成燃料电池,其电池反应原理为:4NH3+3O2=2N2+6H2O.已知电解质溶液为KOH溶液,则负极的电极反应式为2NH3+6OH--6e-═N2+6H2O.
(3)合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的化学平衡常数K值和温度的关系如表:
| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
②理论上,为了增大平衡时H2的转化率,可采取的措施是AD(选填字母);
A.增大压强 B.使用合适的催化剂 C.升高温度 D.及时分离出产物中的NH3
③400℃时,测得某时刻氨气、氮气、氢气的物质的量浓度分别为3mol•L-1、2mol•L-1、l mol•L-1,此时刻该反应的V正(N2)=< V逆(N2).(填“>”、“<”或“=”).
(4)已知25℃时,Ksp[Fe(OH)3]=1.0×l0-38,Ksp[Al(OH)3]=4.0×l0-34,当溶液中的金属离子浓度小于1.0×10-5mol•L-1时,可以认为沉淀完全.在含Fe3+、A13+的浓度均为1.05mol•L-1的溶液中加入氨水,当Fe3+完全沉淀时,A13+沉淀的百分数70%.
 将水分解制得氢气的一种工业方法是“硫-碘循环法”,依次涉及下列三步反应:
将水分解制得氢气的一种工业方法是“硫-碘循环法”,依次涉及下列三步反应: