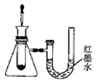
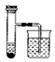
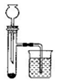
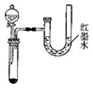
3.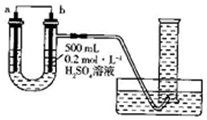 利用如图装置可以测定铜锌原电池工作时转移电子的物质的量,假设量筒的量程足够大,锌片和铜片中无杂质,气体体积已转换为标准状况.下列说法正确的是( )
利用如图装置可以测定铜锌原电池工作时转移电子的物质的量,假设量筒的量程足够大,锌片和铜片中无杂质,气体体积已转换为标准状况.下列说法正确的是( )
 利用如图装置可以测定铜锌原电池工作时转移电子的物质的量,假设量筒的量程足够大,锌片和铜片中无杂质,气体体积已转换为标准状况.下列说法正确的是( )
利用如图装置可以测定铜锌原电池工作时转移电子的物质的量,假设量筒的量程足够大,锌片和铜片中无杂质,气体体积已转换为标准状况.下列说法正确的是( )| A. | a电极的电极材料是铜 | |
| B. | 如果将稀硫酸换为CuSO4溶液,则不能达到实验目的 | |
| C. | 锌与稀硫酸反应时放出的热量对实验测定不产生影响 | |
| D. | 若量筒中收集到a L H2,则电解质溶液中通过了$\frac{a}{11.2}$mol电子 |
2.某元素R与氮元素位于同主族,其原子结构示意图为  ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | R的核电荷数是43 | |
| B. | R的最高正化合价为+3价 | |
| C. | R的最高价氧化物对应水化物的酸性比硝酸弱 | |
| D. | 气态氢化物的稳定性:NH3<RH3 |
20.根据下列实验操作和实验现象所得结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向石蕊溶液中滴加氯水至足量 | 石蕊溶液先变红再褪色 | Cl2有酸性和漂白性 |
| B | 向大豆油、煤油中分别加入足量NaOH溶液,充分加热 | 一种液体仍然分层,另一种液体不再分层 | 分层者为煤油,不分层者为大豆油 |
| C | 向某溶液中加入足量盐酸 | 生成白色沉淀 | 该溶液中含有Ag+ |
| D | 用容量瓶配制一定物质的量浓度的K2SO4溶液,定容后反复摇匀 | 液面低于刻度线 | 所配溶液浓度偏高 |
| A. | A | B. | B | C. | C | D. | D |
19.化学与生产、生活密切相关,下列与化学有关的说法正确的是( )
| A. | 生理盐水和A1(OH)3胶体的本质区别是能否产生丁达尔效应 | |
| B. | 纤维素和聚氯乙烯均为可降解的高分子化合物 | |
| C. | 水晶项链和玻璃杯均属于硅酸盐产品 | |
| D. | 耐蚀合金的防腐原理与电化学无关 |
18.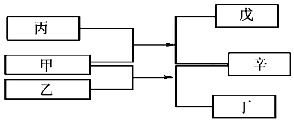 A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质,常温常压下乙为液体.常温下,0.1mol/L 丁溶液的pH为13,上述各物质间的转化关系如图所示.下列说法正确的是( )
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质,常温常压下乙为液体.常温下,0.1mol/L 丁溶液的pH为13,上述各物质间的转化关系如图所示.下列说法正确的是( )
 A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质,常温常压下乙为液体.常温下,0.1mol/L 丁溶液的pH为13,上述各物质间的转化关系如图所示.下列说法正确的是( )
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质,常温常压下乙为液体.常温下,0.1mol/L 丁溶液的pH为13,上述各物质间的转化关系如图所示.下列说法正确的是( )| A. | 元素B、C、D的原子半径由大到小的顺序为 r(D)>r(C)>r(B) | |
| B. | 1L0.lmol/L戊溶液中阴离子的总物质的量小于0.1mol | |
| C. | 1mol甲与足量的乙完全反应共转移了约6.02×1023个电子 | |
| D. | 元素的非金属性B>C>A |
17.下列关于有机物的说法正确的是( )
| A. | 乙烯、聚乙烯和苯均能发生加成反应 | |
| B. | lmol葡萄糖能水解生成2molCH3CH2OH和2molCO2 | |
| C. | 用碳酸钠溶液可一次性鉴别乙酸、苯和乙醇三种无色液体 | |
| D. | 戊烷的一氯代物和丙烷的二氯代物的同分异构体数目相同 |
15. 硫代硫酸钠(Na2S2O3•5H2O)俗名“大苏打”,又称为“海波”.它易溶于水,难溶于乙醇,加热、遇酸均易分解.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:
硫代硫酸钠(Na2S2O3•5H2O)俗名“大苏打”,又称为“海波”.它易溶于水,难溶于乙醇,加热、遇酸均易分解.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:
实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节分液的滴速,使反应产生的SO2气体较均匀地通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸.
②直至析出的浑浊不再消失,并控制溶液的pH接近7时,停止通入SO2气体.
…
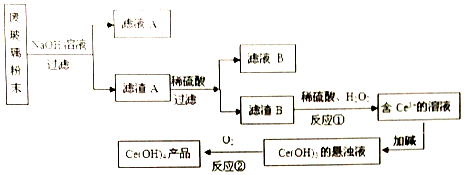
(1)写出仪器A的名称蒸馏烧瓶.
(2)为了保证硫代硫酸钠的产量,实验中不能让溶液pH<7,请用离子方程式解释原因S2O32-+2H+=S↓+SO2↑+H2O.
(3)写出三颈烧瓶B中制取Na2S2O3,反应的总化学反应方程式4SO2+2Na2S+Na2CO3=CO2+3Na2S2O3.
(4)从上述生成物混合液中获得较高产率Na2S2O3•5H2O的步骤为:
向反应混合液加活性炭脱色$\stackrel{操作①}{→}$滤液$\stackrel{操作②}{→}$$→_{③}^{操作}$粗晶体
为减少产品的损失,操作①为趁热过滤,“趁热”的原因是为了防止晶体在漏斗中大量析出导致产率降低;操作②是蒸发浓缩,冷却结晶;操作①是抽滤、洗涤、干燥.
(5)测定产品纯度
取6.00g产品,配制成100mL溶液.取10.00mL溶液,以淀粉溶液为指示剂,用浓度为00.500mol/LI2的标准溶液进行滴定,反应原理为2S2O32-+I2=S4O62-+2I-.相关数据记录如表所示.
滴定时,达到滴定终点的现象是溶液由无色变蓝色,且半分钟不褪色.产品的纯度为82.67%.
(6)Na2S2O3常用作脱氧剂,在溶液中易被Cl2氧化成SO42-,该反应的离子方程式为S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+.
 硫代硫酸钠(Na2S2O3•5H2O)俗名“大苏打”,又称为“海波”.它易溶于水,难溶于乙醇,加热、遇酸均易分解.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:
硫代硫酸钠(Na2S2O3•5H2O)俗名“大苏打”,又称为“海波”.它易溶于水,难溶于乙醇,加热、遇酸均易分解.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节分液的滴速,使反应产生的SO2气体较均匀地通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸.
②直至析出的浑浊不再消失,并控制溶液的pH接近7时,停止通入SO2气体.
…
(1)写出仪器A的名称蒸馏烧瓶.
(2)为了保证硫代硫酸钠的产量,实验中不能让溶液pH<7,请用离子方程式解释原因S2O32-+2H+=S↓+SO2↑+H2O.
(3)写出三颈烧瓶B中制取Na2S2O3,反应的总化学反应方程式4SO2+2Na2S+Na2CO3=CO2+3Na2S2O3.
(4)从上述生成物混合液中获得较高产率Na2S2O3•5H2O的步骤为:
向反应混合液加活性炭脱色$\stackrel{操作①}{→}$滤液$\stackrel{操作②}{→}$$→_{③}^{操作}$粗晶体
为减少产品的损失,操作①为趁热过滤,“趁热”的原因是为了防止晶体在漏斗中大量析出导致产率降低;操作②是蒸发浓缩,冷却结晶;操作①是抽滤、洗涤、干燥.
(5)测定产品纯度
取6.00g产品,配制成100mL溶液.取10.00mL溶液,以淀粉溶液为指示剂,用浓度为00.500mol/LI2的标准溶液进行滴定,反应原理为2S2O32-+I2=S4O62-+2I-.相关数据记录如表所示.
| 编号 | 1 | 2 | 3 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.98 | 22.50 | 20.02 |
(6)Na2S2O3常用作脱氧剂,在溶液中易被Cl2氧化成SO42-,该反应的离子方程式为S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+.
14.现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚( ),同时利用此装置的电能在铁上镀铜,下列说法错误的是( )
),同时利用此装置的电能在铁上镀铜,下列说法错误的是( )
0 162724 162732 162738 162742 162748 162750 162754 162760 162762 162768 162774 162778 162780 162784 162790 162792 162798 162802 162804 162808 162810 162814 162816 162818 162819 162820 162822 162823 162824 162826 162828 162832 162834 162838 162840 162844 162850 162852 162858 162862 162864 162868 162874 162880 162882 162888 162892 162894 162900 162904 162910 162918 203614
 ),同时利用此装置的电能在铁上镀铜,下列说法错误的是( )
),同时利用此装置的电能在铁上镀铜,下列说法错误的是( )
| A. | 铁电极应与Y相连接 | |
| B. | 反应过程中甲中右边区域溶液pH逐渐升高 | |
| C. | A极的电极反应式为 +2e-+H+=Cl-+ +2e-+H+=Cl-+ | |
| D. | 当外电路中有0.2 mole-转移时,A极区增加的H+的个数为0.1NA |