13.表为元素周期表的一部分:
请填写下列空白:
(1)表中元素,原子半径最大的是Na(填写元素符号);①的核外电子排布式1s22s22p4;③和⑥两元素形成化合物的电子式为 .
.
(2)②③④三种元素最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式).
(3))比较④、⑤两种元素的简单离子半径:S2->Al3+(填离子符号);元素④最高价氧化物对应的水化物与硝酸反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
(4))列举一个事实来证明元素①比元素⑤的非金属性强H2O的稳定性大于H2S.
(5))若8g甲烷气体完全燃烧生成液态水时放出445.15kJ的热量,请写出其热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3KJ•mol-1.
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | ||
| 二 | C | N | ① | |||||
| 三 | ② | ③ | ④ | P | ⑤ | ⑥ |
(1)表中元素,原子半径最大的是Na(填写元素符号);①的核外电子排布式1s22s22p4;③和⑥两元素形成化合物的电子式为
 .
.(2)②③④三种元素最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式).
(3))比较④、⑤两种元素的简单离子半径:S2->Al3+(填离子符号);元素④最高价氧化物对应的水化物与硝酸反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
(4))列举一个事实来证明元素①比元素⑤的非金属性强H2O的稳定性大于H2S.
(5))若8g甲烷气体完全燃烧生成液态水时放出445.15kJ的热量,请写出其热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3KJ•mol-1.
12.下列化工生产涉及的变化主要是物理变化的是( )
| A. | 煤的干馏 | B. | 石油的分馏 | C. | 石油的裂化 | D. | 石油的裂解 |
11.可用来鉴别乙醇、乙醛的试剂是( )
| A. | 银氨溶液 | B. | 乙酸溶液 | C. | 氯化铁溶液 | D. | 氢氧化钠溶液 |
10.2004年2月2日,俄国杜布纳实验室宣布用核反应得到了两种新元素X和Y.X是用高能48Ca撞击${\;}_{95}^{243}$Am靶得到的.其质量数为288,质子数为115,则X元素原子核内中子数和核外电子数之差为( )
| A. | 58 | B. | 173 | C. | 3 | D. | 128 |
9.用NA表示阿伏加德罗常数的值.下列叙述中不正确的是( )
| A. | 标准状况下,22.4LHF中的原子数目为2NA | |
| B. | 在18 g18O2中含有NA个氧原子 | |
| C. | 常温常压下,17g的NH3含有的电子数为10NA | |
| D. | NA 个CO2分子中含有4mol极性键 |
7.下列图示与对应的叙述符合的是( )
| A. | 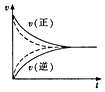 用实线、虚线分别表示某可逆反应未使用催化剂和使用催化剂的正、逆反应速率随时间的变化 | |
| B. | 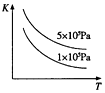 表示反应2SO2(g)+O2(g)?2SO3(g)△H<0的平衡常数K与温度和压强的关系 | |
| C. | 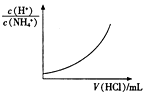 表示向0.1mol/L的NH4Cl溶液中滴加0.1mol/L的HCl溶液时,溶液中$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$随HCl溶液体积变化关系 | |
| D. | 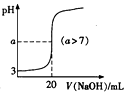 表示常温下向20mL pH=3的醋酸中滴加pH=11的NaOH溶液,溶液的pH随NaOH溶液体积的变化关系 |
6.H2是一种化工原料,可以制备一系列物质(如图所示).下列说法正确的是( )
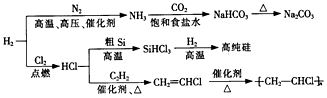

| A. | 使用催化剂可以降低合成氨反应的活化能 | |
| B. | 用澄清石灰水可以检验NaHCO3中是否混有Na2CO3 | |
| C. | 由粗硅制高纯硅的反应类型依次为化合反应、置换反应 | |
| D. | 聚合物 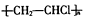 的链节为CH2=CHCl 的链节为CH2=CHCl |
4.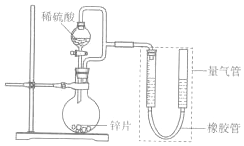 某同学设计计如图所示装罝(部分夹持装置己略去)进行实验探究:
某同学设计计如图所示装罝(部分夹持装置己略去)进行实验探究:
(1)用上述装置探究影响化学反应速率的因素.以生成9.0mL气体为计时终点,结果为t1>t2.
①比较实验I和Ⅱ可以得出的实验结论是在其他条件一定时,化学反应速率随反应物浓度的增大而增大.
②若将锌片换成含杂质的粗锌片,其他条件使其与上述一致,所测得的反应速率均大于上述实验对应的数据.粗锌片中所含杂质可能是BCD (填序号).
A.二氧化硅 B.银 C.铜 D.石墨
(2)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀
①圆底烧瓶中的试剂可选用BD(填序号)
A.稀HCl B.NaCl溶液 C.乙醇 D.NaOH溶液
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是量气管右端液面下降,左端液面上升.
0 162719 162727 162733 162737 162743 162745 162749 162755 162757 162763 162769 162773 162775 162779 162785 162787 162793 162797 162799 162803 162805 162809 162811 162813 162814 162815 162817 162818 162819 162821 162823 162827 162829 162833 162835 162839 162845 162847 162853 162857 162859 162863 162869 162875 162877 162883 162887 162889 162895 162899 162905 162913 203614
 某同学设计计如图所示装罝(部分夹持装置己略去)进行实验探究:
某同学设计计如图所示装罝(部分夹持装置己略去)进行实验探究:(1)用上述装置探究影响化学反应速率的因素.以生成9.0mL气体为计时终点,结果为t1>t2.
| 序号 | V(H2SO4)/mL | C(H2SO4)/mol•L-1 | t/s |
| I | 40 | 1 | t1 |
| II | 40 | 4 | t2 |
②若将锌片换成含杂质的粗锌片,其他条件使其与上述一致,所测得的反应速率均大于上述实验对应的数据.粗锌片中所含杂质可能是BCD (填序号).
A.二氧化硅 B.银 C.铜 D.石墨
(2)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀
①圆底烧瓶中的试剂可选用BD(填序号)
A.稀HCl B.NaCl溶液 C.乙醇 D.NaOH溶液
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是量气管右端液面下降,左端液面上升.
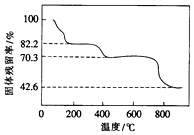 硫酸高铈[Ce(SO4)2]是一种常用的强氧化剂.
硫酸高铈[Ce(SO4)2]是一种常用的强氧化剂.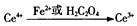
 .
. .
.