题目内容
10.2004年2月2日,俄国杜布纳实验室宣布用核反应得到了两种新元素X和Y.X是用高能48Ca撞击${\;}_{95}^{243}$Am靶得到的.其质量数为288,质子数为115,则X元素原子核内中子数和核外电子数之差为( )| A. | 58 | B. | 173 | C. | 3 | D. | 128 |
分析 原子中:核内质子数=核外电子数,中子数=质量数-质子数,据此分析.
解答 解:质量数为288,质子数为115,核内质子数=核外电子数,则电子数为115,中子数=288-115=173,所以原子核内中子数和核外电子数之差为173-115=58,故A正确;
故选A.
点评 本题考查了质量数、质子数、中子数之间的关系,难度不大,注意质子数决定元素种类,质量数决定核素种类,侧重考查学生分析问题、解答问题能力.

练习册系列答案
相关题目
10.下列实验设计及其对应的离子方程式均正确的是( )
| A. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ | |
| B. | Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++2OH-+O2↑ | |
| C. | 硫化钠水溶液呈碱性的原因:S2-+2H2O?H2S↑+2OH- | |
| D. | 铝粉与NaOH溶液反应产生H2:2A1+2OH-+2H2O=2Al(OH)3↓+3H2↑ |
18.下列关于有机物结构或性质说法正确的是( )
| A. | 乙烯的结构式为CH2=CH2 | |
| B. | CH2Cl2属于正四面体的空间结构 | |
| C. | 乙炔是含碳量最高的烃 | |
| D. | 正戊烷分子中所有碳原子一定不在同一条直线上 |
15.根据下列实验及其现象,所得出的结论正确的是( )
| 实验 | 现象 | 结论 | |
| A | 用大理石和盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中 | 出现白色沉淀 | 非金属性:Cl>C>S |
| B | 向某溶液先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中含有SO42-、SO32-、HSO32-中的一种或几种 |
| C | 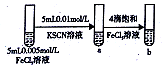 | 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
| D | 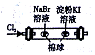 | 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性:Cl2>Br2>I2 |
| A. | A | B. | B | C. | C | D. | D |
2.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4LH2O2中所含H原子个数远大于2NA | |
| B. | 常温常压下,14.2g的Na2SO4和Na2S2O3的混合物含有Na原子个数为O.4NA | |
| C. | 标准状况下,1.5mol的MnO2粉末与足量浓盐酸共热转移电子数目小于3NA | |
| D. | 3.6gD2O所含质子数为2NA |
19.碱金属钫(Fr)具有放射性,它是碱金属元素中最重的元素,下列对其性质的预言中,不正确的是( )
| A. | 它的原子半径比钠大,失电子能力不如钠 | |
| B. | 它的金属性比钠强,跟水反应会更剧烈 | |
| C. | 它的氢氧化物(FrOH)是一种强碱,遇酚酞溶液变红 | |
| D. | 它可与硫酸铜溶液反应,但是不易得到金属铜 |
20.能用共价键键能大小解释的性质是( )
| A. | 稳定性:HCl>HI | B. | 密度:HI>HCl | C. | 沸点:HI>HCl | D. | 还原性:HI>HCl |

 .
. .
.