13.用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的是( )
| A. |  干燥Cl2 干燥Cl2 | B. |  吸收HCl | C. |  制备干燥的氨气 | D. |  吸收NH3 |
12.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,80gSO3的体积为22.4L | |
| B. | 标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA | |
| C. | 已知反应:2NH3+NO+NO2═2N2+3H2O,每生成28g N2转移的电子数目为3NA | |
| D. | 6.0gSiO2中含有0.1NA个 SiO2分子 |
11.用NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 100 mL 1 mol/L的FeCl3溶液完全生成Fe(OH)3胶体,其胶粒数目为0.1 NA | |
| B. | 7.8 gNa2O2中含有的离子总数目为0.4 NA | |
| C. | 标准状况下,44.8 L HF所含分子数为2 NA | |
| D. | 标准状况下,80 gSO3中所含的原子数为4 NA |
10.下列有关叙述中正确的是( )
| A. | 元素的性质随着相对原子质量的递增而呈周期性变化 | |
| B. | 元素的性质随着原子序数的递增而呈周期性变化 | |
| C. | 周期表中的主族中都既有非金属元素又有金属元素 | |
| D. | 原子的最外层电子数相同的元素,一定属于同一族 |
9.表为元素周期表的一部分.
请判断 X、Y、Z,并用相应的元素符号回答下列问题.
(1)X是Si,它的原子M层电子数是4.
(2)表中元素原子半径最大的是Si.
(3)Y在元素周期表中的位置是第二周期第ⅥA族,用电子式表示Y的最简单氢化物的形成过程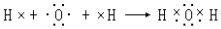 .
.
(4)氮气中氮原子之间的化学键属于共价键键,由氮气与氢气反应生成1mol氨气时转移电子的数目是3NA.
(5)硫与Z两种元素相比,非金属性强的是Cl,请用化学方程式说明这一结论H2S+Cl2=S↓+2HCl.
(6)碳、氮、Y三种元素的最简单气态氢化物的稳定性由强到弱的顺序是H2O>NH3>CH4.由最高价碳元素与最低价氮元素组成化合物的化学式是C3N4.
| 碳 | 氮 | Y | |
| X | 硫 | Z |
(1)X是Si,它的原子M层电子数是4.
(2)表中元素原子半径最大的是Si.
(3)Y在元素周期表中的位置是第二周期第ⅥA族,用电子式表示Y的最简单氢化物的形成过程
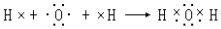 .
.(4)氮气中氮原子之间的化学键属于共价键键,由氮气与氢气反应生成1mol氨气时转移电子的数目是3NA.
(5)硫与Z两种元素相比,非金属性强的是Cl,请用化学方程式说明这一结论H2S+Cl2=S↓+2HCl.
(6)碳、氮、Y三种元素的最简单气态氢化物的稳定性由强到弱的顺序是H2O>NH3>CH4.由最高价碳元素与最低价氮元素组成化合物的化学式是C3N4.
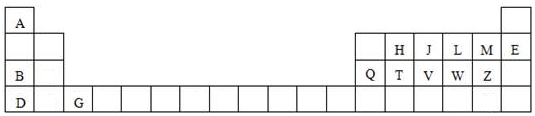
8. A、B、C、D四种短周期元素在周期表中的位置如图所示,其中C的原子序数是D的原子序数的2倍.下列有关说法正确的是( )
A、B、C、D四种短周期元素在周期表中的位置如图所示,其中C的原子序数是D的原子序数的2倍.下列有关说法正确的是( )
 A、B、C、D四种短周期元素在周期表中的位置如图所示,其中C的原子序数是D的原子序数的2倍.下列有关说法正确的是( )
A、B、C、D四种短周期元素在周期表中的位置如图所示,其中C的原子序数是D的原子序数的2倍.下列有关说法正确的是( )| A. | B 的M层电子数是K层的3倍 | |
| B. | C 的离子具有与 Na+相同的电子层结构 | |
| C. | A 与 D 形成的化合物属于离子化合物 | |
| D. | C 的简单阴离子比 D 的简单阴离子还原性强 |
6.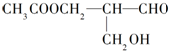 在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”.凡有一个手性碳原子的物质一定具有光学活性,下面的物质有光学活性:发生下列反应后生成的有机物无光学活性的是( )
在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”.凡有一个手性碳原子的物质一定具有光学活性,下面的物质有光学活性:发生下列反应后生成的有机物无光学活性的是( )
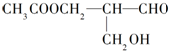 在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”.凡有一个手性碳原子的物质一定具有光学活性,下面的物质有光学活性:发生下列反应后生成的有机物无光学活性的是( )
在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”.凡有一个手性碳原子的物质一定具有光学活性,下面的物质有光学活性:发生下列反应后生成的有机物无光学活性的是( )| A. | 与甲酸发生酯化反应 | B. | 与新制的氢氧化铜作用 | ||
| C. | 与银氨溶液作用 | D. | 在催化剂存在下与H2作用 |
5.下列操作中,不正确的是( )
0 162717 162725 162731 162735 162741 162743 162747 162753 162755 162761 162767 162771 162773 162777 162783 162785 162791 162795 162797 162801 162803 162807 162809 162811 162812 162813 162815 162816 162817 162819 162821 162825 162827 162831 162833 162837 162843 162845 162851 162855 162857 162861 162867 162873 162875 162881 162885 162887 162893 162897 162903 162911 203614
| A. | 苯酚沾在手上应立即用酒精洗涤 | |
| B. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 | |
| C. | 点燃甲烷、乙烯等可燃性气体前必须先检验其纯度 | |
| D. | 在苯酚溶液中滴入少量稀溴水出现白色沉淀 |