题目内容
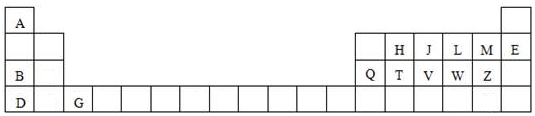
9.表为元素周期表的一部分.| 碳 | 氮 | Y | |
| X | 硫 | Z |
(1)X是Si,它的原子M层电子数是4.
(2)表中元素原子半径最大的是Si.
(3)Y在元素周期表中的位置是第二周期第ⅥA族,用电子式表示Y的最简单氢化物的形成过程
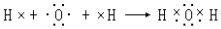 .
.(4)氮气中氮原子之间的化学键属于共价键键,由氮气与氢气反应生成1mol氨气时转移电子的数目是3NA.
(5)硫与Z两种元素相比,非金属性强的是Cl,请用化学方程式说明这一结论H2S+Cl2=S↓+2HCl.
(6)碳、氮、Y三种元素的最简单气态氢化物的稳定性由强到弱的顺序是H2O>NH3>CH4.由最高价碳元素与最低价氮元素组成化合物的化学式是C3N4.
分析 (1)X与碳位于同一主族,则X为Si元素,Si原子M层含有4个电子;
(2)电子层越大,原子半径越大,电子层相同时,核电荷数越大,原子半径越小;
(3)Y位于S的上一主族,为O元素,原子序数为8,据此判断O的位置;Y的简单氢化物为水,水分子为共价化合物,分子中含有2个O-H键;
(4)氮气分子中含有的N-N键为共价键;氨气分子中N元素的化合价为-1价,生成1mol氨气转移了3mol电子;
(5)Z的原子序数比S元素大1,位Cl元素,同一周期中,核电荷数越大,非金属性越强,通过单质间的置换反应可以证明;
(6)非金属性越强,最简单气态氢化物的稳定性越强;C的最高价为+4,N的最低价为-3,据此判断二者形成化合物的化学式.
解答 解:(1)根据各元素相对位置可知,X位于碳的下一主族,为Si元素,Si最外层M层含有4个电子,
故答案为:Si; 4;
(2)Si元素位于第三周期,且表中第三周期元素中Si的原子序数最小,则Si的原子半径最大,
故答案为:Si;
(3)Y与S位于同一主族,则Y为O元素,位于周期表中第二周期ⅥA,O的氢化物为水,水分子为共价化合物,用电子式表示其形成过程为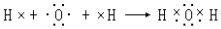 ,
,
故答案为:二;ⅥA;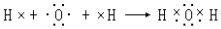 ;
;
(4)氮气中氮原子之间的化学键属于共价键;氨气分子中N元素的化合价为-3价,则由氮气与氢气反应生成1mol氨气时转移了3mol电子,转移电子的数目是3NA,
故答案为:共价键;3;
(5)Z比S的原子序数多1,其原子序数为17,是Cl元素,Cl、S位于同一周期,原子序数越大,非金属性越强,则Cl的非金属性较强,通过反应 H2S+Cl2=S↓+2HCl可以证明,
故答案为:Cl; H2S+Cl2=S↓+2HCl;
(6)非金属性:O>N>C,则碳、氮、O三种元素的最简单气态氢化物的稳定性由强到弱的顺序是:H2O>NH3>CH4,
碳元素最高价碳为+4,N的最低价氮为-3,则最高价碳元素与最低价氮元素组成化合物的化学式C3N4,
故答案为:H2O>NH3>CH4;C3N4.
点评 本题考查位置、结构与性质关系的应用,题目难度不大,推断元素为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题知识点较多,充分考查了学生的分析能力及综合应用能力.

| A. | 电解饱和食盐水,产生黄绿色气体:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2+Cl2 | |
| B. | 用Na2CO3溶液将水垢中的CaSO4转化为CaCO3:CO32-+Ca2+=CaCO3 | |
| C. | 向H202溶液中滴加CuSO4溶液,产生气泡:2H2O2 $\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2 T | |
| D. | 向苯酚浊液中滴加Na2CO3溶液,溶液变澄清: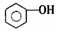 +CO32-→ +CO32-→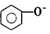 +HCO3- +HCO3- |
| A. | 如图的键线式表示烃的名称为3-甲基-4-乙基-7-甲基辛烷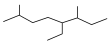 | |
| B. | 符合分子式为C3H8O的醇有三种不同的结构 | |
| C. | 乙烯在一定条件下能发生加成反应、加聚反应,被酸性高锰酸钾溶液氧化,也能在一定条件下被氧气氧化成乙酸 | |
| D. | 溴水能将 甲苯、乙烯、乙醇、四氯化碳、乙酸五种溶液鉴别开来 |
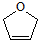 是一种有机烯醚,可由链烃A通过下列路线制得,下列说法正确的是( )
是一种有机烯醚,可由链烃A通过下列路线制得,下列说法正确的是( )A$→_{①}^{Br_{2}/CCl_{4}}$B$→_{②}^{NaOH溶液}$C$→_{△③}^{浓H_{2}SO_{4}}$
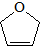
| A. | B中含有的官能团有溴原子、碳碳双键 | |
| B. | A的结构简式是CH2═CHCH2CH3 | |
| C. | 该有机烯醚不能发生加聚反应 | |
| D. | ①②③的反应类型分别为加成反应、取代反应、消去反应 |
| A. | 7.8gNa2O2中含阴离子的数目为0.1NA | |
| B. | 25℃时,1L pH=1的H2SO4溶液中含H+的数目为0.2NA | |
| C. | 9.0g淀粉和葡萄糖的混合物中含碳原子的数目为0.3NA | |
| D. | 将10mL 1mol/L FeCl3溶液滴入沸水中,所得氢氧化铁胶粒的数目为0.01NA |
| A. | 生理盐水和A1(OH)3胶体的本质区别是能否产生丁达尔效应 | |
| B. | 纤维素和聚氯乙烯均为可降解的高分子化合物 | |
| C. | 水晶项链和玻璃杯均属于硅酸盐产品 | |
| D. | 耐蚀合金的防腐原理与电化学无关 |
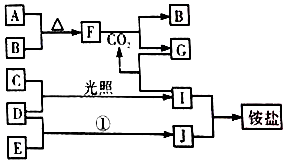 如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金单质,且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种重要固氮反应
如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金单质,且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种重要固氮反应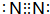 ,F
,F ;
; ;
;