3.下列的实验操作、现象与解释均正确的是( )
| 编号 | 实验操作 | 实验现象 | 解释 |
| A | 将铜粉加入1.0mol/LFe(SO4)3溶液中 | 溶液变蓝 | 金属铁比铜活泼 |
| B | 将在Na2SiO3稀溶液中浸泡过的小木条立即置于酒精灯外焰 | 小木条不易燃烧 | Na2SiO3溶液有阻燃的作用 |
| C | 向NaBr溶液中滴加氯水 | 溶液颜色变成橙黄色 | 氯水中含有HClO |
| D | 将一小块金属钠放置于坩埚里加热 | 钠块先融化成小球,再燃烧 | 钠的熔点比钠的着火点低 |
| A. | A | B. | B | C. | C | D. | D |
2.下列实验操作,对实验结果不产生影响的是( )
| A. | 在淀粉溶液中加入稀硫酸加热一段时间后,再滴加银氨溶液检验淀粉的水解产物 | |
| B. | 测定中和反应的反应热时,将碱溶液缓慢倒入酸溶液中 | |
| C. | 用蒸馏水湿润pH试纸后测定硫酸钠溶液的pH | |
| D. | 用酸碱中和滴定法测定未知浓度的碱液时,在锥形瓶中加入2-3mL酚酞试液作指示剂 |
1.下列关于有机化合物的说法正确的是( )
| A. | 乙烷、苯、葡萄糖溶液均不能使酸性高锰酸钾溶液褪色 | |
| B. | 2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物数目相同 | |
| C. | 苯的密度比水小,但由苯反应制得的溴苯、硝基苯、环己烷的密度都比水大 | |
| D. | 油脂的皂化反应属于加成反应 |
20.肼(N2H4)是一种高能燃料,在生产和研究中用途广泛.化学小组同学在实验室中用过量NH3和NaC1O溶液反应制取N2H4(液)并探究其性质.回答下列问题:
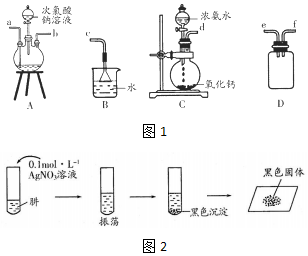
(1)肼的制备
①用图1装置制取肼,其连接顺序为defabc(按气流方向,用小写字母表示).
②装置A中发生反应的化学方程式为NaClO+2NH3=N2H4+NaCl+H2O,装置D的作用是防止倒吸或安全瓶.
(2)探究:N2H4和AgNO3溶液的反应将制得的肼分离提纯后,进行如下实验如图2:
证明黑色沉淀已洗涤干净的操作是取最后一次洗涤液少许于试管中,滴加NaCl溶液,无白色沉淀生成说明沉淀已洗涤干净.
【查阅资料】N2H4水溶液的碱性弱于氨水;N2H4有强还原性.AgOH在溶液中不稳定易分解生成Ag2O;Ag2O和粉末状的Ag均为黑色;Ag2O可溶于氨水.
【提出假设】
假设1:黑色固体可能是Ag;
假设2:黑色固体可能是Ag2O;
假设3:黑色固体可能是Ag和Ag2O.
【实验验证】该同学基于上述假设,设计如下方案,进行实验,请完成下表中的空白部分.
根据实验现象,假设1成立,则N2H4与AgNO3溶液反应的离子方程式为N2H4+4Ag+=4Ag↓+N2↑+4H+.

(1)肼的制备
①用图1装置制取肼,其连接顺序为defabc(按气流方向,用小写字母表示).
②装置A中发生反应的化学方程式为NaClO+2NH3=N2H4+NaCl+H2O,装置D的作用是防止倒吸或安全瓶.
(2)探究:N2H4和AgNO3溶液的反应将制得的肼分离提纯后,进行如下实验如图2:
证明黑色沉淀已洗涤干净的操作是取最后一次洗涤液少许于试管中,滴加NaCl溶液,无白色沉淀生成说明沉淀已洗涤干净.
【查阅资料】N2H4水溶液的碱性弱于氨水;N2H4有强还原性.AgOH在溶液中不稳定易分解生成Ag2O;Ag2O和粉末状的Ag均为黑色;Ag2O可溶于氨水.
【提出假设】
假设1:黑色固体可能是Ag;
假设2:黑色固体可能是Ag2O;
假设3:黑色固体可能是Ag和Ag2O.
【实验验证】该同学基于上述假设,设计如下方案,进行实验,请完成下表中的空白部分.
| 实验编号 | 操作 | 现象 | 实验结论 |
| 1 | 取少量黑色固体于试管,加入足量氨水,振荡 | 黑色固体不溶解 | 假设1成立 |
| 2 | 操作同实验1 | 黑色固体完全溶解 | 假设2成立 |
| 3 | ①取少量黑色固体于试管中,加入适量氨水,振荡,静置,取上层清液于洁净试管中,加入几滴乙醛,水浴加热②取少量黑色固体于试管中,加入足量稀硝酸,振荡 | ①试管内壁有银镜生成 ②固态完全溶解,并有气体产生 | 假设3成立 |
18.下列有关化学用语表达正确的是( )
| A. | NH4Cl 的电子式: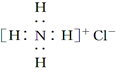 | B. | 次氯酸的结构式:H-Cl-O | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 用电子式表示氧化钠的形成过程: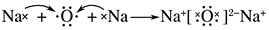 |
17.下列说法中不正确的是( )
| A. | 碱金属元素锂、钠、钾、铷、铯,随着核电荷数的增加其单质的熔沸点逐渐降低 | |
| B. | 卤族元素氟、氯、溴、碘,随着核电荷数的增加其单质的熔沸点逐渐升高 | |
| C. | NaOH、KOH、Mg(OH)2的碱性依次减弱 | |
| D. | 在周期表中金属与非金属的分界处可以找到半导体材料 |
16.下列反应的离子方程式及对应的说法都正确的是( )
| A. | 碳酸氢钙溶液加到醋酸溶液中:Ca(HCO3)2+2CH3COOH═Ca2++2CH3COO-+2CO2↑+2H2O | |
| B. | 漂白粉溶液中通入过量的CO2:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO3 | |
| C. | Fe-Cu-H2SO4溶液组成的原电池中负极反应式为:Fe-3e-=Fe3+ | |
| D. | 在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
15.下列有机物命名正确的是( )
| A. | 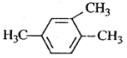 1,3,4-三甲苯 1,3,4-三甲苯 | B. | 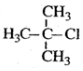 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 | C. | 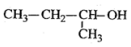 2-甲基-1-丙醇 2-甲基-1-丙醇 | D. | 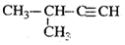 2-甲基-3-丁炔 2-甲基-3-丁炔 |
14.下列关子有机化合物的说法正确的是( )
0 162707 162715 162721 162725 162731 162733 162737 162743 162745 162751 162757 162761 162763 162767 162773 162775 162781 162785 162787 162791 162793 162797 162799 162801 162802 162803 162805 162806 162807 162809 162811 162815 162817 162821 162823 162827 162833 162835 162841 162845 162847 162851 162857 162863 162865 162871 162875 162877 162883 162887 162893 162901 203614
| A. | 以淀粉为原料可以制取乙酸乙酸 | |
| B. | 油脂的皂化反应属于加成反应 | |
| C. | 乙酸中所有原子可能处于同一平面 | |
| D. | 分子式为C3H6Cl2的同分异构体有5种(不考虑立体异构) |



