2.大苏打是五水合硫代硫酸钠(Na2S2O3•5H2O)的俗称,又称海波,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成.向Na2CO3和Na2S混合溶液中通入SO2反应后制得Na2S2O3•5H2O,通常制得的产品含有少量Na2SO3和Na2SO4.
Ⅰ、某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O),实验装置如图所示(省略夹持装置):
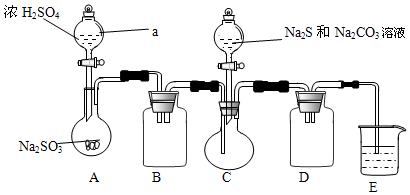
实验步骤:
(1)检查装置气密性,按图示加入试剂.仪器a的名称是分液漏斗,组装仪器之前必须检查仪器a是否漏水的操作是关闭活塞,向分液漏斗内注入一定量水,观察活塞是否漏水,旋转活塞1800观察活塞是否漏水.E中NaOH溶液的作用是吸收SO2,防止污染空气.
(2)先向C中烧瓶加入Na2S和Na2CO3混合溶液,再向A中烧瓶滴加H2SO4.A装置中发生反应的化学方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O.
(3)待C反应结束后,过滤其混合物,将滤液蒸发浓缩、结晶、过滤、洗涤、干燥,得到产品.
Ⅱ.【探究与反思】
(4)为验证产品 中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整.(所需试剂从稀HNO3、稀H2SO4、稀HCl、BaCl2溶液、蒸馏水中选择)
(5)为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验步骤(2)进行了改进,改进后的操作是先向A中烧瓶滴加浓H2SO4,产生的气体将装置中空气排尽后,再向C中烧瓶加入Na2S和Na2CO3混合溶液.
(6)为测定所得样品中Na2S2O3•5H2O的纯度,称取mg产品配成稀溶液并除去Na2SO3和Na2SO4,然后用c mol•L-1标准碘溶液进行滴定(用淀粉溶液作指示剂),反应方程式为2Na2S2O3+I2═2NaI+Na2S4O6.若三次滴定平均消耗碘溶液的体积为V mL,则测量的Na2S2O3•5H2O的纯度为$\frac{49.6cV}{m}$%.(已知Na2S2O3•5H2O的式量是248)
Ⅰ、某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O),实验装置如图所示(省略夹持装置):

实验步骤:
(1)检查装置气密性,按图示加入试剂.仪器a的名称是分液漏斗,组装仪器之前必须检查仪器a是否漏水的操作是关闭活塞,向分液漏斗内注入一定量水,观察活塞是否漏水,旋转活塞1800观察活塞是否漏水.E中NaOH溶液的作用是吸收SO2,防止污染空气.
(2)先向C中烧瓶加入Na2S和Na2CO3混合溶液,再向A中烧瓶滴加H2SO4.A装置中发生反应的化学方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O.
(3)待C反应结束后,过滤其混合物,将滤液蒸发浓缩、结晶、过滤、洗涤、干燥,得到产品.
Ⅱ.【探究与反思】
(4)为验证产品 中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整.(所需试剂从稀HNO3、稀H2SO4、稀HCl、BaCl2溶液、蒸馏水中选择)
| 实验操作 | 现象 | 结论 |
| 取适量产品配成稀溶液,滴加足量BaCl2溶液 | 有白色沉淀生成 | |
| 过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀HCl | 沉淀部分溶解,并有刺激性气味的气体产生 | 确定产品中含有Na2SO3和Na2SO4 |
(6)为测定所得样品中Na2S2O3•5H2O的纯度,称取mg产品配成稀溶液并除去Na2SO3和Na2SO4,然后用c mol•L-1标准碘溶液进行滴定(用淀粉溶液作指示剂),反应方程式为2Na2S2O3+I2═2NaI+Na2S4O6.若三次滴定平均消耗碘溶液的体积为V mL,则测量的Na2S2O3•5H2O的纯度为$\frac{49.6cV}{m}$%.(已知Na2S2O3•5H2O的式量是248)
1.下列叙述中错误的是( )
| A. | 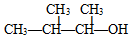 的命名为:3-甲基-2-丁醇 的命名为:3-甲基-2-丁醇 | |
| B. | 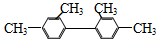 分子中至少有11个碳原子处于同一平面 分子中至少有11个碳原子处于同一平面 | |
| C. | 羟基的电子式是 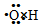 | |
| D. | 软脂酸和油酸互为同系物 |
20.NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 16 g O2和O3 的混合气体中含有的分子数为0.5 NA | |
| B. | 25℃时,Ksp(BaSO4)=1×10-10,则BaSO4饱和溶液中Ba2+数日为1×10-5 NA | |
| C. | 标准状况下,2.24 L Cl2 通入足量H2O或NaOH溶液中转移的电子数均为0.1 NA | |
| D. | 常温下,1 mol的NaHCO3固体中含HCO3-的数目为NA |
19.下列与化学有关的说法中错误的是( )
| A. | 候氏制碱、制取肥皂的工艺过程中均应用了物质溶解度的差异 | |
| B. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦提取青蒿素的过程中发生了化学变化 | |
| C. | “外观如雪,强烧之,紫青烟起”,南北朝陶弘景对硝酸钾的鉴定过程中利用了焰色反应 | |
| D. | 使用可再生资源、用超临界二氧化碳替代有机溶剂、注重原子的经济性、采用低能耗生产工艺等都是绿色化学的内容 |
18. MnSO4在工业中有重要应用.用软锰矿浆(主要成分为MnO2和水,含有Fe2O3、FeO、Al2O3和少量PbO等杂质)浸出制备MnSO4,其过程如下:
MnSO4在工业中有重要应用.用软锰矿浆(主要成分为MnO2和水,含有Fe2O3、FeO、Al2O3和少量PbO等杂质)浸出制备MnSO4,其过程如下:
I. 向软锰矿浆中通入SO2,锰、铁、铝、铅元素以离子形式浸出,测得浸出液的pH<2.
II. 向浸出液中加MnO2,充分反应后,加入石灰乳,调溶液pH=4.7.
III.再加入阳离子吸附剂,静置后过滤.
IV.滤液蒸发浓缩,冷却结晶,获得MnSO4晶体.
【资料】部分阳离子形成氢氧化物沉淀的pH
(1)I中向软锰矿浆中通入SO2生成MnSO4,该反应的化学方程式是SO2+MnO2=MnSO4.
(2)II 中加入MnO2的主要目的是将Fe2+氧化为Fe3+;调溶液 pH=4.7,生成的沉淀主要含有Fe(OH)3、Al(OH)3
和少量CaSO4.
(3)III中加入阳离子吸附剂,主要除去的离子是Ca2+、Pb2+.
(4)用惰性电极电解MnSO4溶液,可以制得高活性MnO2.
①电解MnSO4溶液的离子方程式是Mn2++2H2O$\frac{\underline{\;通电\;}}{\;}$MnO2+H2↑+2H+.
②高活性MnO2可用于催化降解甲醛,有关微粒的变化如图所示,其中X是HCO3-,总反应的化学方程式是HCHO+O2$\frac{\underline{\;MnO_{2}\;}}{\;}$CO2+H2O.
 MnSO4在工业中有重要应用.用软锰矿浆(主要成分为MnO2和水,含有Fe2O3、FeO、Al2O3和少量PbO等杂质)浸出制备MnSO4,其过程如下:
MnSO4在工业中有重要应用.用软锰矿浆(主要成分为MnO2和水,含有Fe2O3、FeO、Al2O3和少量PbO等杂质)浸出制备MnSO4,其过程如下:I. 向软锰矿浆中通入SO2,锰、铁、铝、铅元素以离子形式浸出,测得浸出液的pH<2.
II. 向浸出液中加MnO2,充分反应后,加入石灰乳,调溶液pH=4.7.
III.再加入阳离子吸附剂,静置后过滤.
IV.滤液蒸发浓缩,冷却结晶,获得MnSO4晶体.
【资料】部分阳离子形成氢氧化物沉淀的pH
| 离子 | Fe2+ | Fe3+ | Al3+ | Mn2+ | Pb2+ |
| 开始沉淀时的pH | 7.6 | 2.7 | 3.8 | 8.3 | 8.0 |
| 完全沉淀时的pH | 9.7 | 3.7 | 4.7 | 9.8 | 8.8 |
(2)II 中加入MnO2的主要目的是将Fe2+氧化为Fe3+;调溶液 pH=4.7,生成的沉淀主要含有Fe(OH)3、Al(OH)3
和少量CaSO4.
(3)III中加入阳离子吸附剂,主要除去的离子是Ca2+、Pb2+.
(4)用惰性电极电解MnSO4溶液,可以制得高活性MnO2.
①电解MnSO4溶液的离子方程式是Mn2++2H2O$\frac{\underline{\;通电\;}}{\;}$MnO2+H2↑+2H+.
②高活性MnO2可用于催化降解甲醛,有关微粒的变化如图所示,其中X是HCO3-,总反应的化学方程式是HCHO+O2$\frac{\underline{\;MnO_{2}\;}}{\;}$CO2+H2O.
17. 在一定条件下,利用CO2合成CH3OH的反应如下:
在一定条件下,利用CO2合成CH3OH的反应如下:
CO2(g)+3H2(g)?H3OH(g)+H2O(g)△H1,
研究发现,反应过程中会有副反应:
CO2(g)+H2(g)?CO(g)+H2O(g)△H2.
温度对CH3OH、CO的产率影响如图所示.下列说法中,不正确的是( )
 在一定条件下,利用CO2合成CH3OH的反应如下:
在一定条件下,利用CO2合成CH3OH的反应如下:CO2(g)+3H2(g)?H3OH(g)+H2O(g)△H1,
研究发现,反应过程中会有副反应:
CO2(g)+H2(g)?CO(g)+H2O(g)△H2.
温度对CH3OH、CO的产率影响如图所示.下列说法中,不正确的是( )
| A. | △H1<0,△H2>0 | |
| B. | 增大压强有利于加快合成反应的速率 | |
| C. | 生产过程中,温度越高越有利于提高CH3OH的产率 | |
| D. | 合成CH3OH反应的平衡常数表达式是K=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$ |
16.下列事实不能用元素周期律解释的是( )
| A. | 酸性:HClO4>H2SO4 | |
| B. | Na、Mg与水反应,Na更剧烈 | |
| C. | 气态氢化物的稳定性:HF>HCl | |
| D. | 向Na2SO3溶液中加盐酸,有气泡产生 |
15.下列事实与水解反应无关的是( )
| A. | 用Na2S除去废水中的Hg2+ | B. | 用热的Na2CO3溶液去油污 | ||
| C. | 利用油脂的皂化反应制造肥皂 | D. | 配制CuSO4溶液时加少量稀H2SO4 |
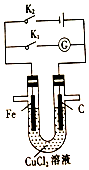
13.由U形管、铁棒、石墨棒、1L 0.lmol/LC uCl2溶液等组成如图装置,下列说法不正确的是( )
0 162664 162672 162678 162682 162688 162690 162694 162700 162702 162708 162714 162718 162720 162724 162730 162732 162738 162742 162744 162748 162750 162754 162756 162758 162759 162760 162762 162763 162764 162766 162768 162772 162774 162778 162780 162784 162790 162792 162798 162802 162804 162808 162814 162820 162822 162828 162832 162834 162840 162844 162850 162858 203614

| A. | 同时打开K1、K2,铁棒上有紫红色物质析出 | |
| B. | 只闭合K1,石墨棒上有紫红色物质析出 | |
| C. | 只闭合K2,当电路中通过0.3mol电子时,两极共产生4.48L(标准状况)气体 | |
| D. | 只闭合K2,一段时间后,将电解质溶液搅拌均匀,溶液的pH变大(不考虑Cl2的溶解) |
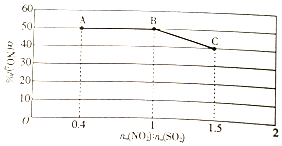 已知NO2与以SO2能发生反应:NO2(g)+SO2(g)?SO3(g)+NO(g).
已知NO2与以SO2能发生反应:NO2(g)+SO2(g)?SO3(g)+NO(g).