19.氮氧化物、二氧化硫是造成大气污染的主要物质,某科研小组进行如下研究.
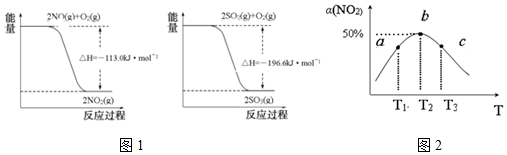
(1)已知:写出SO2(g)与NO2(g)反应生成SO3(g)和NO(g)的热化学方程式SO2(g)+NO2(g)=SO3(g)+NO(g)△H=-41.8kJ/mol.
(2)向容积为1L密闭容器中分别充入0.10mol NO2和0.15mol SO2,在不同温度下测定同一时刻NO2的转化率,结果如图1所示.
①如图2a、c两点反应速率大小关系:υ(a)<υ(c).(填“>”、“<”或“=”)
②温度为T2时从反应开始经过2min达到b点,用SO3表示这段时间的反应速率为0.025mol•L-1•min-1,此温度下该反应的平衡常数为0.5,若在此温度下,保持容器的容积不变,再向容器中充入0.20mol NO2和0.30mol SO2,NO2的转化率不变.(填“增大”、“减小”或“不变”)
③NO2的转化率随温度升高先增大后减小的原因是:温度为T2,b点为平衡点,T2以前温度升高,反应速率加快,NO2转化率增大,T2以后,该反应为放热反应,升高温度,平衡向逆反应方向移动,转化率减小.
(3)常温下用NaOH溶液吸收SO2,在吸收过程中,溶液pH随n(SO32-):n(HSO3-)变化关系如表:
①当吸收液呈中性时,溶液中离子浓度由大到小排列顺序为c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-).
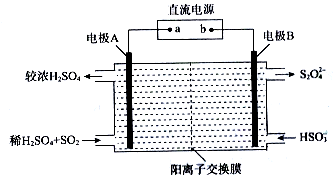
②当向NaOH溶液中通入足量的SO2时,得到NaHSO3溶液,在pH为4~7之间电解,硫元素在阴极上被还原为Na2S2O4,这是电化学脱硫技术之一,写出该阴极的电极反应式2HSO3-+2H++2e-=S2O42-+2H2O.

(1)已知:写出SO2(g)与NO2(g)反应生成SO3(g)和NO(g)的热化学方程式SO2(g)+NO2(g)=SO3(g)+NO(g)△H=-41.8kJ/mol.
(2)向容积为1L密闭容器中分别充入0.10mol NO2和0.15mol SO2,在不同温度下测定同一时刻NO2的转化率,结果如图1所示.
①如图2a、c两点反应速率大小关系:υ(a)<υ(c).(填“>”、“<”或“=”)
②温度为T2时从反应开始经过2min达到b点,用SO3表示这段时间的反应速率为0.025mol•L-1•min-1,此温度下该反应的平衡常数为0.5,若在此温度下,保持容器的容积不变,再向容器中充入0.20mol NO2和0.30mol SO2,NO2的转化率不变.(填“增大”、“减小”或“不变”)
③NO2的转化率随温度升高先增大后减小的原因是:温度为T2,b点为平衡点,T2以前温度升高,反应速率加快,NO2转化率增大,T2以后,该反应为放热反应,升高温度,平衡向逆反应方向移动,转化率减小.
(3)常温下用NaOH溶液吸收SO2,在吸收过程中,溶液pH随n(SO32-):n(HSO3-)变化关系如表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
②当向NaOH溶液中通入足量的SO2时,得到NaHSO3溶液,在pH为4~7之间电解,硫元素在阴极上被还原为Na2S2O4,这是电化学脱硫技术之一,写出该阴极的电极反应式2HSO3-+2H++2e-=S2O42-+2H2O.
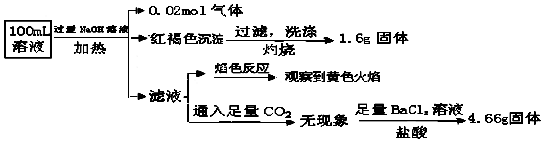
16.某溶液可能含有Clˉ、SO42ˉ、CO32ˉ、NH4+、Fe3+、Fe2+ 和Na+.某同学为了确认其成分,取部分试液,设计并完成了如下实验:下列说法正确的是( )
0 162573 162581 162587 162591 162597 162599 162603 162609 162611 162617 162623 162627 162629 162633 162639 162641 162647 162651 162653 162657 162659 162663 162665 162667 162668 162669 162671 162672 162673 162675 162677 162681 162683 162687 162689 162693 162699 162701 162707 162711 162713 162717 162723 162729 162731 162737 162741 162743 162749 162753 162759 162767 203614

| A. | 原溶液中c(Fe3+)=0.2mol•L-1 | |
| B. | 溶液中至少有4种离子存在,其中Clˉ一定存在,且c(Clˉ)≥0.2mol•L-1 | |
| C. | SO42ˉ、NH4+、Na+一定存在,CO32ˉ一定不存在 | |
| D. | 要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加入适量氯水,无现象,再加KSCN溶液,溶液成血红色,则含有Fe2+ |
 ,反应类型为酯化反应.
,反应类型为酯化反应.