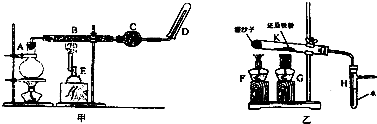
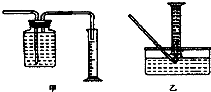
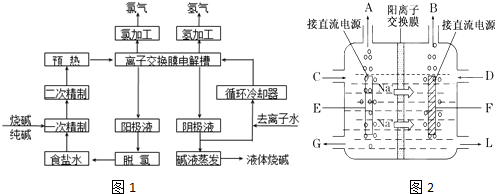
9.在一定条件下发生反应2A(g)═2B(g)+C(g),将2mol A通入2L容积恒定的密闭容器甲中,若维持容器内温度不变,5min末测得A的物质的量为0.8mol.用B的浓度变化来表示该反应的速率为( )
| A. | 0.24 mol/(L•min) | B. | 0.08 mol/(L•min) | C. | 0.06 mol/(L•min) | D. | 0.12 mol/(L•min) |
7.1919年,Langmuir提出等电子原理:原子数相同、电子总数相同的微粒,互称为等电子体.等电子体的结构相似、物理性质相近.根据上述原理,下列微粒中,不互为等电子体的是( )
| A. | N2 和 CO | B. | CO2 和 N2O | C. | O3 和 CO2 | D. | CO32- 和 NO3- |
6.下列有关推断中,不正确的是( )
| 事 实 | 结 论 | |
| A | CaCO3+2CH3COOH=(CH3COO)2Ca+CO2↑+H2O | 酸性:CH3COOH>H2CO3 |
| B | 氢硫酸(H2S)放置在空气中变浑浊 | 氧化性:O2>S |
| C | Al(OH)3既溶于强酸又溶于强碱 | Al元素既有金属性也有非金属性 |
| D | 反应A+2B?C达平衡后,升高温度平衡正向移动 | 升高温度,使v正增大、v逆减小 |
| A. | A | B. | B | C. | C | D. | D |
5.某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子,在ag HmX中所含质子的物质的量是( )
| A. | $\frac{a}{A+n}$mol | B. | $\frac{a}{A}$mol | C. | $\frac{(A-N+m)a}{A+m}$mol | D. | $\frac{a}{A}$mol |
3.下列关于金属铝的叙述中,不正确的是( )
| A. | Al是地壳中含量最多的金属元素,但铝是使用较晚的金属 | |
| B. | Al是比较活泼的金属,在化学反应中容易失去电子,表现还原性 | |
| C. | Al箔在空气中受热可以熔化,且发生剧烈燃烧 | |
| D. | Al箔在空气中受热可以熔化,由于氧化膜的存在,熔化的Al并不滴落 |
1.有时候,将氧化还原反应方程式拆开写成两个“半反应”.下面是一个“半反应”式:MnO4-+____H++____e---____Mn2++____H2O
该反应方程式的配平化学计量数是( )
该反应方程式的配平化学计量数是( )
| A. | 1,8,4,1,4 | B. | 2,16,5,2,8 | C. | 1,6,5,1,3 | D. | 1,8,5,1,4 |
13.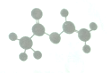 法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖:轮烷是一种分子机器的一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )
法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖:轮烷是一种分子机器的一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )
0 162504 162512 162518 162522 162528 162530 162534 162540 162542 162548 162554 162558 162560 162564 162570 162572 162578 162582 162584 162588 162590 162594 162596 162598 162599 162600 162602 162603 162604 162606 162608 162612 162614 162618 162620 162624 162630 162632 162638 162642 162644 162648 162654 162660 162662 162668 162672 162674 162680 162684 162690 162698 203614
 法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖:轮烷是一种分子机器的一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )
法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖:轮烷是一种分子机器的一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )| A. | 该化合物的名称为乙酸乙酯 | |
| B. | 该化合物可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且反应类型相同 | |
| C. | 该化合物既能发生取代反应,又能发生加成反应和氧化反应 | |
| D. | 该化合物的同分异构体中,能与NaHCO3反应放出CO2的只有2种 |
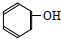 ②
② ③
③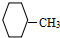 ④
④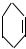 ⑤
⑤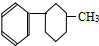 ⑥
⑥
 ⑧
⑧ ⑨
⑨ ⑩
⑩