题目内容
1.有时候,将氧化还原反应方程式拆开写成两个“半反应”.下面是一个“半反应”式:MnO4-+____H++____e---____Mn2++____H2O该反应方程式的配平化学计量数是( )
| A. | 1,8,4,1,4 | B. | 2,16,5,2,8 | C. | 1,6,5,1,3 | D. | 1,8,5,1,4 |
分析 反应中MnO4-中Mn从+7价降低到+2价,则需要得5个电子,再依据反应前后原子个数、电荷守恒配平,据此解答.
解答 解:反应中MnO4-中Mn从+7价降低到+2价,则需要得5个电子,依据反应前后电荷守恒,则需要8个H+,再依据反应前后原子个数,“半反应”式为MnO4-+8H++5e-=1Mn2++4H2O,
故选:D.
点评 本题考查了氧化还原反应方程式的书写,准确把握反应中各元素化合价变化,明确氧化还原反应得失电子守恒是解题关键,题目难度不大.

练习册系列答案
相关题目
5.对下列实验事实的解释不正确的是( )
| 现 象 | 解释或结论 | |
| A | SO2使酸性高锰酸钾溶液褪色 | SO2表现漂白性 |
| B | 浓硝酸在光照条件下变黄 | 浓硝酸不稳定,生成有色物质且能溶于浓硝酸 |
| C | 向饱和Na2CO3中通入足量CO2,溶液变浑浊 | 析出了NaHCO3 |
| D | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色. | Fe3+的氧化性比I2的强 |
| A. | A | B. | B | C. | C | D. | D |
2.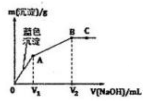 向含MgCl2和CuCl2的溶液中逐滴加入0.1 mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
向含MgCl2和CuCl2的溶液中逐滴加入0.1 mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
 向含MgCl2和CuCl2的溶液中逐滴加入0.1 mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
向含MgCl2和CuCl2的溶液中逐滴加入0.1 mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )| A. | 水的电离程度:A>B>C | |
| B. | 该实验不能证明Cu(OH)2的Ksp比Mg(OH)2的Ksp小 | |
| C. | 原溶液中MgCl2和CuCl2的物质的量浓度相等 | |
| D. | 若向Mg(OH)2悬浊液中加入CuCl2溶液,一定会有Cu(OH)2生成 |
9.当可逆反应CO+H2(g)?CO2+H2达到平衡后,改变条件达到新的平衡,体系中二氧化碳的体积百分含量增大,则平衡( )
| A. | 一定向正反应方向移动 | |
| B. | 一定向逆反应方向移动 | |
| C. | 不移动 | |
| D. | 可能向正反应方向移动,也可能向逆反应方向移动 |
6.下列有关推断中,不正确的是( )
| 事 实 | 结 论 | |
| A | CaCO3+2CH3COOH=(CH3COO)2Ca+CO2↑+H2O | 酸性:CH3COOH>H2CO3 |
| B | 氢硫酸(H2S)放置在空气中变浑浊 | 氧化性:O2>S |
| C | Al(OH)3既溶于强酸又溶于强碱 | Al元素既有金属性也有非金属性 |
| D | 反应A+2B?C达平衡后,升高温度平衡正向移动 | 升高温度,使v正增大、v逆减小 |
| A. | A | B. | B | C. | C | D. | D |
13.对于反应N2+O2$\frac{\underline{\;一定条件\;}}{\;}$2NO在密闭容器中进行,下列哪些条件能加快反应的速率( )
| A. | 缩小体积使压强增大 | B. | 增大体积使压强减小 | ||
| C. | 体积不变充入H2使压强增大 | D. | 压强不变充入N2使体积增大 |
10.下列离子方程式书写正确的是( )
| A. | 向饱和碳酸氢钙溶液中加入过量的NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| B. | 向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═NH3•H2O+Al(OH)3↓+2BaSO4↓ | |
| C. | 氢氧化钠溶液吸收足量SO2气体:SO2+2OH-═SO32-+H2O | |
| D. | 标准状况下,将1.12LCO2气体通入1L0.1mol/L的NaAlO2溶液中:CO2+2H2O+AlO2-═Al(OH)3↓+HCO3- |
11.200mL某硫酸盐溶液中,含硫酸根离子1.5NA个,含金属离子NA个,则该硫酸盐溶液的物质的量浓度为( )
| A. | 2.5mol/L | B. | 5mol/L | C. | 7.5mol/L | D. | 2mol/L |