11.下列关于电解质溶液的叙述正确的是( )
| A. | 常温下电离常数为Ka的酸HA 溶液中 c (H+)=$\sqrt{{K}_{a}}$mol•L-1 | |
| B. | 将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明Ksp[Ca(OH)2]大于Ksp(CaSO4) | |
| C. | 0.2mol•L-1 CH3COOH溶液与0.1mol•L-1NaOH溶液等体积混合2c(H+)-2c(OH-)═c(CH3COO-)-c(CH3COOH) | |
| D. | 向0.1mol•L-1的氨水中加入少量硫酸铵固体,则溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 |
10.表一是某种常见金属的部分性质:
表一:
将该金属投入到稀盐酸中,可产生大量的无色气体.根据上述信息回答下列问题:
(1)推断该金属的一种用途是做导线.
(2)该金属的活动性比铜强(填“强”或“弱”).
(3)请自选试剂,设计实验探究该金属与铁的活动性的强弱,并完成下表二:
表二:
表一:
| 颜色和状态 | 硬度 | 密度 | 熔点 | 导电性 | 导热性 | 延展性 |
| 银白色固体 | 较软 | 2.70g•cm-3 | 660.4℃ | 良好 | 良好 | 良好 |
(1)推断该金属的一种用途是做导线.
(2)该金属的活动性比铜强(填“强”或“弱”).
(3)请自选试剂,设计实验探究该金属与铁的活动性的强弱,并完成下表二:
表二:
| 一种猜想 | 验证方法 | 现象 | 结论 |
7.现有下列三个氧化还原反应:
①2B-+Z2=B2+2Z-②2A2++B2=2A3++2B-③2XO4-+10Z-+16H+=2X2++5Z2+8H2O
根据上述反应,判断下列结论中错误的是( )
①2B-+Z2=B2+2Z-②2A2++B2=2A3++2B-③2XO4-+10Z-+16H+=2X2++5Z2+8H2O
根据上述反应,判断下列结论中错误的是( )
| A. | 要除去含有 A2+、Z-和B-混合溶液中的A2+,而不氧化Z-和B-,应加入Z2 | |
| B. | 还原性强弱顺序为:A2+>B->Z->X2+ | |
| C. | X2+是 XO4- 的还原产物,B2是 B-的氧化产物 | |
| D. | 在溶液中可能发生反应:XO4-+5 A2++8H+=X2++5A3++4H2O |
5.下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作及现象 | 结论 |
| A | 测定等物质的量浓度的Na2CO3和Na2SO3溶液的pH,前者pH比后者的大 | 非金属性:S>C |
| B | 向苯酚浊液中滴加Na2CO3溶液,浊液变澄清 | CO32-结合质子能力比C6H5O-弱 |
| C | 向10mL 0.2mol•L-1NaOH溶液中滴入2滴0.1mol•L-1MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol•L-1FeCl3溶液,白色沉淀转化为红褐色沉淀 | 相同温度下的Ksp:Mg(OH)2>Fe(OH)3 |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置,下层溶液显紫红色 | Fe3+的氧化性大于I2 |
| A. | A | B. | B | C. | C | D. | D |
4.下列说法不正确的是( )
0 162483 162491 162497 162501 162507 162509 162513 162519 162521 162527 162533 162537 162539 162543 162549 162551 162557 162561 162563 162567 162569 162573 162575 162577 162578 162579 162581 162582 162583 162585 162587 162591 162593 162597 162599 162603 162609 162611 162617 162621 162623 162627 162633 162639 162641 162647 162651 162653 162659 162663 162669 162677 203614
| A. | 活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同 | |
| B. | 非金属氧化物不一定是酸性氧化物,金属氧化物多数是碱性氧化物 | |
| C. | 同温同压下,两份相同质量的铁粉,分别与足量的稀硫酸和稀硝酸反应,产生气体的体积不同 | |
| D. | 将SO2气体通入BaCl2溶液中至饱和未见沉淀生成,继续通入NO2则有沉淀生成 |
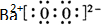 (写电子式).
(写电子式).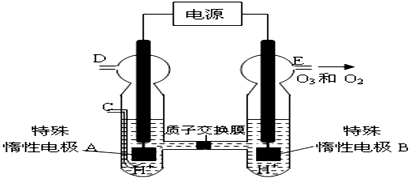
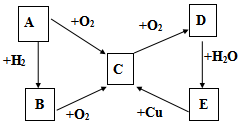 已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.
已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.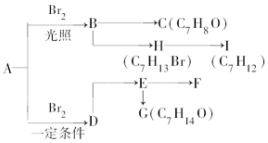 A是分子式为C7H8的芳香烃,已知它存在以下一系列转化关系,其中C是一种一元醇,D是A的对位一取代物,H与E、I与F分别互为同分异构体:
A是分子式为C7H8的芳香烃,已知它存在以下一系列转化关系,其中C是一种一元醇,D是A的对位一取代物,H与E、I与F分别互为同分异构体: ,
, .
.