18.下列各组物质在水中混合后,有白色沉淀且有刺激性气味的气体产生的是( )
| A. | NaHS、AlCl3 | B. | Al2(SO4)3、NaHCO3 | C. | Na2SO4、BaCO3 | D. | Na2CO3、CuSO4 |
17.下列有关装置I~Ⅳ的实验方法及操作的说法正确的是( )
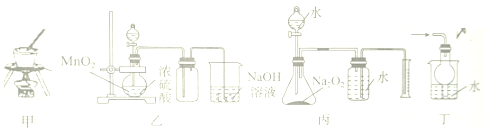

| A. | 利用甲装置甲从海水中提取NaCl晶体 | |
| B. | 利用装置乙制备并收集Cl2 | |
| C. | 利用装置丙测定变质Na2O2的纯度 | |
| D. | 利用装置丁吸收HCl尾气,防止液体倒吸 |
16.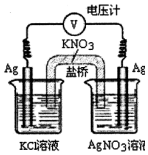 一定条件下,实验室利用如图所示装置,通过测电压求算Kkp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
一定条件下,实验室利用如图所示装置,通过测电压求算Kkp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
 一定条件下,实验室利用如图所示装置,通过测电压求算Kkp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
一定条件下,实验室利用如图所示装置,通过测电压求算Kkp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )| A. | 右池中的银电极作正极 | B. | 总反应为Ag++Cl-═AgCl | ||
| C. | 正极反应为Ag-e-═Ag+ | D. | 盐桥中的NO3-向右池方向移动 |
14.某有机物的结构简式为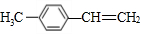 ,其分子结构中处在同一平面内的原子最多有( )
,其分子结构中处在同一平面内的原子最多有( )
 ,其分子结构中处在同一平面内的原子最多有( )
,其分子结构中处在同一平面内的原子最多有( )| A. | 15个 | B. | 16个 | C. | 17个 | D. | 18个 |
13.36.96L(标准状况)的H2、D2、O2的混合气体点燃正好完全反应,生成20g的H2O、D2O、HDO组成的水,原混合物中的O2的质量是( )
| A. | 16g | B. | 17.6g | C. | 17.8g | D. | 18g |
12.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1molCl2作为反应物,转移电子数一定为2NA | |
| B. | 25℃时,1.0LpH=13的Ba(OH)2溶液中水电离的OH-数目为0.1NA | |
| C. | 17g烃基和17gOH-含有的电子数均为10NA | |
| D. | 标准状况下,NA个NO分子和0.5NA个O2分子充分反应后气体分子数小于NA |
11. 某实验小组同学设计了如图装置,探究生铁与少置浓硫酸反应生成的气体产物.
某实验小组同学设计了如图装置,探究生铁与少置浓硫酸反应生成的气体产物.
(1)该实验的操作依次是CAB (填序号).
A.加热a试管直到b中澄淸石灰水变浑浊,熄灭酒精灯
B.将生铁丝上提离开液面
C.连接好装置,检验气密性,加人试剂
(2)b中的澄清石灰水变浑浊,甲同学认为产生的肯定是SO2气体,你是否同意不同意(填“同意”或“不同意)理由是.
(3)乙同学认为该反应过程中产生SO2、CO2、H2三种气体,请用如图所列各装置设计一个实验,来验证所产生的气体.(图中加热装置、夹持仪器省略,除装置⑤外,其他装置试剂均为足量)
①装置的连接顺序(按产物气流从左至右的方向→E→A→C→D→B(填装置的编号)
②证明生成的气体中存在SO2的现象是装置①中溶液紫红色变浅说明生成SO2,相应的离子方程式为5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+
(4)用2L0.3mol•L-1的NaOH溶液吸收标准状况下的11.2L的SO2气体生成的Na2SO3和NaHSO3的物质的量之比为1:4
(5)已知常温下H2SO3的电离平衡常数为:Ka1=10×10-1.9 Ka2=10-7.2计算0.1mol•L-1NaSO3溶液的pH
值10.1(忽略SO32-的二级水解)
 某实验小组同学设计了如图装置,探究生铁与少置浓硫酸反应生成的气体产物.
某实验小组同学设计了如图装置,探究生铁与少置浓硫酸反应生成的气体产物.(1)该实验的操作依次是CAB (填序号).
A.加热a试管直到b中澄淸石灰水变浑浊,熄灭酒精灯
B.将生铁丝上提离开液面
C.连接好装置,检验气密性,加人试剂
(2)b中的澄清石灰水变浑浊,甲同学认为产生的肯定是SO2气体,你是否同意不同意(填“同意”或“不同意)理由是.
(3)乙同学认为该反应过程中产生SO2、CO2、H2三种气体,请用如图所列各装置设计一个实验,来验证所产生的气体.(图中加热装置、夹持仪器省略,除装置⑤外,其他装置试剂均为足量)
| A | B | C | D | E |
 |  |  |  |  |
②证明生成的气体中存在SO2的现象是装置①中溶液紫红色变浅说明生成SO2,相应的离子方程式为5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+
(4)用2L0.3mol•L-1的NaOH溶液吸收标准状况下的11.2L的SO2气体生成的Na2SO3和NaHSO3的物质的量之比为1:4
(5)已知常温下H2SO3的电离平衡常数为:Ka1=10×10-1.9 Ka2=10-7.2计算0.1mol•L-1NaSO3溶液的pH
值10.1(忽略SO32-的二级水解)
10.在25℃时,H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是( )


| A. | H2R是二元弱酸,其Ka1=1×10-2 | |
| B. | NaHR在溶液中水解程度小于电离程度 | |
| C. | pH<7.2的溶液中一定存在:c( Na+)>c( HR-)>c(R2-)>c(H+)>c(OH-) | |
| D. | 含Na2R与NaHR各0.1 mol的混合溶液的pH=7.2 |
9.短周期元素R、T、X、Y、Z在元素周期表的相对位置如表所示,它们的最外层电子数之和为24.则下列判断正确的是( )
0 162453 162461 162467 162471 162477 162479 162483 162489 162491 162497 162503 162507 162509 162513 162519 162521 162527 162531 162533 162537 162539 162543 162545 162547 162548 162549 162551 162552 162553 162555 162557 162561 162563 162567 162569 162573 162579 162581 162587 162591 162593 162597 162603 162609 162611 162617 162621 162623 162629 162633 162639 162647 203614
| R | T | |
| X | Y | Z |
| A. | R位于元素周期表中第二周期第VA族 | |
| B. | R能分别与X、Z形成共价化合物 | |
| C. | 原子半径大小顺序为X>T>Y | |
| D. | Z元素的最高价氧化物对应的水化的化学式为HZO4 |