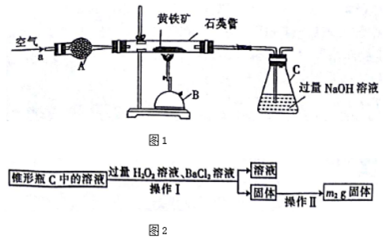
20. 雾霾天气严重影响人们的生活和健康.其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等.因此改善能源结构、机动车限号等措施能有效减少PM2.5、SO2、NOx等污染.
雾霾天气严重影响人们的生活和健康.其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等.因此改善能源结构、机动车限号等措施能有效减少PM2.5、SO2、NOx等污染.
请回答下列问题:
(1)将一定量的某利M2.5样品用蒸馏水溶解制成待测试样(忽略OH-).常温下测得该训试样的组成及其浓度如表一:根据表一中数据判断该试样的pH=4.
表一:
(2)汽车尾气中NOx和CO的生成:①已知汽缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是D.
A.混合气体的密度不再变化 B.混合气体的压强不再变化
C.N2、O2、NO的物质的量之比为1:1:2D.氧气的转化率不再变化
(3)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料.已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8KJ•mol-1
C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5KJ•mol-1
写出焦炭与水蒸气反应的热化学方程式:C(s)+H2O(g)═CO(g)+H2(g)△H=+13l.3kJ•mol-1.
②洗涤含SO2的烟气.下列可作为洗涤含SO2的烟气的洗涤剂的是AB.
A.浓氨水 B.碳酸氢钠饱和溶液 C.FeCl2饱和溶液 D.酸性CaCl2饱和溶液
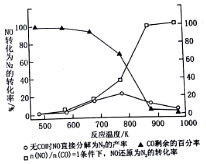
(4)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.某研究性小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示.若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因为NO的分解反应是放热反应,升温有利于反应逆向进行,在$\frac{n(NO)}{n(CO)}$=1的条件下,为更好的除去NOx物质,应控制的最佳温度在870K左右.
(5)车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如表二:
表二:
①写出NO与活性炭反应的化学方程式C+2NO?N2+CO2,②若T1<T2,则该反应的△H<O (填”>”、“<”或“=”).
③上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为80%.
 雾霾天气严重影响人们的生活和健康.其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等.因此改善能源结构、机动车限号等措施能有效减少PM2.5、SO2、NOx等污染.
雾霾天气严重影响人们的生活和健康.其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等.因此改善能源结构、机动车限号等措施能有效减少PM2.5、SO2、NOx等污染.请回答下列问题:
(1)将一定量的某利M2.5样品用蒸馏水溶解制成待测试样(忽略OH-).常温下测得该训试样的组成及其浓度如表一:根据表一中数据判断该试样的pH=4.
表一:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度mol/L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
A.混合气体的密度不再变化 B.混合气体的压强不再变化
C.N2、O2、NO的物质的量之比为1:1:2D.氧气的转化率不再变化
(3)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料.已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8KJ•mol-1
C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5KJ•mol-1
写出焦炭与水蒸气反应的热化学方程式:C(s)+H2O(g)═CO(g)+H2(g)△H=+13l.3kJ•mol-1.
②洗涤含SO2的烟气.下列可作为洗涤含SO2的烟气的洗涤剂的是AB.
A.浓氨水 B.碳酸氢钠饱和溶液 C.FeCl2饱和溶液 D.酸性CaCl2饱和溶液
(4)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.某研究性小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示.若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因为NO的分解反应是放热反应,升温有利于反应逆向进行,在$\frac{n(NO)}{n(CO)}$=1的条件下,为更好的除去NOx物质,应控制的最佳温度在870K左右.
(5)车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如表二:
表二:
| 物质 温度/℃ | 活性炭 | NO | E | F |
| 初始 | 3.000 | 0.10 | 0 | 0 |
| T1 | 2.960 | 0.020 | 0.040 | 0.040 |
| T2 | 2.975 | 0.050 | 0.025 | 0.025 |
③上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为80%.
19.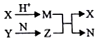 短周期元素A、B、C、D的原子序数依次增大,B和D同主族;X、Y、N分别是由以上四种元素中的两种组成的化合物,Z是由以上三种元素组成的化合物;若X与Y摩尔质量相同,Y为淡黄色固体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定正确的是( )
短周期元素A、B、C、D的原子序数依次增大,B和D同主族;X、Y、N分别是由以上四种元素中的两种组成的化合物,Z是由以上三种元素组成的化合物;若X与Y摩尔质量相同,Y为淡黄色固体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定正确的是( )
 短周期元素A、B、C、D的原子序数依次增大,B和D同主族;X、Y、N分别是由以上四种元素中的两种组成的化合物,Z是由以上三种元素组成的化合物;若X与Y摩尔质量相同,Y为淡黄色固体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定正确的是( )
短周期元素A、B、C、D的原子序数依次增大,B和D同主族;X、Y、N分别是由以上四种元素中的两种组成的化合物,Z是由以上三种元素组成的化合物;若X与Y摩尔质量相同,Y为淡黄色固体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定正确的是( )| A. | 相对分子质量M>N,沸点N<M | B. | .简单离子半径:D>B>C>A | ||
| C. | Z为Na2CO3 | D. | .图中有两个氧化还原反应 |
16.光纤通讯是光导纤维传送信号的一种通讯手段,合成光导纤维及氮化硅(一种无机涂层)的工艺流程如图:
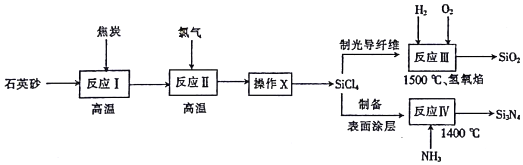
回答下列问题:
(1)反应I的化学方程式为2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,其中还原剂为C(填化学式),该反应涉及的副反应可能有(碳不足)C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑和(碳足量)3C+SiO2$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑.
(2)经反应Ⅱ所得的四氯化硅粗品中所含的物质如表:
图中“操作X”的名称为精馏(或蒸馏或分馏);PCl3的电子式为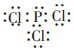 .
.
(3)已知反应Ⅳ的化学方程式为3SiCl4+4NH3$\frac{\underline{\;1400℃\;}}{\;}$Si3N4+12HCl,则反应Ⅲ和Ⅳ中尾气的用途为制取盐酸.若向一2L恒容密闭容器中投入1mol SiC14和1mol NH3,6min后反应完全,则0~6min内,HCl的平均反应速率为0.25 mol•L-l•min-l.

回答下列问题:
(1)反应I的化学方程式为2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,其中还原剂为C(填化学式),该反应涉及的副反应可能有(碳不足)C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑和(碳足量)3C+SiO2$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑.
(2)经反应Ⅱ所得的四氯化硅粗品中所含的物质如表:
| 组分名称 | SiCl4 | SiHCl3 | SiH2Cl2 | HCl | BCl3 | PCl3 |
| 质量分数 | 0.545 | 0.405 | 0.0462 | 0.0003 | 0.00193 | 0.00157 |
| 沸点/℃ | 57.6 | 31.8 | 8.2 | -85 | 12.5 | 75.5 |
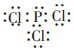 .
.(3)已知反应Ⅳ的化学方程式为3SiCl4+4NH3$\frac{\underline{\;1400℃\;}}{\;}$Si3N4+12HCl,则反应Ⅲ和Ⅳ中尾气的用途为制取盐酸.若向一2L恒容密闭容器中投入1mol SiC14和1mol NH3,6min后反应完全,则0~6min内,HCl的平均反应速率为0.25 mol•L-l•min-l.
15.有机物M是一种香料的合成原料,其结构简式如图所示.下列有关M的说法正确的是( )
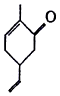

| A. | 可以发生氧化反应 | B. | 分子式为C9H10O | ||
| C. | 分子中所有原子都处于同一平面上 | D. | 能使溴的四氯化碳溶液褪色 |
14.镁锰干电池中反应的化学方程式为Mg+2MnO2+H2O═Mg (OH)2+Mn2O3.下列说法正确的是( )
| A. | 负极的电极反应式为Mg+2OH-+2e-═Mg(OH)2 | |
| B. | 电池放电时,OH-向负极移动 | |
| C. | 电解质溶液可以是稀H2SO4 | |
| D. | 正极的电极反应式为2MnO2+H2O+2e-═Mn2O3+2OH- |
13.设NA为阿伏加德罗常数的数值.下列叙述正确的是( )
| A. | 标准状况下,224 mL水中含有的电子数为0.1NA | |
| B. | 44 g由N2O和CO2组成的混合气体中含有的原子数为3NA | |
| C. | 将20 mL 0.5 mol•L-1 FeCl3溶液煮沸,所得胶粒数目为0.01NA | |
| D. | 在反应:KClO3+6HCl═KCl+3Cl2+3H2O中,每生成3mol Cl2,转移的电子数为6NA |
12.战国所著《周礼》中记载沿海古人“谋饼烧蛎房成灰”(“蛎房”即牡蛎壳),并把这种灰称为“蜃”.蔡伦改进的造纸术,第-步沤浸树皮脱胶的碱液可用“蜃”溶于水制得.“蜃”的主要成分是( )
0 162340 162348 162354 162358 162364 162366 162370 162376 162378 162384 162390 162394 162396 162400 162406 162408 162414 162418 162420 162424 162426 162430 162432 162434 162435 162436 162438 162439 162440 162442 162444 162448 162450 162454 162456 162460 162466 162468 162474 162478 162480 162484 162490 162496 162498 162504 162508 162510 162516 162520 162526 162534 203614
| A. | CaO | B. | Ca(OH)2 | C. | SiO2 | D. | Al2O3 |