19.某干电池在使用过程中发生的主要反应可用下列化学方程式表示:Zn+2MnO2+2NH4Cl(aq)═2MnO(OH)(s)+[Zn(NH3)2]Cl2(aq),其正极反应式是( )
| A. | 2MnO2+2NH4++2e-═2MnO(OH)+2NH3 | B. | Zn-2e-═Zn2+ | ||
| C. | [Zn(NH3)2]2++2e-═Zn+2NH3 | D. | Mn4++e-═Mn3+ |
18.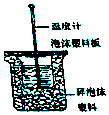 Ⅰ.50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题.
Ⅰ.50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题.
(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒.
(2)烧杯间填满碎纸条的作用是减少实验过程中的热量损失.
(3)实验中改用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比较,所放出的热量不相等(填“相等”或“不相等”),但中和热应相等(填“相等”或“不相等”).
(4)记录的实验数据如表:
已知:Q=cm(t2-t1),反应后溶液的比热容C为4.18KJ•℃-1•Kg-1,各物质的密度均为1g•cm-3.根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l)△H=-56.8kJ•mol-1
过氧化氢是重要的氧化剂,也可作还原剂,它的水溶液称为双氧水,常用于消毒、杀菌、漂白等.某化学研究性学习小组取一定量的市售过氧化氢溶液测定其中H2O2的含量,并探究它的有关性质.
Ⅱ.测定市售过氧化氢溶液中H2O2的质量分数
(1)量取10.00mL密度为ρ g/mL的市售过氧化氢溶液,应选用酸式滴定管(填“酸式滴定管”或“碱式滴定管”);
(2)将上述溶液配制成250.00mL,配制过程需用到的玻璃仪器是烧杯、玻璃棒、250 mL容量瓶、胶头滴管(填名称);
(3)取25.00mL(2)中的溶液于锥形瓶中,用稀H2SO4酸化,并加适量蒸馏水稀释,用高锰酸钾标准液滴定.
①完成反应的离子方程式:
2MnO4-+5H2O2+6H+═2Mn2++8H2O+5O2↑
②重复滴定三次,平均消耗C mol/L KMnO4标准液V mL,则原过氧化氢溶液中H2O2的质量分数为$\frac{17CV}{200ρ}$.
 Ⅰ.50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题.
Ⅰ.50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题.(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒.
(2)烧杯间填满碎纸条的作用是减少实验过程中的热量损失.
(3)实验中改用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比较,所放出的热量不相等(填“相等”或“不相等”),但中和热应相等(填“相等”或“不相等”).
(4)记录的实验数据如表:
| 实验用品 | 溶液温度 | |||
| t1 | t2 | |||
| ① | 50ml0.55mol/LNaOH | 50ml0.5mol/LHCl | 20℃ | 23.3℃ |
| ② | 50ml0.55mol/LNaOH | 50ml0.5mol/LHCl | 20℃ | 23.5℃ |
| 50ml0.55mol/LNaOH | 50ml0.5mol/LHCl | 20℃ | 21.5℃ | |
过氧化氢是重要的氧化剂,也可作还原剂,它的水溶液称为双氧水,常用于消毒、杀菌、漂白等.某化学研究性学习小组取一定量的市售过氧化氢溶液测定其中H2O2的含量,并探究它的有关性质.
Ⅱ.测定市售过氧化氢溶液中H2O2的质量分数
(1)量取10.00mL密度为ρ g/mL的市售过氧化氢溶液,应选用酸式滴定管(填“酸式滴定管”或“碱式滴定管”);
(2)将上述溶液配制成250.00mL,配制过程需用到的玻璃仪器是烧杯、玻璃棒、250 mL容量瓶、胶头滴管(填名称);
(3)取25.00mL(2)中的溶液于锥形瓶中,用稀H2SO4酸化,并加适量蒸馏水稀释,用高锰酸钾标准液滴定.
①完成反应的离子方程式:
2MnO4-+5H2O2+6H+═2Mn2++8H2O+5O2↑
②重复滴定三次,平均消耗C mol/L KMnO4标准液V mL,则原过氧化氢溶液中H2O2的质量分数为$\frac{17CV}{200ρ}$.
17.二氧化硫常温下为无色有刺激性气味的有毒气体,易液化,易溶于水.某同学设计如下实验方案,对二氧化硫的化学性质进行探究,装置如图所示.请回答下列问题:

(1)反应结束时烧瓶中Cu由剩余,某同学认为H2SO4也有剩余,他设计了下列实验方案来测定剩余H2SO4的量.经冷却,定量稀释后进行下列实验,能达到的目的是bc(填序号)
a.用酸碱中和滴定法测定 b.与足量Zn反应,测量生成H2的体积
c.用pH计测溶液PH值 d.与足量BaCl2溶液反应,称量生成沉淀的质量
(2)装置B的作用是防倒吸(或安全瓶),设计装置C的目的是验证SO2的还原性,装置C中发生反应的离子方程式SO2+Br2+2H2O=4H++SO42-+2Br-,装置D中NaOH全部转化为NaHSO3的标志是溶液由红色变为无色
(3)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能情况:
I.HSO3-与ClO-刚好反应完;Ⅱ.NaClO不足;Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请你完成表:(已知酸性:H2SO3>H2CO3>HClO)
(4)设计简单实验证明:室温下HSO3-的电离平衡常数Ka与水解平衡常数Kb的相对大小常温下,用pH试纸(或pH计)测定NaHSO3溶液的pH,若pH<7,则Ka>Kb,若pH>7,则Ka<Kb.

(1)反应结束时烧瓶中Cu由剩余,某同学认为H2SO4也有剩余,他设计了下列实验方案来测定剩余H2SO4的量.经冷却,定量稀释后进行下列实验,能达到的目的是bc(填序号)
a.用酸碱中和滴定法测定 b.与足量Zn反应,测量生成H2的体积
c.用pH计测溶液PH值 d.与足量BaCl2溶液反应,称量生成沉淀的质量
(2)装置B的作用是防倒吸(或安全瓶),设计装置C的目的是验证SO2的还原性,装置C中发生反应的离子方程式SO2+Br2+2H2O=4H++SO42-+2Br-,装置D中NaOH全部转化为NaHSO3的标志是溶液由红色变为无色
(3)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能情况:
I.HSO3-与ClO-刚好反应完;Ⅱ.NaClO不足;Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请你完成表:(已知酸性:H2SO3>H2CO3>HClO)
| 实验序号 | 实验操作 | 现象 | 反应的可能情况 |
| ① | 加入几小块CaCO3固体 | 有气泡产生 | |
| ② | 滴加少量淀粉KI溶液,振荡 | Ⅲ | |
| ③ | 滴加少量溴水,振荡 | Ⅱ | |
| ④ | 滴入加少量酸性KMnO4溶液,振荡 | 溶液为紫色 |
16.取浓度相等的NaOH和HCl溶液,以3:2体积比相混和,所得溶液中的c(OH-)=0.01mol/L,则原溶液的浓度为(溶液体积的变化忽略不计)( )
| A. | 0.01 mol/L | B. | 0.017 mol/L | C. | 0.05 mol/L | D. | 0.50 mol/L |
13.下列说法正确的是( )
| A. | “雨后彩虹”是与胶体、光学等知识有关的自然现象 | |
| B. | “百炼成钢”主要发生了物理变化 | |
| C. | “返青粽叶”指的是添加胆矾(CuSO4•5H2O)后的粽叶青绿新鲜,长期食用有害健康,其中胆矾是混合物 | |
| D. | “明矾净水”与漂白粉用于自来水消毒的原理相同 |
12.下列说法不正确的是( )
| A. | Na2O2、HClO、SO2等物质都具有漂白作用 | |
| B. | 纯碱和小苏打都是碱 | |
| C. | 所有的置换反应都是氧化还原反应,而所有的复分解反应都是非氧化还原反应 | |
| D. | 非金属氧化物不一定是酸性氧化物,有些金属氧化物也能与强碱反应 |
11.在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6gX与Y完全反应后,生成4.4gR,则 在此反应中,Y与R的化学式量之比为( )
| A. | 32:18 | B. | 16:11 | C. | 8:11 | D. | 16:9 |
10.下列说法正确的是( )
0 162259 162267 162273 162277 162283 162285 162289 162295 162297 162303 162309 162313 162315 162319 162325 162327 162333 162337 162339 162343 162345 162349 162351 162353 162354 162355 162357 162358 162359 162361 162363 162367 162369 162373 162375 162379 162385 162387 162393 162397 162399 162403 162409 162415 162417 162423 162427 162429 162435 162439 162445 162453 203614
| A. | 同物质的量的浓度的三种溶液:Na2SO4、MgSO4、Al2(SO4)3,其体积比为3:2:1,则SO42-浓度之比为1:1:3 | |
| B. | 将10 mL 1 mol/L H2SO4稀释成0.1 mol/L的H2SO4,可向该溶液中加入100 mL水 | |
| C. | 将1 mol/L的NaCl溶液和0.5 mol/L的BaCl2溶液等体积混合后,不考虑溶液体积变化c(Cl-)=0.75 mol/L | |
| D. | 50 g浓度为c mol/L,密度为ρ g•cm-3的氨水(ρ<1)中加入一定量的水(ρ=1g•cm-3)稀释成0.5c mol/L,则加入水的体积应小于50 mL |