题目内容
11.在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6gX与Y完全反应后,生成4.4gR,则 在此反应中,Y与R的化学式量之比为( )| A. | 32:18 | B. | 16:11 | C. | 8:11 | D. | 16:9 |
分析 化学反应遵循质量守恒定律,且参加反应的质量之比等于式量之比,以此来解答.
解答 解:R和M的摩尔质量之比为22:9,生成4.4gR时,设生成M为xg,则
$\frac{4.4g}{xg}=\frac{22}{9×2}$,解得x=3.6g,
由质量守恒可知,Y的质量为4.4g+3.6g-1.6g=6.4g,
X+2Y=R+2M
2Y R
6.4g 4.4g
$\frac{2Y}{R}=\frac{6.4}{4.4}$,可知Y:R=8:11,
Y与R的化学式量之比为8:11.
故选C.
点评 本题考查化学反应的计算,为高频考点,把握质量守恒定律、质量关系为解答的关键,侧重分析与计算能力的考查,注意守恒法应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.在常温下,下列各组溶液的c(H+)一定等于1×10-7mol/L的是( )
| A. | 将pH=5的CH3COOH溶液稀释100倍 | |
| B. | 0.05mol/L H2SO4与0.10mol/L NaOH溶液以等体积混合 | |
| C. | pH=2的盐酸和pH=12的氨水两种溶液以等体积混合 | |
| D. | pH=1的H2SO4与0.10mol/L 的Ba(OH)2溶液以等体积混合 |
19.下列关于反应热的说法正确的是( )
| A. | 已知C(石墨,s)=C(金刚石,s)△H>0,说明金刚石比石墨稳定 | |
| B. | 已知H+(aq)+OH-(aq)=H2O(l)△H=-57.4kJ/mol,则含20.0gNaOH的稀溶液与稀醋酸完全中和,放出热量小于28.7kJ | |
| C. | 已知甲烷的燃烧热为890.3kJ/mol,则表示甲烷燃烧热的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ/mol | |
| D. | 将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ/mol |
6.下列因果关系叙述正确的是( )
| A. | 浓硝酸中的HNO3见光会分解,因此有时在实验室看到的浓硝酸呈黄色 | |
| B. | SO2具有漂白性,因此可使溴水褪色 | |
| C. | Na的金属性比Cu强,因此可用Na与CuSO4溶液反应制取Cu | |
| D. | Fe在Cl2中燃烧生成FeCl3,因此在与其他非金属反应的产物中Fe也显+3价 |
16.取浓度相等的NaOH和HCl溶液,以3:2体积比相混和,所得溶液中的c(OH-)=0.01mol/L,则原溶液的浓度为(溶液体积的变化忽略不计)( )
| A. | 0.01 mol/L | B. | 0.017 mol/L | C. | 0.05 mol/L | D. | 0.50 mol/L |
1.下列各组物质不属于同系物的是( )
| A. | 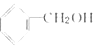 和 和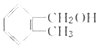 | B. | HOCH2-CH2OH和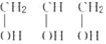 | C. | CH3CH2OH和 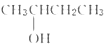 | D. | HOCH2CH2OH和 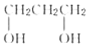 |

 ;CCH3OH;D
;CCH3OH;D ;ECH3COOH.
;ECH3COOH.