1.下列关于物质的量的叙述中,错误的是( )
| A. | 1mol任何粒子的粒子数叫做阿伏伽德罗常数 | |
| B. | 1molH2O中含有3mol原子 | |
| C. | 1molH2O中含有2 mol氢和1mol氧 | |
| D. | 0.012Kg12C中约含有6.02×1023个碳原子 |
20.下列有关气体摩尔体积的描述中正确的是( )
| A. | 单位物质的量的气体所占的体积就是气体摩尔体积 | |
| B. | 通常状况(室温、101kP)下,气体摩尔体积约为22.4L/mol | |
| C. | 标准状况(0℃、101kP)下,气体摩尔体积约为22.4 L | |
| D. | 标准状况(0℃、101kP)下,1 mol H2O的体积是22.4 L |
18.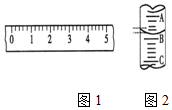 (1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在表中填空,表示称量过程,并在如图1所示的游码尺上画出游码的位置(画“|”表示).
(1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在表中填空,表示称量过程,并在如图1所示的游码尺上画出游码的位置(画“|”表示).
(2)图2表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量筒中的液体的体积是3.2mL.
(3)用18mol•L-1的硫酸溶液配制0.5mol•L-1的硫酸溶液250mL所需的玻璃仪器为10mL量筒,250ml容量瓶,烧杯,玻璃棒,胶头滴管.
 (1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在表中填空,表示称量过程,并在如图1所示的游码尺上画出游码的位置(画“|”表示).
(1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在表中填空,表示称量过程,并在如图1所示的游码尺上画出游码的位置(画“|”表示).| 砝码质量/g | 50 | 20 | 20 | 10 | 5 |
| 取用砝码情况 |
(3)用18mol•L-1的硫酸溶液配制0.5mol•L-1的硫酸溶液250mL所需的玻璃仪器为10mL量筒,250ml容量瓶,烧杯,玻璃棒,胶头滴管.
16.交通警察使用的“司机酒后驾车检测器”是应用氧化还原反应原理制成的,其反应的化学方程式为(Cr为铬元素):4CrO3+C2H5OH+6H2SO4=2Cr2(SO4)3+2CO2↑+9H2O CrO3是一种红色固体,它在酸性条件下与酒精蒸气反应生成蓝绿色的硫酸铬,根据颜色变化来判断司机是否饮酒.下列说法不正确的是( )
| A. | CrO3是氧化剂 | |
| B. | 酒精是还原剂 | |
| C. | 当2mol CrO3被还原时,有3mol电子发生转移 | |
| D. | 当0.02mol酒精参与反应时,生成的CO2在标准状况下的体积为0.896L |
14.用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
0 162191 162199 162205 162209 162215 162217 162221 162227 162229 162235 162241 162245 162247 162251 162257 162259 162265 162269 162271 162275 162277 162281 162283 162285 162286 162287 162289 162290 162291 162293 162295 162299 162301 162305 162307 162311 162317 162319 162325 162329 162331 162335 162341 162347 162349 162355 162359 162361 162367 162371 162377 162385 203614
| A. | 7.8 g Na2O2中含有的阴离子数为0.2NA | |
| B. | 铜与浓硫酸反应中,当转移的电子数为0.2NA时,生成的SO2为2.24 L | |
| C. | 1 mol•L-1的NH4Cl溶液中的NH4+的数目小于NA | |
| D. | 由NO2、O2组成的混合物中共有NA个分子,其中的氧原子数目为2NA |
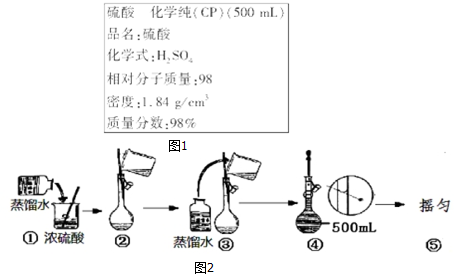
 为探究测定中和热的实验,小明利用50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液,在如图所示的装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热(中和热数值为57.3kJ/mol).
为探究测定中和热的实验,小明利用50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液,在如图所示的装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热(中和热数值为57.3kJ/mol).