3.下列实验操作完全正确的是( )
| 实验 | 操作 | |
| A | 用苯萃取碘水中碘后,静置后取出有机层 | 先从分液漏斗下端管口放出下层液体,关闭活塞,换一个接收容器,再继续从分液漏斗下端管口放出上层液体 |
| B | 配制500mL2mol/L的氯化铵溶液 | 用托盘天平称取53.5g氯化铵晶体放入500mL容量瓶,加少量水,振荡后再加水至刻度线 |
| C | 测定氯水的pH | 用玻璃棒蘸取少量溶液滴于pH试纸中央,片刻后与标准比色卡对照 |
| D | 用标准盐酸滴定未知浓度的NaOH溶液(含酚酞) | 左手控制酸式滴定管活塞使液体滴下,右手不断振荡锥形瓶,眼睛要始终观察锥形瓶中溶液颜色变化 |
| A. | A | B. | B | C. | C | D. | D |
2.下列热化学方程式中△H代表燃烧热(25℃,101kPa)的是( )
| A. | CH4(g)+$\frac{3}{2}$O2(g)═2H2O(l)+CO(g)△H1 | B. | 2CO(g)+O2(g)═2CO2(g)△H2 | ||
| C. | S(s)+$\frac{3}{2}$O2(g)═SO3(s)△H3 | D. | C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l)△H4 |
1.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,11.2LSO3所含的分子数为0.5NA | |
| B. | 12g石墨和C60的混合物中质子总数一定为6NA | |
| C. | 25℃时,1L mol•L-1FeCl3溶液中含有0.1NA个Fe(OH)3胶体粒子 | |
| D. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
20.水是生命之源,下列有关各种“水”的说法中正确的是( )
| A. | 双氧水被称为绿色氧化剂,是因为其还原产物为O2,对环境没有污染 | |
| B. | 王水是浓盐酸和浓硝酸按体积比1:3配成的混合物,可以溶解Au、Pt | |
| C. | 新制备的氯水中存在七种粒子 | |
| D. | 氨水能导电,说明氨气是电解质 |
19.将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO).向反应后的溶液中加入 3mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g.下列叙述不正确的是( )
| A. | 当生成的沉淀量达到最大时,消耗NaOH 溶液的体积V≥100 mL | |
| B. | 当金属全部溶解时,参加反应的硝酸的物质的量一定是 0.4 mol | |
| C. | 参加反应的金属的总质量 9.6g>m>3.6g | |
| D. | 当金属全部溶解时收集到 NO气体的体积一定为2.24L |
18.将 3.84g Cu投入一定量的浓HNO3中,铜完全溶解,生成气体的颜色越来越淡,共收集到1134mL 气体(标准状况).再把盛有此气体的容器倒扣在水中,容器内液面上升,再通入标准状况下一定体积的氧气,恰好使气体完全溶于水中,则通入O2的体积是( )
| A. | 672 mL | B. | 168 mL | C. | 504 mL | D. | 224 mL |
15.下列做法不存在安全隐患或不会导致实验失败的是( )
0 162189 162197 162203 162207 162213 162215 162219 162225 162227 162233 162239 162243 162245 162249 162255 162257 162263 162267 162269 162273 162275 162279 162281 162283 162284 162285 162287 162288 162289 162291 162293 162297 162299 162303 162305 162309 162315 162317 162323 162327 162329 162333 162339 162345 162347 162353 162357 162359 162365 162369 162375 162383 203614
| A. | 氢气还原氧化铜当反应完成后,先停止通氢气再停止加热 | |
| B. | 将饱和FeCl3溶液加热煮沸来制备Fe(OH3胶体) | |
| C. | 工业制备HCl气体时将氢气和氯气的混合气体在光照条件下反应 | |
| D. | 浓硫酸稀释时如图操作 |
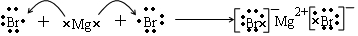 .
.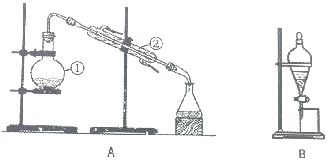 如图装置是实验室中物质分离的常用装置,请回答下列问题.
如图装置是实验室中物质分离的常用装置,请回答下列问题.