19. 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
(1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化.
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是D.
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
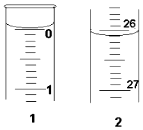
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,所用盐酸
溶液的体积为26.10mL.
(4)某学生根据三次实验分别记录有关数据如表:
请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度:C(NaOH)=0.1044mol/L(保留小数点后4位).
 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:(1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化.
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是D.
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,所用盐酸
溶液的体积为26.10mL.
(4)某学生根据三次实验分别记录有关数据如表:
| 滴定 次数 | 待测氢氧化钠溶 液的体积/mL | 0.1000mol•L+1盐酸的体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 0.00 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 |
| 第三次 | 25.00 | 0.22 | 26.31 |
16.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如表数据(盐酸的物质的量浓度相同):
则下列分析推理中正确的是( )
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
| A. | 根据表中数据不能计算出混合物中NaHCO3的质量 | |
| B. | 根据表中数据可救出盐酸的物质的量浓度为3mol•L-1 | |
| C. | 加入混合物9.2 g时恰好与盐酸完全反应 | |
| D. | 15.7 g混合物恰好与盐酸完全反应 |
14.表是前20号元素中的部分元素的一些数据:
试回答下列问题:
(1)以上10种元素电负性最大的是O(填元素符号).比元素B原子序数大7的元素在元素周期表中的位置:第4周期,第VIII族,其基态原子的核外电子排布式是1s22s22p63s23p63d64s2(或[Ar]3d64s2).
(2)H、I、J三种元素对应单质的熔点依次升高的顺序是(用单质的具体化学式排序)N2<Na<Si.
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子.其分子中共形成7个σ键,1个π键.
(4)I与氢元素形成的10电子分子X的空间构型为三角锥形;将X溶于水后的溶液滴入到CuSO4溶液中至过量,得到的络离子的化学式为[Cu(NH3)4]2+,其中X与Cu2+之间以配位键结合.
(5)如图1是I元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:
a.HNO3是极性分子,易溶于极性的水中
b.HNO3分子中的-OH易与水分子之间形成氢键
(6)如图2是J和E组成的晶体结构,则每个与J周围最近J原子数目为12,若晶胞边长为a cm,则晶体的密度为(用含a、NA的代数式表示)$\frac{4×M(SiC)}{{a}^{3}{N}_{A}}$或$\frac{4×40}{{a}^{3}{N}_{A}}$或$\frac{160}{{a}^{3}{N}_{A}}$(g/mL)

0 162172 162180 162186 162190 162196 162198 162202 162208 162210 162216 162222 162226 162228 162232 162238 162240 162246 162250 162252 162256 162258 162262 162264 162266 162267 162268 162270 162271 162272 162274 162276 162280 162282 162286 162288 162292 162298 162300 162306 162310 162312 162316 162322 162328 162330 162336 162340 162342 162348 162352 162358 162366 203614
| A | B | C | D | E | F | G | H | I | J | |
| 原子半径(10-10 m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
(1)以上10种元素电负性最大的是O(填元素符号).比元素B原子序数大7的元素在元素周期表中的位置:第4周期,第VIII族,其基态原子的核外电子排布式是1s22s22p63s23p63d64s2(或[Ar]3d64s2).
(2)H、I、J三种元素对应单质的熔点依次升高的顺序是(用单质的具体化学式排序)N2<Na<Si.
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子.其分子中共形成7个σ键,1个π键.
(4)I与氢元素形成的10电子分子X的空间构型为三角锥形;将X溶于水后的溶液滴入到CuSO4溶液中至过量,得到的络离子的化学式为[Cu(NH3)4]2+,其中X与Cu2+之间以配位键结合.
(5)如图1是I元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:
a.HNO3是极性分子,易溶于极性的水中
b.HNO3分子中的-OH易与水分子之间形成氢键
(6)如图2是J和E组成的晶体结构,则每个与J周围最近J原子数目为12,若晶胞边长为a cm,则晶体的密度为(用含a、NA的代数式表示)$\frac{4×M(SiC)}{{a}^{3}{N}_{A}}$或$\frac{4×40}{{a}^{3}{N}_{A}}$或$\frac{160}{{a}^{3}{N}_{A}}$(g/mL)

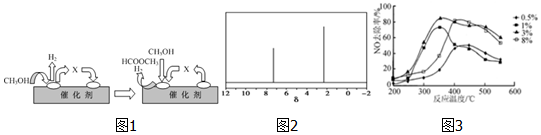
 CH3OH.
CH3OH. .
.