7.NA表示阿伏伽德罗常数,下列说法中正确的是( )
| A. | 标况下,22.4升的H2O含有的水分子数为NA | |
| B. | 标况下,11.2升CCl4中含有的Cl原子数为2NA | |
| C. | 17克NH3中含有的电子总数为10NA | |
| D. | 0.5mol/L的H2SO4溶液中含有的H+数为NA |
5.硫是一种生命元素,组成某些蛋白质时离不开它.SO2是硫的一种重要氧化物,为探究SO2的性质,某化学兴趣小组的同学设计了如下系列实验:
(1)为验证SO2具有还原性.将SO2气体通入溴水中,溴水褪色.写出反应的化学方程式SO2+Br2+2H2OH2SO4+2HBr.
(2)已知与SO2Na2O2的反应为进一步探究Na2O2与SO2的反应,用如图所示装置进行实验.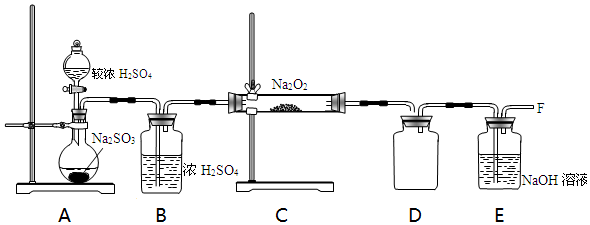
①写出A中反应的化学方程式H2SO4+Na2SO3 =Na2SO4+SO2↑+H2O.
②B装置的作用是干燥吸水.
③在F处检验到有O2生成,据此甲同学认为Na2O2与SO2发生了反应,反应的化学方程式为2Na2O2+2SO2=2Na2SO3+O2.
④乙同学认为Na2O2与SO2反应除生成Na2SO3和O2外,还有Na2SO4生成,为检验是否有Na2SO4生成,他们设计了如下实验方案.
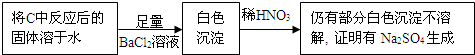
上述方案(“合理”或“不合理”)不合理,简要说明理由稀硝酸能将亚硫酸钡氧化为硫酸钡,如果反应后的固体中还残留Na2O2,它溶于水也能将亚硫酸根氧化成硫酸根.
⑤E装置中溶液呈碱性,为检验吸收液中其他阴离子,完成下列实验方案.
(1)为验证SO2具有还原性.将SO2气体通入溴水中,溴水褪色.写出反应的化学方程式SO2+Br2+2H2OH2SO4+2HBr.
(2)已知与SO2Na2O2的反应为进一步探究Na2O2与SO2的反应,用如图所示装置进行实验.

①写出A中反应的化学方程式H2SO4+Na2SO3 =Na2SO4+SO2↑+H2O.
②B装置的作用是干燥吸水.
③在F处检验到有O2生成,据此甲同学认为Na2O2与SO2发生了反应,反应的化学方程式为2Na2O2+2SO2=2Na2SO3+O2.
④乙同学认为Na2O2与SO2反应除生成Na2SO3和O2外,还有Na2SO4生成,为检验是否有Na2SO4生成,他们设计了如下实验方案.

上述方案(“合理”或“不合理”)不合理,简要说明理由稀硝酸能将亚硫酸钡氧化为硫酸钡,如果反应后的固体中还残留Na2O2,它溶于水也能将亚硫酸根氧化成硫酸根.
⑤E装置中溶液呈碱性,为检验吸收液中其他阴离子,完成下列实验方案.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量吸收液于试管中滴加BaCl2溶液至过量 | 白色浑浊 | 吸收液中存在SO32-和SO42- |
| 取步骤I中白色沉淀于试管中,加入过量的稀盐酸 | 固体部分溶解,产生气泡 |
4.淀粉碘化钾试纸或溶液是实验室中的常用试剂.某中学化学兴趣小组用淀粉碘化钾溶液进行如下实验:
针对实验中出现的一些反常现象,需要设计实验进行探究:
(1)提出问题:
①实验1、实验2现象不同,猜想原因最有可能是二氧化碳参与氧气与碘离子的氧化反应;要证明该猜想是正确的,可以将用淀粉碘化钾溶液湿润的滤纸置于混有二氧化碳的氧气中,若滤纸变蓝,证明猜想正确.此过程中发生反应的离子方程式是2CO2+O2+4I-=2CO32-+2I2.
②实验3中溶液蓝色褪去的原因可能是
猜想一:氯气将碘单质氧化
猜想二:氯气将淀粉氧化
猜想三:氯气将碘单质和淀粉都氧化
(2)设计探究方案
要证明实验3褪色的原因是猜想一所致,可向褪色后的溶液中滴加少量碘水,若溶液变蓝色,即可证明.
(3)实验反思
查阅相关材料可知,氯所可将单质碘氧化为HIO3,酸性条件下,IO3-可被SO32-、I-还原为碘单质.其工业废水中的阴离子可能含有IO3-、I-中的一种或两种,要证明其中含有何种阴离子,你设计的实验方案是取废水少许于试管中,依次加入淀粉溶液和稀硫酸溶液,弱溶液变蓝色证明同时含有I-、IO3-离子,弱溶液不变蓝,在滴入KI溶液弱溶液变蓝色则证明含、IO3-离子,弱溶液不变蓝证明只含有I-(写出简单的实验步骤、现象和结论).发生反应的离子方程式是IO3-+5I-+6H+=3I2+3H2O.
| 实验编号 | 1 | 2 | 3 |
| 实验步骤 | 取一小片滤纸用淀粉碘化钾溶液湿润后,放在表面皿上,置于空气中,观察现象 | 取一小片滤纸用淀粉碘化钾溶液湿润后,放在表面皿上,置于氧气中,观察现象 | 取少量淀粉碘化钾溶液置于试管中,通往足量的氯气,观察现象 |
| 实验现象 | 试纸缓慢变蓝 | 试纸不变蓝 | 溶液先变蓝后褪色 |
(1)提出问题:
①实验1、实验2现象不同,猜想原因最有可能是二氧化碳参与氧气与碘离子的氧化反应;要证明该猜想是正确的,可以将用淀粉碘化钾溶液湿润的滤纸置于混有二氧化碳的氧气中,若滤纸变蓝,证明猜想正确.此过程中发生反应的离子方程式是2CO2+O2+4I-=2CO32-+2I2.
②实验3中溶液蓝色褪去的原因可能是
猜想一:氯气将碘单质氧化
猜想二:氯气将淀粉氧化
猜想三:氯气将碘单质和淀粉都氧化
(2)设计探究方案
要证明实验3褪色的原因是猜想一所致,可向褪色后的溶液中滴加少量碘水,若溶液变蓝色,即可证明.
(3)实验反思
查阅相关材料可知,氯所可将单质碘氧化为HIO3,酸性条件下,IO3-可被SO32-、I-还原为碘单质.其工业废水中的阴离子可能含有IO3-、I-中的一种或两种,要证明其中含有何种阴离子,你设计的实验方案是取废水少许于试管中,依次加入淀粉溶液和稀硫酸溶液,弱溶液变蓝色证明同时含有I-、IO3-离子,弱溶液不变蓝,在滴入KI溶液弱溶液变蓝色则证明含、IO3-离子,弱溶液不变蓝证明只含有I-(写出简单的实验步骤、现象和结论).发生反应的离子方程式是IO3-+5I-+6H+=3I2+3H2O.
2.为了探究AgNO3的氧化性,某化学兴趣小组设计了如下实验:将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出.为检验溶液中Fe的氧化产物,将溶液中的Ag+除尽后,进行了如下实验,可选用试剂:KSCN溶液、酸性高锰酸钾溶液、氯水、氢氧化钠溶液、双氧水.
【实验结论】Fe的氧化产物为Fe2+和Fe3+.
0 161975 161983 161989 161993 161999 162001 162005 162011 162013 162019 162025 162029 162031 162035 162041 162043 162049 162053 162055 162059 162061 162065 162067 162069 162070 162071 162073 162074 162075 162077 162079 162083 162085 162089 162091 162095 162101 162103 162109 162113 162115 162119 162125 162131 162133 162139 162143 162145 162151 162155 162161 162169 203614
| 操作 | 现象 | 结论 |
| 取少量除尽Ag+后的溶液于试管中,滴加几滴KSCN溶液,振荡 | 溶液呈血红色 | 存在Fe3+ |
| 取少量除尽Ag+后的溶液于试管中,滴加几滴K3[Fe(CN)6]溶液,振荡 | 产生蓝色沉淀 | 存在Fe2+ |