题目内容
9.该镁铝碱式碳酸盐[Mg6Al2(OH)16CO3•4H2O]可以由MgCl2、NaAlO2、NaOH和Na2CO3反应制备,制备的化学方程式为6MgCl2+2NaAlO2+8NaOH+Na2CO3+8H2O=Mg6Al2(OH)16CO3•4H2O↓+12NaCl.分析 该镁铝碱式碳酸盐(镁铝碱式酸盐Mg6Al2(OH)16CO3•4H2O)可以由MgCl2、NaAlO2、NaOH和Na2CO3反应制备,结合原子守恒配平书写化学方程式.
解答 解:镁铝碱式碳酸盐可以由MgCl2、NaAlO2、NaOH和Na2CO3反应制备,反应的化学方程式为6MgCl2+2NaAlO2+8NaOH+Na2CO3+8H2O=Mg6Al2(OH)16CO3•4H2O↓+12NaCl,
故答案为:6MgCl2+2NaAlO2+8NaOH+Na2CO3+8H2O=Mg6Al2(OH)16CO3•4H2O↓+12NaCl.
点评 本题考查方程式的书写,根据镁铝碱式碳酸盐以及反应物结合原子守恒即可书写,题目难度不大.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
17.由2个 、2个
、2个 、1个
、1个 和1个
和1个 构成的有机分子有(不考虑立体异构)( )
构成的有机分子有(不考虑立体异构)( )
 、2个
、2个 、1个
、1个 和1个
和1个 构成的有机分子有(不考虑立体异构)( )
构成的有机分子有(不考虑立体异构)( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 9种 |
14.A、B两种元素,A的原子序数为a,如果A和B同在第ⅣA族,当B的周期数大于A的周期数时,B的原子序数不可能为( )
| A. | a+2 | B. | a+8 | C. | a+26 | D. | a+18 |
4.淀粉碘化钾试纸或溶液是实验室中的常用试剂.某中学化学兴趣小组用淀粉碘化钾溶液进行如下实验:
针对实验中出现的一些反常现象,需要设计实验进行探究:
(1)提出问题:
①实验1、实验2现象不同,猜想原因最有可能是二氧化碳参与氧气与碘离子的氧化反应;要证明该猜想是正确的,可以将用淀粉碘化钾溶液湿润的滤纸置于混有二氧化碳的氧气中,若滤纸变蓝,证明猜想正确.此过程中发生反应的离子方程式是2CO2+O2+4I-=2CO32-+2I2.
②实验3中溶液蓝色褪去的原因可能是
猜想一:氯气将碘单质氧化
猜想二:氯气将淀粉氧化
猜想三:氯气将碘单质和淀粉都氧化
(2)设计探究方案
要证明实验3褪色的原因是猜想一所致,可向褪色后的溶液中滴加少量碘水,若溶液变蓝色,即可证明.
(3)实验反思
查阅相关材料可知,氯所可将单质碘氧化为HIO3,酸性条件下,IO3-可被SO32-、I-还原为碘单质.其工业废水中的阴离子可能含有IO3-、I-中的一种或两种,要证明其中含有何种阴离子,你设计的实验方案是取废水少许于试管中,依次加入淀粉溶液和稀硫酸溶液,弱溶液变蓝色证明同时含有I-、IO3-离子,弱溶液不变蓝,在滴入KI溶液弱溶液变蓝色则证明含、IO3-离子,弱溶液不变蓝证明只含有I-(写出简单的实验步骤、现象和结论).发生反应的离子方程式是IO3-+5I-+6H+=3I2+3H2O.
| 实验编号 | 1 | 2 | 3 |
| 实验步骤 | 取一小片滤纸用淀粉碘化钾溶液湿润后,放在表面皿上,置于空气中,观察现象 | 取一小片滤纸用淀粉碘化钾溶液湿润后,放在表面皿上,置于氧气中,观察现象 | 取少量淀粉碘化钾溶液置于试管中,通往足量的氯气,观察现象 |
| 实验现象 | 试纸缓慢变蓝 | 试纸不变蓝 | 溶液先变蓝后褪色 |
(1)提出问题:
①实验1、实验2现象不同,猜想原因最有可能是二氧化碳参与氧气与碘离子的氧化反应;要证明该猜想是正确的,可以将用淀粉碘化钾溶液湿润的滤纸置于混有二氧化碳的氧气中,若滤纸变蓝,证明猜想正确.此过程中发生反应的离子方程式是2CO2+O2+4I-=2CO32-+2I2.
②实验3中溶液蓝色褪去的原因可能是
猜想一:氯气将碘单质氧化
猜想二:氯气将淀粉氧化
猜想三:氯气将碘单质和淀粉都氧化
(2)设计探究方案
要证明实验3褪色的原因是猜想一所致,可向褪色后的溶液中滴加少量碘水,若溶液变蓝色,即可证明.
(3)实验反思
查阅相关材料可知,氯所可将单质碘氧化为HIO3,酸性条件下,IO3-可被SO32-、I-还原为碘单质.其工业废水中的阴离子可能含有IO3-、I-中的一种或两种,要证明其中含有何种阴离子,你设计的实验方案是取废水少许于试管中,依次加入淀粉溶液和稀硫酸溶液,弱溶液变蓝色证明同时含有I-、IO3-离子,弱溶液不变蓝,在滴入KI溶液弱溶液变蓝色则证明含、IO3-离子,弱溶液不变蓝证明只含有I-(写出简单的实验步骤、现象和结论).发生反应的离子方程式是IO3-+5I-+6H+=3I2+3H2O.
14.下列有关的判断或表示方法正确的是( )
| A. | 一定条件下,将0.5 mol N2(g)和1.5 mol H2(g)置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H<-38.6 kJ•mol-1 | |
| B. | 中和热的测定实验中需要用的主要玻璃仪器:两个大小相同的烧杯、两个大小相同的量筒、温度计、环形玻璃搅拌棒,也可以用保温杯代替烧杯做有关中和热测定的实验 | |
| C. | 在测定中和热的实验中,至少需要测定并记录的温度是3次 | |
| D. | CO(g)的燃烧热是283.0 kJ•mol-1,则CO2分解的热化学方程式为:2CO2(g)═2CO(g)+O2(g)△H=+283.0 kJ•mol-1 |
1.有混合气体X,它是由NO、H2、CO2组成,通入足量的Na2O2后,变成混合气体Y,将Y用电火花引燃使其充分反应,只得到质量百分数为70%的HNO3溶液,无其他任何气体,则X中各气体的体积之比为( )
| A. | 2:4:7 | B. | 4:2:7 | C. | 7:4:2 | D. | 3:5:8 |
18.已知HI在催化剂作用下分解速率会加快,其能量随反应进程的变化如图所示.下列说法正确的是( )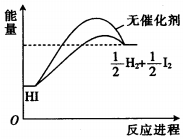

| A. | 加入催化剂,减小了反应的活化能 | |
| B. | 加入催化剂,可提高HI的平衡转化率 | |
| C. | 降低温度,HI的分解速率加快 | |
| D. | 反应物的总能量大于生成物的总能量 |
19.实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
(1)配制100mL 0.10mol/L NaOH标准溶液.
(2)取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定.重复上述滴定操作2~3次,记录数据如表.
①滴定达到终点的现象是最后一滴氢氧化钠溶液加入,溶液由无色恰好变成浅红色,且半分钟内不褪色.此时锥形瓶内溶液的pH为8.2~10.
②根据上述数据,可计算出该盐酸的浓度约为0.11mol/L(保留两位有效数字)
③排去碱式滴定管中气泡的方法应采用操作丙,然后轻轻挤压玻璃球使尖嘴部分充满碱液.

④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有D、F.(多选扣分)
A、滴定终点读数时俯视读数
B、酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C、锥形瓶水洗后未干燥
D、称量前NaOH固体中混有Na2CO3固体
E、配制好的NaOH标准溶液保存不当,部分与空气中的CO2反应生成了Na2CO3
F、碱式滴定管尖嘴部分有气泡,滴定后消失.
(1)配制100mL 0.10mol/L NaOH标准溶液.
(2)取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定.重复上述滴定操作2~3次,记录数据如表.
| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
②根据上述数据,可计算出该盐酸的浓度约为0.11mol/L(保留两位有效数字)
③排去碱式滴定管中气泡的方法应采用操作丙,然后轻轻挤压玻璃球使尖嘴部分充满碱液.

④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有D、F.(多选扣分)
A、滴定终点读数时俯视读数
B、酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C、锥形瓶水洗后未干燥
D、称量前NaOH固体中混有Na2CO3固体
E、配制好的NaOH标准溶液保存不当,部分与空气中的CO2反应生成了Na2CO3
F、碱式滴定管尖嘴部分有气泡,滴定后消失.