5.X、Y、Z、W均为短周期主族元素,原子序数依次增加,Z是活泼金属元素,Y的最常用单质与Z的单质在适当条件下可按物质的量之比1:4或1:2的比例恰好反应生成Q或M,X、W能形成强含氧酸.下列说法错误的是( )
| A. | 简单离子半径:Z<Y<X<W | |
| B. | 气态简单氢化物的稳定性:Y<X | |
| C. | Q和M中的阴、阳离子个数比均为1:2,但化学键种类有差异 | |
| D. | Z与W能形成ZW或Z2W型离子化合物 |
1.下列物质在常温下发生水解时,对应的离子方程式正确的是( )
①Na2CO3:CO32-+2H2O?H2O+CO2↑+2OH-
②NH4Cl:NH4++H2O?NH3•H2O+H+
③CuSO4:Cu2++2H2O?Cu(OH)2+2H+
④NaF:F-+H2O═HF+OH-.
0 161839 161847 161853 161857 161863 161865 161869 161875 161877 161883 161889 161893 161895 161899 161905 161907 161913 161917 161919 161923 161925 161929 161931 161933 161934 161935 161937 161938 161939 161941 161943 161947 161949 161953 161955 161959 161965 161967 161973 161977 161979 161983 161989 161995 161997 162003 162007 162009 162015 162019 162025 162033 203614
①Na2CO3:CO32-+2H2O?H2O+CO2↑+2OH-
②NH4Cl:NH4++H2O?NH3•H2O+H+
③CuSO4:Cu2++2H2O?Cu(OH)2+2H+
④NaF:F-+H2O═HF+OH-.
| A. | ①④ | B. | ②③ | C. | ①③ | D. | ②④ |
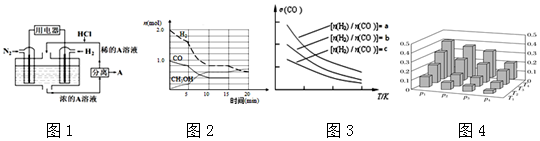
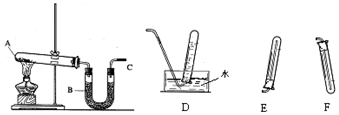
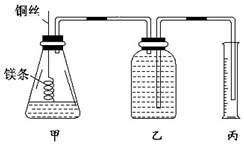 某研究性学习小组欲测定室温下(25℃、101 kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:
某研究性学习小组欲测定室温下(25℃、101 kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示: