题目内容
4.四种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重复:NH4+、Ba2+、Na+、H+、SO42-、NO3-、OH-、HCO3-.将这四种溶液分别标记为A、B、C、D,进行如下实验:①B溶液滴入另外三种溶液中,均能发生化学反应;
②C和D反应生成的气体能被B吸收,吸收时溶液中会出现浑浊,C属于盐类.
试回答下列问题:
(1)B的化学式是Ba(OH)2,判断理由是上述离子之间能产生的气体只有CO2、NH3,遇气体产生沉淀只有Ba(OH)2.
(2)写出其余几种物质的化学式:ANH4NO3,CNaHCO3,DH2SO4.
(3)写出A与B反应的离子方程式NH4++OH-=NH3.H2O.
分析 题给离子中只有H+与HCO3-、OH-与NH4+能反应生成气体,Ba2+、SO42-不能共存,H+与OH-、HCO3-不能共存,由①B溶液滴入另外三种溶液中,均能发生化学反应;
②C和D反应生成的气体能被B吸收,吸收时溶液中会出现浑浊,C属于盐类,产生的气体应为二氧化碳,能被B吸收,说明B是一种碱,生成沉淀为碳酸钡,可知C为NaHCO3,D为H2SO4,B为Ba(OH)2,A为NH4NO3,以此解答该题.
解答 解:(1)由上述分析可知B为Ba(OH)2,因上述离子之间能产生的气体只有CO2、NH3,遇气体产生沉淀只有Ba(OH)2,
故答案为:Ba(OH)2;上述离子之间能产生的气体只有CO2、NH3,遇气体产生沉淀只有Ba(OH)2;
(2)由上述分析可知,A、C、D分别为NH4NO3、NaHCO3、H2SO4,
故答案为:NH4NO3; NaHCO3; H2SO4;
(3)A与B反应的离子方程式为NH4++OH-=NH3.H2O,
故答案为:NH4++OH-=NH3.H2O.
点评 本题考查无机物的推断,为高频考点,把握离子之间的反应、B吸收气体生成沉淀为解答的关键,侧重分析与推断能力的考查,注意沉淀为碳酸钡为推断的突破口,题目难度中等.

练习册系列答案
相关题目
14.下列各组离子,在指定环境中一定能大量共存的是( )
| A. | pH=7的溶液中:Al3+、K+、SO42-、HCO3- | |
| B. | FeCl2溶液中:SO42-、H+、MnO4-、Na+ | |
| C. | 水电离的c (H+)=1×10-13 mol•L-1:S2-、SO32-、S2O32-、SO42- | |
| D. | 滴加甲基橙试剂显红色的溶液中:Na+、NH4+、Cl-、NO3- |
15.在恒温恒容的容器中,发生反应:H2(g)+CO(g)?C(s)+H2O(g).初始时加入平均相对分子质量为15的H2、CO混合气,一段时间后测得气体的平均相对分子质量为16,下列说法中不正确的是( )
| A. | 反应前后气体的压强之比为4:3 | |
| B. | 反应前后气体的密度之比为l5:16 | |
| C. | H2与CO的转化率相等,均为50% | |
| D. | 若H2与CO按8:5体积比混合,则反应前后混合气体的平均相对分子质量不变 |
12.环境污染已成为人类杜会面临的重大威胁,各种污染数不胜数.下列名词与环境污染无关的是( )
| A. | 白色垃圾 | B. | 潮汐 | C. | 酸雨 | D. | 光化学烟雾 |
9.在100mL 0.1mol/L NaOH的溶液中,所含NaOH的质量是( )
| A. | 40 g | B. | 4 g | C. | 0.4 g | D. | 0.04 g |
13.下列四种化学操作名称从左到右分别是( )
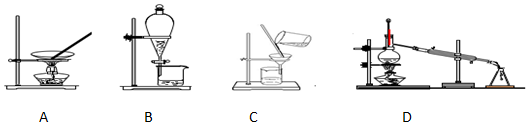

| A. | 蒸发、过滤、分液、蒸馏 | B. | 蒸发、分液、过滤、蒸馏 | ||
| C. | 蒸发、蒸馏、过滤、分液 | D. | 蒸发、蒸馏、分液、过滤 |
14.设NA为阿伏伽德罗常数的值,下列有关草酸(HOOC-COOH)的说法错误的是( )
| A. | 9.0g草酸中共用电子对数目为0.9NA | |
| B. | 9.0g草酸被NaClO氧化生成CO2,转移的电子数为0.2NA | |
| C. | 9.0g草酸溶于水,其中C2O${\;}_{4}^{2-}$和HC2O${\;}_{4}^{-}$的微粒数之和为0.1NA | |
| D. | 9.0g草酸受热完全分解为CO2、CO、H2O,标准状况下测得生成的气体体积为4.48L |
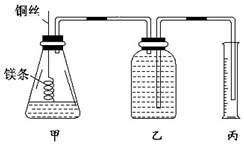 某研究性学习小组欲测定室温下(25℃、101 kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:
某研究性学习小组欲测定室温下(25℃、101 kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示: