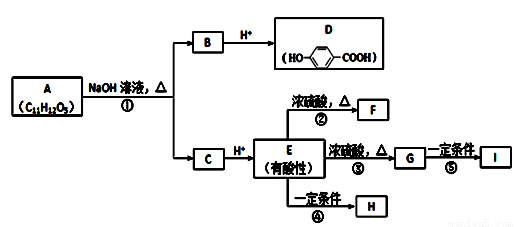
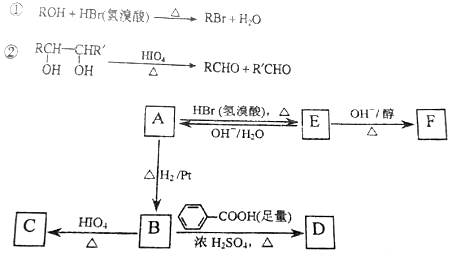
下列实验操作及现象与实验结论一致的是( )
选项 | 实验操作及现象 | 实验结论 |
A | 向某溶液中加入盐酸酸化的BaCl2溶液,生成白色沉淀 | 该溶液中不一定含有SO42- |
B | 光洁的铁钉放在冷的浓硫酸中,无明显现象 | 铁钉与冷的浓硫酸不反应 |
C | 将少量的溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CCl4振荡静置,下层分别呈无色和紫红色 | 氧化性:Br2>Fe3+>I2 |
D | 向浓度均为0.1 mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01 mol·L-1的AgNO3溶液,产生的沉淀呈黄色 | Ksp(AgCl)<Ksp(AgI) |
13.不用任何试剂,即可鉴别开的一组试剂是( )
0 161615 161623 161629 161633 161639 161641 161645 161651 161653 161659 161665 161669 161671 161675 161681 161683 161689 161693 161695 161699 161701 161705 161707 161709 161710 161711 161713 161714 161715 161717 161719 161723 161725 161729 161731 161735 161741 161743 161749 161753 161755 161759 161765 161771 161773 161779 161783 161785 161791 161795 161801 161809 203614
| A. | Na2CO3和HCl | B. | NaCl和Na2CO3 | C. | H2SO4和BaCl2 | D. | NaCl和Na2SO4 |


 Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示
Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示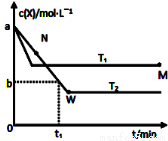



 存在,再加入1.1gKI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用0.0250mol/L硫代硫酸钠溶液滴定至终点,平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL。
存在,再加入1.1gKI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用0.0250mol/L硫代硫酸钠溶液滴定至终点,平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL。