3.某种新型细菌燃料电池的工作原理是:首先利用细菌将某种有机酸分解生成H2,然后将生成的H2通过以H3PO4稀溶液为电解质的燃料电池进行发电.这种细菌燃料电池发电时负极发生的反应为( )
| A. | H2=2H++2e- | B. | H2+2OH--2e-═2H2O | ||
| C. | O2+2H2O+4e-═4OH- | D. | 4H++O2═2H2O-4e- |
2.20℃、1大气压下,lgH2完全燃烧生成稳定的氧化物,测得放出142.9kJ的热量.下列表示该反应的热化学方程式正确的是( )
| A. | 2H2(g)+O2(g)═2H2O(1)△H=-149.2 kJ/mol | B. | H2(g)+O2(g)═H2O(1)△H=+285.8 kJ/mol | ||
| C. | 2H2(g)+O2(g)═2H2O(g)△H=-571.6kJ/mol | D. | 2H2(g)+O2(g)═2H2O(1)△H=-571.6kJ/mol |
1.已知反应:aA(g)+bB(g)?cC(g),若其他条件不变时,改变某一条件对其平衡的影响的几种情况的图象(图中p表示压强,r表示温度,n表示物质的量,a表示平衡转化率,横坐标均为时间)如下.下列判断正确的是( )
| A. | 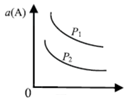 图:p1>p2,则此反应只能在高温下自发进行 | |
| B. |  图:此反应的△H<0,且T1<T2 | |
| C. |  图:表示t1时刻一定是使用催化剂对反应速率的影响 | |
| D. |  图:表示t1时刻增大B的浓度对反应速率的影响 |
20.在一定温度下,一定体积的密闭容器中有如下平衡:H2(g)+I2(g)?2HI(g)已知H2和I2的起始浓度均为0.10moL•L-1,达平衡时HI的浓度为0.16moL•L-1.若H2和I2的起始浓度均变为0.20moL•L-1时,则平衡时H2的浓度是( )
| A. | 0.16 moL•L-1 | B. | 0.08 moL•L-1 | C. | 0.04moL•L-1 | D. | 0.02moL•L-1 |
19.能说明某温度下,反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在密闭容器中,已达到平衡状态的是( )
| A. | NH3、NO消耗的速率相等 | |
| B. | 容器内NH3、O2、NO、H2O四种气体共存 | |
| C. | NO、H2O的生成速率相等 | |
| D. | 单位时间内NH3、O2消耗的物质的量相等 |
18.在一容积可变的密闭容器中,存在2HI(g)?H2(g)+I2(g)△H>0.欲使体系颜色加深,可采取的措施是( )
| A. | 缩小容器的体积 | B. | 在体积不变的情况下充入适量H2 | ||
| C. | 适当降低温度 | D. | 在保持压强不变情况下充入适量N2 |
17.升髙温度能加快反应速率的主要原因是( )
| A. | 活化分子的能量明显增加 | B. | 改变了化学反应的能量变化 | ||
| C. | 降低了反应的活化能 | D. | 增加了活化分子的百分数 |
16.下列离子方程式(或电离方程式)不正确的是( )
| A. | H2O+H2O?H3O++OH- | B. | CO32-+H2O?HCO3-+OH- | ||
| C. | Fe3++Fe?2Fe2+ | D. | HNO3?H++NO3- |
14.下列说法中,不正确的是( )
0 161575 161583 161589 161593 161599 161601 161605 161611 161613 161619 161625 161629 161631 161635 161641 161643 161649 161653 161655 161659 161661 161665 161667 161669 161670 161671 161673 161674 161675 161677 161679 161683 161685 161689 161691 161695 161701 161703 161709 161713 161715 161719 161725 161731 161733 161739 161743 161745 161751 161755 161761 161769 203614
| A. | Si可用来制造半导体材料 | |
| B. | 用丁达尔效应可以鉴别溶液和胶体 | |
| C. | 铁制容器可用于常温下贮存、运输浓硫酸 | |
| D. | SO3溶于水形成的溶液能导电,所以SO3是电解质 |

 ;
;