4.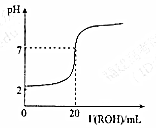 室温时,往20mL 0.1mol•L-1的HM酸溶液中逐滴滴入0.1mol•L-1的ROH碱溶液,溶液的pH与所加的ROH溶液的体积关系如图所示,下列说法正确的是( )
室温时,往20mL 0.1mol•L-1的HM酸溶液中逐滴滴入0.1mol•L-1的ROH碱溶液,溶液的pH与所加的ROH溶液的体积关系如图所示,下列说法正确的是( )
 室温时,往20mL 0.1mol•L-1的HM酸溶液中逐滴滴入0.1mol•L-1的ROH碱溶液,溶液的pH与所加的ROH溶液的体积关系如图所示,下列说法正确的是( )
室温时,往20mL 0.1mol•L-1的HM酸溶液中逐滴滴入0.1mol•L-1的ROH碱溶液,溶液的pH与所加的ROH溶液的体积关系如图所示,下列说法正确的是( )| A. | V(ROH)<20mL时,随着V(ROH)增大,HM的电离程度减小 | |
| B. | K(HM)=K(ROH) | |
| C. | RM不能发生水解反应 | |
| D. | V(ROH)>20mL时,溶液中c(R+)<c(M-) |
2.由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是旧键断裂和新键的形成过程.
已知反应N2(g)+3H2(g)2NH3(g)△H=-93kJ•mol-1.试根据表中所列键能数据,计算a 的数值为391kJ/mol.
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | a | 945 |
11.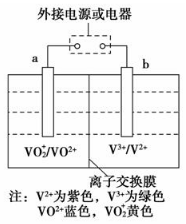 某可充电电池的原理如图所示,已知a、b为惰性电极,溶液呈酸性.充电时右槽溶液颜色由绿色变为紫色.下列叙述正确的是( )
某可充电电池的原理如图所示,已知a、b为惰性电极,溶液呈酸性.充电时右槽溶液颜色由绿色变为紫色.下列叙述正确的是( )
 某可充电电池的原理如图所示,已知a、b为惰性电极,溶液呈酸性.充电时右槽溶液颜色由绿色变为紫色.下列叙述正确的是( )
某可充电电池的原理如图所示,已知a、b为惰性电极,溶液呈酸性.充电时右槽溶液颜色由绿色变为紫色.下列叙述正确的是( )| A. | 放电时,H+从左槽迁移进右槽 | |
| B. | 放电过程中,左槽溶液颜色由黄色变为蓝色 | |
| C. | 充电时,b极接直流电源正极,a极接直流电源负极 | |
| D. | 充电过程中,a极的电极反应式为:VO2++2H++e-═VO2++H2O |
10.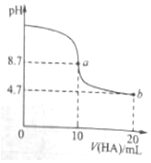 室温下向10ml 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
室温下向10ml 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
 室温下向10ml 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
室温下向10ml 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )| A. | a点所示溶液中c(A-)+c(HA)=0.1mol•L-1 | |
| B. | b点所示溶液中c(HA)>c(A-) | |
| C. | pH=7时,c(Na+)=c(A-)+c(HA) | |
| D. | a、b两点所示溶液中水的电离程度a>b |
9.表给出了X、Y、Z、W四种短周期主族元素的部分信息.请根据这些信息判断下列说法中正确的是( )
| 元素 | X | Y | Z | W |
| 原子半径 | 0.102 | 0.16 | 0.074 | 0.071 |
| 最高正价或最低负价 | +6 | +2 | -2 | -1 |
| A. | HW是热稳定性最强的氢化物 | |
| B. | Z的最高正价为+6 | |
| C. | 原子序数X>Y>Z>W | |
| D. | 纯净的X单质与纯净的Z单质反应生成XZ3 |
8.在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列物质参与反应的先后顺序正确的是( )
| A. | 含等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+ | |
| B. | 含等物质的量的Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+、Fe2+ | |
| C. | 含等物质的量的AlO2-、OH-、CO32-的溶液中,逐滴加入盐酸:OH-、AlO2-、CO32- | |
| D. | 含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2:KOH、Ba(OH)2、K2CO3、BaCO3 |
7.根据表中信息判断,下列选项不正确的是( )
0 161519 161527 161533 161537 161543 161545 161549 161555 161557 161563 161569 161573 161575 161579 161585 161587 161593 161597 161599 161603 161605 161609 161611 161613 161614 161615 161617 161618 161619 161621 161623 161627 161629 161633 161635 161639 161645 161647 161653 161657 161659 161663 161669 161675 161677 161683 161687 161689 161695 161699 161705 161713 203614
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4-、Cl- | Cl2、Mn2+ |
| A. | 第①组反应的其余产物为H2O和O2 | |
| B. | 第②组反应中参加反应的Cl2与FeBr2的物质的量之比为1:2 | |
| C. | 第③组反应中生成1molCl2,转移电子2mol | |
| D. | 氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2 |
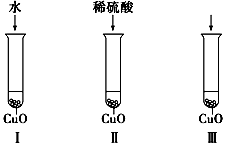 氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解.请你和他一起通过如图所示Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.
氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解.请你和他一起通过如图所示Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.