6.下列有关说法正确的是( )
| A. | 漂白粉、氨水和冰醋酸都属于混合物 | |
| B. | Fe(OH)3胶体无色、透明,能产生丁达尔现象 | |
| C. | 淀粉、纤维素、天然橡胶都是天然高分子化合物 | |
| D. | SiO2既能和NaOH溶液反应又能和氢氟酸反应,所有是两性氧化物 |
5.利用下列试剂,选用合适方法鉴别Na2SO4、Na2SO3、Na2CO3、NaCl四种溶液,最佳试剂组是( )
| A. | BaCl2、HCl、品红溶液 | B. | BaCl2、H2SO4、石蕊溶液 | ||
| C. | AgNO3和HNO3溶液 | D. | AgNO3和BaCl2溶液 |
4.已知常温下CH3COOH和NH3•H2O的电离常数相等,现向10mL浓度为0.1mol•L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中下列说法正确的是( )
| A. | 水的电离程度始终增大 | |
| B. | $\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$先增大再减小 | |
| C. | 当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO-),c(H+)=c(OH-) | |
| D. | 当加入氨水的体积为10mL时,溶液中的pH=7,由水电离出的c(H+)=1×10-7 |
3.胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统.实验测得101kPa时,1mol H2完全燃烧生成液态水,放出285.8kJ的热量;1mol CH4完全燃烧生成液态水和CO2,放出890.3kJ的热量.下列热化学方程式书写正确的是( )
| A. | 2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 | |
| B. | CH4 (g)+2 O2(g)═CO2(g)+2 H2O (l)△H=-890.3 kJ•mol-1 | |
| C. | CH4(g)+2 O2(g)═CO2(g)+2 H2O (g)△H=-890.3 kJ•mol-1 | |
| D. | CH4(g)+2 O2 (g)═CO2(g)+2 H2O (l)△H=+890.3 kJ•mol-1 |
2.下列依据相关实验得出的结论,正确的是( )
| A. | 用干净的铂丝蘸取少量溶液在酒精灯外焰上灼烧,发现火焰呈黄色,则溶液中无K+ | |
| B. | 检验某补铁药片(主要成分为亚铁化合物)是否氧化变质,使用氯水和硫氰化钾溶液 | |
| C. | 向某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- | |
| D. | 向某溶液X中滴加盐酸无明显现象,再滴加BaCl2溶液有白色沉淀,则X中含有SO42- |
1.氨气是一种重要的化工产品,是生产铵盐、尿素等原料,工业合成氨的反应如下:
N2(g)+3H2(g)?2NH3(g)△H=一92.4KJ•mol-1
(1)已知H2(g)的燃烧热为285KJ/mol,写出NH3(g)在纯氧中燃烧生成无毒、无害物质的热化学方程式.
(2)25℃时,将a mol (NH4)2SO4溶于水,向该溶液中滴加V L稀氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将逆向(填“正向”、“不”或“逆向”)移动,所滴加稀氨水的物质的量浓度为$\frac{a}{100V}$mol•L-1.(25℃时,NH3•H2O的电离平衡常数Kb≈2×10-5)
(3)工业上常通过如下反应合成尿素[CO(NH2)2]:
CO2(g)+2NH3(g)?CO(NH2)2(l)+H2O(g)△H<0,t℃时,向容积恒定为2L的密闭容器中加入0.10molCO2和0.40molNH3.反应中CO2( g)的物质的量随时间变化如表所示:
①20min时,υ正(CO2 )>80min时.υ逆(H2O)(填“>”、“=”或“<”).在t℃时,该反应额平衡常数表达式为K=$\frac{c({H}_{2}O)}{c(C{O}_{2}){c}^{2}(N{H}_{3})}$;
②在100min时,保持其它条件不变,再向容器中充入0.050mo1CO2和0.20molNH3,重新建立平衡后CO2的转化率与原平衡相比将增大(填“增大”、“不变”或“减小”).
③上述可逆反应的平衡常数为76.53(保留二位小数).
④根据表中数据在图甲中绘制出在t℃下NH3的转化率随时间变化的图象;保持其它条件不变;则(t+10)℃下正确的图象可能是B(填图甲中的“A”或“B”).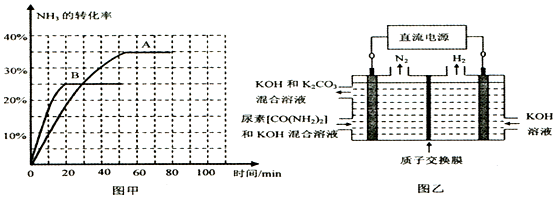
⑤图乙所示装置(阴、阳极均为惰性电极)可用于电解尿素〔CO(NH2)2〕的碱性溶液制取氢气.该装置中阳极的电极反应式为CO(NH2)2-6e-+8OH-=CO32-+N2↑+6H2O,若两极共收集到气体22.4L(标况),则消耗的尿素为15g(忽略气体的溶解).
N2(g)+3H2(g)?2NH3(g)△H=一92.4KJ•mol-1
(1)已知H2(g)的燃烧热为285KJ/mol,写出NH3(g)在纯氧中燃烧生成无毒、无害物质的热化学方程式.
(2)25℃时,将a mol (NH4)2SO4溶于水,向该溶液中滴加V L稀氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将逆向(填“正向”、“不”或“逆向”)移动,所滴加稀氨水的物质的量浓度为$\frac{a}{100V}$mol•L-1.(25℃时,NH3•H2O的电离平衡常数Kb≈2×10-5)
(3)工业上常通过如下反应合成尿素[CO(NH2)2]:
CO2(g)+2NH3(g)?CO(NH2)2(l)+H2O(g)△H<0,t℃时,向容积恒定为2L的密闭容器中加入0.10molCO2和0.40molNH3.反应中CO2( g)的物质的量随时间变化如表所示:
| 时间/min | 0 | 30 | 70 | 80 | 100 |
| n(CO2)/mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
②在100min时,保持其它条件不变,再向容器中充入0.050mo1CO2和0.20molNH3,重新建立平衡后CO2的转化率与原平衡相比将增大(填“增大”、“不变”或“减小”).
③上述可逆反应的平衡常数为76.53(保留二位小数).
④根据表中数据在图甲中绘制出在t℃下NH3的转化率随时间变化的图象;保持其它条件不变;则(t+10)℃下正确的图象可能是B(填图甲中的“A”或“B”).

⑤图乙所示装置(阴、阳极均为惰性电极)可用于电解尿素〔CO(NH2)2〕的碱性溶液制取氢气.该装置中阳极的电极反应式为CO(NH2)2-6e-+8OH-=CO32-+N2↑+6H2O,若两极共收集到气体22.4L(标况),则消耗的尿素为15g(忽略气体的溶解).
20.在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:C(s)+H2O(g)?CO(g)+H2(g),不能确定上述可逆反应在一定条件下已达到化学平衡状态的是( )
| A. | 体系的压强不再发生变化 | |
| B. | 混合气体的平均相对分子质量不再发生变化 | |
| C. | v正(CO)=v逆(H2O) | |
| D. | 1 mol H-H键断裂的同时断裂2 mol H-O键 |
19.下列反应中,反应后固体物质增重的是( )
| A. | 氢气通过灼热的CuO粉末 | B. | 二氧化碳通过Na2O2粉末 | ||
| C. | 将Na2O2投入水中 | D. | 将锌粒投入Cu(NO3)2溶液 |
18.把一定量的铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe3+和Fe2+的浓度恰好相等.则己反应的Fe3+和未反应的Fe3+的物质的量之比为( )
| A. | 1:1 | B. | 2:1 | C. | 2:3 | D. | 3:2 |
17.下列离子的检验方法、现象及结论均合理的是( )
0 161508 161516 161522 161526 161532 161534 161538 161544 161546 161552 161558 161562 161564 161568 161574 161576 161582 161586 161588 161592 161594 161598 161600 161602 161603 161604 161606 161607 161608 161610 161612 161616 161618 161622 161624 161628 161634 161636 161642 161646 161648 161652 161658 161664 161666 161672 161676 161678 161684 161688 161694 161702 203614
| A. | 向某溶液中先滴加氯水,再滴加KSCN溶滚,溶液显血红色,说明原溶液中含有Fe3+ | |
| B. | 向某溶液中滴加过量氨水,先有白色沉淀产生,然后沉淀溶解,说明原溶液中含有Al3+ | |
| C. | 向某溶液中滴加Ca(OH)2溶液,得到白色沉淀,说明原溶液中含有CO32- | |
| D. | 向某溶液中滴加过量NaOH溶液,得到蓝色沉淀,说明原溶液中含有Cu2+ |