题目内容
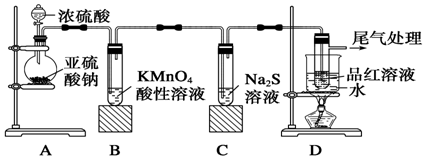
5.利用下列试剂,选用合适方法鉴别Na2SO4、Na2SO3、Na2CO3、NaCl四种溶液,最佳试剂组是( )| A. | BaCl2、HCl、品红溶液 | B. | BaCl2、H2SO4、石蕊溶液 | ||
| C. | AgNO3和HNO3溶液 | D. | AgNO3和BaCl2溶液 |
分析 BaSO4、BaSO3、BaCO3均不溶于水,但BaSO3和BaCO3溶于盐酸,并且BaSO3与盐酸反应生成刺激性气味的SO2气体,而BaCO3与盐酸反应无色无味的CO2,SO2和CO2都能是石蕊试液变红,但SO2可使品红褪色.
解答 解:A.在Na2SO4、Na2SO3、Na2CO3、NaCl中滴加BaCl2和HCl.Na2SO4生成沉淀不溶解;NaCl不生成沉淀;Na2SO3、Na2CO3生成沉淀后都溶解,但Na2SO3生成的气体可以使品红褪色,而Na2CO3不能,可鉴别,故A正确;
B.Na2SO4、Na2SO3、Na2CO3中滴加BaCl2和硫酸.都生成沉淀,不能鉴别,故B错误;
C.加入AgNO3和HNO3溶液,Na2SO3被氧化为Na2SO4,不能鉴别,故C错误;
D.加入AgNO3和BaCl2溶液,都生成白色沉淀,不能鉴别,故D错误.
故选A.
点评 本题考查物质的鉴别和检验,为高频考点,侧重考查学生对元素与化合物知识的掌握情况及思维的灵活性,题目难度中等,注意相关物质的性质的把握.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
3.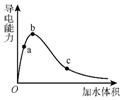 一定温度下,将一定量的纯醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
一定温度下,将一定量的纯醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
 一定温度下,将一定量的纯醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
一定温度下,将一定量的纯醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )| A. | 醋酸的电离度:c<b<a | |
| B. | 溶液的pH值:b<a<c | |
| C. | 蘸取a点溶液滴在湿润的pH试纸上,测得pH值一定偏大 | |
| D. | 若分别取a、b、c三点的溶液各10mL,各用同浓度的氢氧化钠溶液中和,消耗NaOH溶液的体积a>b>c |
20.在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:C(s)+H2O(g)?CO(g)+H2(g),不能确定上述可逆反应在一定条件下已达到化学平衡状态的是( )
| A. | 体系的压强不再发生变化 | |
| B. | 混合气体的平均相对分子质量不再发生变化 | |
| C. | v正(CO)=v逆(H2O) | |
| D. | 1 mol H-H键断裂的同时断裂2 mol H-O键 |
10.短周期主族元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与Y同主族.下列说法正确的是( )
| A. | Z元素的简单离子是其所在周期中元素的简单离子半径最小的 | |
| B. | Y的简单气态氢化物的热稳定性比W的强 | |
| C. | Y与W形成的化合物一定能使酸性高锰酸钾溶液腿色 | |
| D. | 最高价氧化物对应水化物的酸性X比W的强 |
17.某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2,下列对该溶液的叙述不正确的是( )
| A. | 由水电离出来的H+的浓度是1.0×10-10 mol/L | |
| B. | 该温度高于25°C | |
| C. | 加入NaHSO4晶体抑制了水的电离 | |
| D. | c(H+)=c(OH-)+c(SO42-) |
14.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 食盐、醋、糖都有防腐功效 | |
| B. | 煤粉碎后更易燃烧,是因为粉碎增强了煤的还原性 | |
| C. | 鸡蛋煮熟后,蛋白质水解成了氨基酸 | |
| D. | 月饼包装中的还原铁粉小包和旺旺仙贝包装中的生石灰小包的作用相同 |
15.下列表示正确的是( )
| A. | 含20个电子的氯原子的符号为:3517Cl | |
| B. | 四氯化碳的球棍模型: | |
| C. | 氩的原子结构示意图: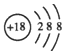 | |
| D. | 乙烯的结构简式:CH2CH2 |