4.下列有关物质的量和摩尔质量的叙述,正确的是( )
| A. | 水的摩尔质量是18 g | |
| B. | 0.012 Kg 12C中约含有6.02×1023个碳原子 | |
| C. | 1 mol水中含有2 mol氢和1 mol氧 | |
| D. | 1 mol任何物质都含有6.02×1023个分子 |
3.臭氧在烟气脱硝中的反应为2NO2(g)+O3(g)?N2O5(g)+O2(g).若此反应在恒容密闭容器中进行,相关图象如下列选项,其中对应分析结论正确的是( )
| A | B | C | D |
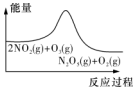 |  |  |  |
| 平衡后升温,NO2含量降低 | 0~2s内,v(O2)=0.2mol•L-1•s-1 | v正:b点>a点,b点:v逆>v正 | 恒温,t1时再充入O3 |
| A. | .A. | B. | .B | C. | .C | D. | .D |
2.下列离子方程式正确的是( )
| A. | 硝酸银溶液与铜:Cu+Ag+=Cu2++Ag | |
| B. | 氧化铜与盐酸反应:O2-+2H+=H2O | |
| C. | 硫酸氢钠与氢氧化钠溶液混合:OH-+H+=H2O | |
| D. | 向澄清石灰水中加入盐酸:2H++Ca(OH)2=Ca2++2H2O |
20. 酒精检测仪可帮助执法交警测试驾驶员饮酒的多少,其工作原理示意图如图所示.反应原理为:CH3CH2OH+O2═CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量.下列说法正确的是( )
酒精检测仪可帮助执法交警测试驾驶员饮酒的多少,其工作原理示意图如图所示.反应原理为:CH3CH2OH+O2═CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量.下列说法正确的是( )
 酒精检测仪可帮助执法交警测试驾驶员饮酒的多少,其工作原理示意图如图所示.反应原理为:CH3CH2OH+O2═CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量.下列说法正确的是( )
酒精检测仪可帮助执法交警测试驾驶员饮酒的多少,其工作原理示意图如图所示.反应原理为:CH3CH2OH+O2═CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量.下列说法正确的是( )| A. | b为正极,电极反应式为:O2+4H++4e-═2H2O | |
| B. | 电解质溶液中的H+移向a电极 | |
| C. | 若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气 | |
| D. | 呼出气体中酒精含量越高,微处理器中通过的电流越小 |
18.下列关于配制一定物质的量浓度的溶液说法正确的是( )
| A. | 将NaCl固体置于托盘天平右盘称量:左盘砝码(8g)和游码(0.6g)读数的和为8.6g | |
| B. | 容量瓶上标有刻度线、温度和浓度,使用前要事先检查是否漏水 | |
| C. | 配制一定物质的量浓度的溶液用到的主要仪器有:托盘天平、量筒、烧杯、玻璃棒、容量瓶、胶头滴管 | |
| D. | 配制1L0.2mol/L的H2SO4溶液,定容时仰视刻度线操作,则配出浓度偏高 |
17.在常温下,分别利用下列反应产生氢气,其反应方程式分别为:
①2KMnO4+16HCl(浓)→2KCl+2MnCl2+5Cl2↑+8H2O
②KClO3+6HCl(浓)→KCl+3Cl2↑+3H2O
如果上述两个反应所产生的氯气质量相等,被氧化的还原剂的物质的量之比为( )
①2KMnO4+16HCl(浓)→2KCl+2MnCl2+5Cl2↑+8H2O
②KClO3+6HCl(浓)→KCl+3Cl2↑+3H2O
如果上述两个反应所产生的氯气质量相等,被氧化的还原剂的物质的量之比为( )
| A. | 8:5 | B. | 6:5 | C. | 2:1 | D. | 1:1 |
16.设NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 6.2 g Na2O所含的离子数为0.2 NA | |
| B. | 46 gNO2与N2O4的混合气体中所含的原子数是3NA | |
| C. | 2.8 gN2中含有共用电子对的数目为0.1 NA | |
| D. | 0.1 molH2与Cl2的混合气体充分反应后,体系中含有共价键总数为0.2NA |
15.下列变化中,属于还原反应的是( )
0 161499 161507 161513 161517 161523 161525 161529 161535 161537 161543 161549 161553 161555 161559 161565 161567 161573 161577 161579 161583 161585 161589 161591 161593 161594 161595 161597 161598 161599 161601 161603 161607 161609 161613 161615 161619 161625 161627 161633 161637 161639 161643 161649 161655 161657 161663 161667 161669 161675 161679 161685 161693 203614
| A. | H+→H2O | B. | SO3→H2SO4 | C. | Fe2+→Fe3+ | D. | Cl2→Cl- |
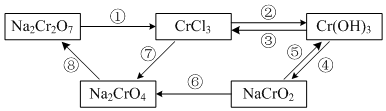
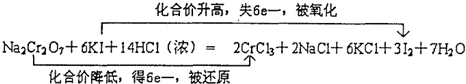
 我国规定:室内甲醛含量不得超过0.08mg•m-3.某研究性学习小组欲利用酸性KMnO4溶液测定空气中甲醛的含量,请你协助他们完成相关学习任务.(部分装置如图),其反应原理及步骤如下:
我国规定:室内甲醛含量不得超过0.08mg•m-3.某研究性学习小组欲利用酸性KMnO4溶液测定空气中甲醛的含量,请你协助他们完成相关学习任务.(部分装置如图),其反应原理及步骤如下: