9.欲配制100mL1.0mol/LNa2SO4溶液,全部正确的方法是( )
①将14.2gNa2SO4溶于适量水中配成100mL溶液
②将32.2gNa2SO4.10H2O溶于少量水中,再用水稀释至100mL
③将20ml5.0mol/LNa2SO4溶液用水稀释至100mL
④将14.2gNa2SO4溶于100mL水中.
①将14.2gNa2SO4溶于适量水中配成100mL溶液
②将32.2gNa2SO4.10H2O溶于少量水中,再用水稀释至100mL
③将20ml5.0mol/LNa2SO4溶液用水稀释至100mL
④将14.2gNa2SO4溶于100mL水中.
| A. | ①②③④ | B. | ①③ | C. | ①②③ | D. | ①② |
8.下列关于萃取和蒸馏的说法中,正确的有( )
| A. | 用乙醇萃取溴水中的溴单质可选用分液漏斗 | |
| B. | 为了保证冷凝效果,蒸馏操作时冷凝水流向要与蒸馏水流动方向相同 | |
| C. | 蒸馏操作时温度计的水银球要与圆底烧瓶的支管口相平 | |
| D. | 分液时,需将分液漏斗上口的塞子打开或使玻璃凹槽和小孔连通 |
6.下列说法或实验操作正确的是( )
| A. | 酒精、汽车在桌面上着火时,立即用水扑灭 | |
| B. | 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 | |
| C. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应立即转移到容量瓶中定容,以减小误差 | |
| D. | 用分液漏斗分液时,下层液体从下口放出,上层液体从上口倒出 |
1.汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3=K2O+5Na2O+16N2↑.若氧化产物比还原产物多 1.75mol,则下列判断正确的是( )
| A. | N2是还原产物 | |
| B. | 有 0.250 mol KNO3 被氧化 | |
| C. | NaN3中氮元素为-3 价 | |
| D. | 被氧化的 N 原子的物质的量为 3.75mol |
20.设 N A表示阿伏加德罗常数的值,下列说法正确的是( )
0 161450 161458 161464 161468 161474 161476 161480 161486 161488 161494 161500 161504 161506 161510 161516 161518 161524 161528 161530 161534 161536 161540 161542 161544 161545 161546 161548 161549 161550 161552 161554 161558 161560 161564 161566 161570 161576 161578 161584 161588 161590 161594 161600 161606 161608 161614 161618 161620 161626 161630 161636 161644 203614
| A. | 5.6 g Fe 和足量的氧气完全燃烧失去电子数为 3N A | |
| B. | 1L 浓度为 0.5mol/LFeCl3 溶液加热煮沸后,会生成 0.5molFe(OH)3胶体粒子 | |
| C. | 常温常压下,23 g NO2 和 N2O4 的混合气体一定含有 N A 个氧原子 | |
| D. | 标况下,4.48L 的水中含有 H2O 分子的数目为 0.2N A |




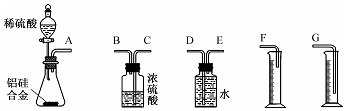

 →
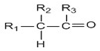
→
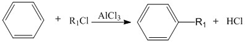
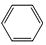 +R1Cl$\stackrel{AlCl_{3}}{→}$
+R1Cl$\stackrel{AlCl_{3}}{→}$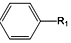 +HCl
+HCl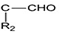 +H2O(R1、R2、R3代表烃基或氢原子)回答下列问题:
+H2O(R1、R2、R3代表烃基或氢原子)回答下列问题: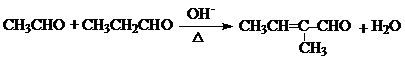 .
.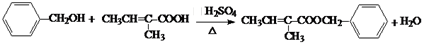 .
.