题目内容
9.欲配制100mL1.0mol/LNa2SO4溶液,全部正确的方法是( )①将14.2gNa2SO4溶于适量水中配成100mL溶液
②将32.2gNa2SO4.10H2O溶于少量水中,再用水稀释至100mL
③将20ml5.0mol/LNa2SO4溶液用水稀释至100mL
④将14.2gNa2SO4溶于100mL水中.
| A. | ①②③④ | B. | ①③ | C. | ①②③ | D. | ①② |
分析 结合n=$\frac{m}{M}$、c=$\frac{n}{V}$及稀释前后溶质的物质的量不变计算.
解答 解:①将14.2gNa2SO4溶于适量水中配成100mL溶液,n=$\frac{14.2g}{142g/mol}$=0.1mol、c=$\frac{0.1mol}{0.1L}$=1.0mol/L,故正确;
②将32.2gNa2SO4.10H2O溶于少量水中,再用水稀释至100mL,n=$\frac{32.2g}{322g/mol}$0.1mol、c=$\frac{0.1mol}{0.1L}$=1.0mol/L,故正确;
③将20ml5.0mol/LNa2SO4溶液用水稀释至100mL,则c=$\frac{0.02L×5.0mol/L}{0.1L}$=0.1mol/L,故正确;
④将14.2gNa2SO4溶于100mL水中,水为溶剂,溶液体积未知,不能计算c,故错误;
故选C.
点评 本题考查物质的量浓度及溶液配制,为高频考点,把握物质的量、质量、浓度的关系为解答该题的关键,侧重分析与计算能力的考查,注意溶液体积的判断,题目难度不大.

练习册系列答案
相关题目
17.下列各组离子一定能大量共存的是( )
| A. | 在无色溶液中:NH4+、MnO4-、SO42-、CO32- | |
| B. | 在含大量 Ba2+的溶液中:NH4+、Na+、Cl-、OH- | |
| C. | 在强碱溶液中:Na+、K+、Cl-、SO32- | |
| D. | 在 pH=1 的溶液中:K+、Fe2+、Cl-、CH3COO- |
14.下列反应中既属于离子反应,又属于氧化还原反应的是( )
| A. | Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O | B. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 | ||
| C. | NaCl+AgNO3═NaNO3+AgCl↓ | D. | Zn+CuSO4═Cu+ZnSO4 |
2. 乙苯是一种用途广泛的有机原料,可制备多种化工产品.
乙苯是一种用途广泛的有机原料,可制备多种化工产品.
(一)制备α-氯乙基苯的反应如下:
 +Cl2(g)$\stackrel{催化剂}{?}$
+Cl2(g)$\stackrel{催化剂}{?}$ -CH(g)+HCl(g)△H>0,T℃时,向一恒压密闭容器中充入等物质的量的乙苯气体和氯气发生上述反应(已排除其他反应干扰),测得乙苯物质的量分数随时间变化如表所示:
-CH(g)+HCl(g)△H>0,T℃时,向一恒压密闭容器中充入等物质的量的乙苯气体和氯气发生上述反应(已排除其他反应干扰),测得乙苯物质的量分数随时间变化如表所示:
(1)若初始投入乙苯为2mol,恒压容器容积10L,用氯气表示该反应0-5分钟内的速率υ(Cl2)=0.32mol•L-1•mim-1.T℃时,计算该反应的化学平衡常数K=16.6分钟时,仅改变一种条件破坏了平衡,则改变的外界条件为升高温度.
(2)图中能正确反映平衡常数K随温度变化关系的曲线为b(填曲线标记字母),其判断理由是该反应正方向放热,升高温度使平衡正向移动,平衡常数增大.
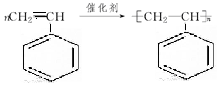
(二)催化脱氢生产苯乙烯的反应如下:
 $\stackrel{催化剂}{?}$
$\stackrel{催化剂}{?}$ =CH2(g)+H2(g)△H=+124kJ/mol
=CH2(g)+H2(g)△H=+124kJ/mol
(3)气相反应的化学平衡常数有多种表示方法,可用各气体物质的量分数代替浓度项表示平衡常数,写出上述反应的平衡常数表达式Kχ=$\frac{λ(氢气)•λ(苯乙烯)}{λ(乙苯)}$.(用符号χ表示气体物质的量分数).
(4)工业上,在恒压条件下进行上述反应时,将乙苯与水蒸气的混合气体通入反应器中(已知水蒸气不参与反应),加入水蒸气可以使乙苯的转化率增大,用化学平衡理论解释乙苯转化率增加的原因恒压条件下加入水蒸气,体积增大,使反应体系减压,平衡正向移动.
 乙苯是一种用途广泛的有机原料,可制备多种化工产品.
乙苯是一种用途广泛的有机原料,可制备多种化工产品.(一)制备α-氯乙基苯的反应如下:
 +Cl2(g)$\stackrel{催化剂}{?}$
+Cl2(g)$\stackrel{催化剂}{?}$ -CH(g)+HCl(g)△H>0,T℃时,向一恒压密闭容器中充入等物质的量的乙苯气体和氯气发生上述反应(已排除其他反应干扰),测得乙苯物质的量分数随时间变化如表所示:
-CH(g)+HCl(g)△H>0,T℃时,向一恒压密闭容器中充入等物质的量的乙苯气体和氯气发生上述反应(已排除其他反应干扰),测得乙苯物质的量分数随时间变化如表所示:| 时间/(min) | 0 | 2 | 5 | 6 | 9 | 10 |
| χ(乙苯) | 0.5 | 0.25 | 0.1 | 0.1 | 0.05 | 0.05 |
(2)图中能正确反映平衡常数K随温度变化关系的曲线为b(填曲线标记字母),其判断理由是该反应正方向放热,升高温度使平衡正向移动,平衡常数增大.
(二)催化脱氢生产苯乙烯的反应如下:
 $\stackrel{催化剂}{?}$
$\stackrel{催化剂}{?}$ =CH2(g)+H2(g)△H=+124kJ/mol
=CH2(g)+H2(g)△H=+124kJ/mol(3)气相反应的化学平衡常数有多种表示方法,可用各气体物质的量分数代替浓度项表示平衡常数,写出上述反应的平衡常数表达式Kχ=$\frac{λ(氢气)•λ(苯乙烯)}{λ(乙苯)}$.(用符号χ表示气体物质的量分数).
(4)工业上,在恒压条件下进行上述反应时,将乙苯与水蒸气的混合气体通入反应器中(已知水蒸气不参与反应),加入水蒸气可以使乙苯的转化率增大,用化学平衡理论解释乙苯转化率增加的原因恒压条件下加入水蒸气,体积增大,使反应体系减压,平衡正向移动.
20.下列说法不正确的是( )
| A. | 用小苏打(NaHCO3)发酵面团制作馒头 | |
| B. | 光导纤维的主要成分是SiO2 | |
| C. | 干燥的氯气和液氯均能使干燥的有色布条褪色 | |
| D. | 用Al(OH)3治疗胃酸过多 |


 →
→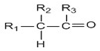
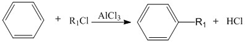
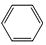 +R1Cl$\stackrel{AlCl_{3}}{→}$
+R1Cl$\stackrel{AlCl_{3}}{→}$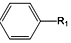 +HCl
+HCl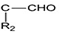 +H2O(R1、R2、R3代表烃基或氢原子)回答下列问题:
+H2O(R1、R2、R3代表烃基或氢原子)回答下列问题: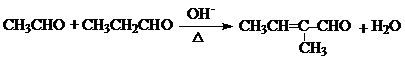 .
.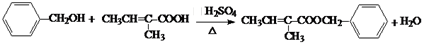 .
.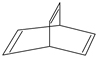 有机物的结构可用键线式简化表示,如CH3-CH═CH-CH3可表示为
有机物的结构可用键线式简化表示,如CH3-CH═CH-CH3可表示为 有一种有机物X的键线式如图所示.
有一种有机物X的键线式如图所示. .
. .
. .
.