9.下列有关的叙述正确的是( )
| A. | CO2水溶液能够导电,所以CO2是电解质 | |
| B. | 向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 | |
| C. | 根据分散质粒子的直径大小,分散系可分为溶液、浊液和胶体,浊液的分散质粒子大小介于溶液与胶体之间 | |
| D. | “血液透析”原理与胶体的性质无关 |
8.设NA表示阿伏加徳罗常数,下列叙述中正确的是( )
| A. | 1L 1mol•L-1的盐酸溶液中,所含氯化氢分子数为NA | |
| B. | 11.2L氧气中所含有的原子数为NA | |
| C. | 常温常压下42g乙烯和丁烯混合气体中,极性键数为6NA | |
| D. | 1L0.lmol/L 的 Fe2(SO4)3 溶液中,Fe3+的数目为 0.2NA |
7.对下列事实的解释正确的是( )
| A. | 浓硝酸光照变黄,证明硝酸不稳定,且产物有红棕色气体可溶于浓硝酸 | |
| B. | 向某溶液中加入氯化钡溶液和稀硝酸,生成白色沉淀,则原溶液一定含有硫酸根 | |
| C. | 常温下,将铝片放入浓硫酸中无明显现象,说明铝不与浓硫酸反应 | |
| D. | 溴水中通入SO2后,颜色褪去,说明SO2表现了漂白性 |
6.下列说法正确的是( )
| A. | 催化剂是影响化学反应速率的本质因素 | |
| B. | 当反应体系容积不变时,减小反应物的量肯定能降低反应速率 | |
| C. | 可逆反应达到反应限度时,化学反应速率为0 | |
| D. | 化学反应速率可用单位时间内反应物的浓度变化量来表示 |
5.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1molFe与足量氯气充分反应时转移的电子数为2NA | |
| B. | 18 g水中所含的电子数为10NA | |
| C. | 0.3 mol•L-1Na2SO4溶液中含0.6NA个Na+ | |
| D. | 11.2 L氮气中含NA个氮原子 |
4.下列关于漂白粉的叙述正确的是( )
| A. | 漂白粉的有效成分是Ca(ClO)2 | |
| B. | 漂白粉暴露在空气中久置不会变质 | |
| C. | 漂白粉是由Cl2与石灰乳制得 | |
| D. | 漂白粉变质过程中不涉及氧化还原反应 |
2.0.1molH2和Cl2组成的混合气体,其中Cl2的体积分数为70%,光照充分反应后,将所得的混合气体缓慢通入含有0.15molNaOH的溶液中充分反应,下列说法正确的是( )
| A. | 光照以后,所得混合气体中含有0.07 molHCl | |
| B. | 光照以后,所得混合气体体积小于原混合气体体积(相同条件下) | |
| C. | 最终所得溶液中,NaCl和NaClO的物质的量比为5:2 | |
| D. | 最终所得溶液中,还含有0.02 molNaOH |
1.已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2均为正值):H2(g)+Cl2(g)→2HCl(g)+Q1 ①; H2(g)+Br2(g)→2HBr(g)+Q2②有关上述反应的叙述错误的是( )
0 161446 161454 161460 161464 161470 161472 161476 161482 161484 161490 161496 161500 161502 161506 161512 161514 161520 161524 161526 161530 161532 161536 161538 161540 161541 161542 161544 161545 161546 161548 161550 161554 161556 161560 161562 161566 161572 161574 161580 161584 161586 161590 161596 161602 161604 161610 161614 161616 161622 161626 161632 161640 203614
| A. | Ql>Q2 | |
| B. | 反应物总能量均高于生成物总能量 | |
| C. | 1molHBr(g)具有的能量大于1molHBr(l)具有的能量 | |
| D. | 反应①生成2 molHCl(l)时放出Q1热量 |

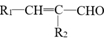 +H2O
+H2O +R2-OH$\stackrel{一定条件}{→}$
+R2-OH$\stackrel{一定条件}{→}$ .
. .
.