16.下列属于热化学方程式的是( )
| A. | C+O2$\stackrel{点燃}{→}$CO2 | B. | C(s)+O2(g)$\stackrel{点燃}{→}$CO2(g)+393.5kJ | ||
| C. | C(s)+O2(g)$\stackrel{点燃}{→}$CO2(g) | D. | C(s)+O2(g)=CO2(g)+393.5kJ |
14.如图是实验室制备1,2-二溴乙烷并进行一系列相关实验的装置(加热及夹持设备已略).
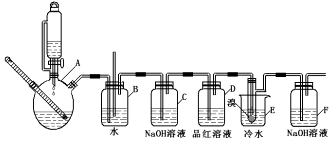
已知:
CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O
CH3CH2OH$→_{140℃}^{浓硫酸}$CH3CH2OCH2CH3+H2O
相关数据列表如表:
请完成下列填空:
(1)实验中应迅速将温度升高到170℃左右的原因是减少副产物乙醚生成.
(2)气体发生装置使用连通滴液漏斗的原因使连通滴液漏斗里的溶液容易滴下.
(3)安全瓶B在实验中有多重作用,其一可以检查实验进行中B后面的装置中导管是否发生堵塞,请写出发生堵塞时瓶B中的现象B中长直玻璃管内有一段液柱上升;
(4)装置D中品红溶液的作用是验证二氧化硫是否被除尽;
(5)容器C、F中都盛有NaOH溶液,F中NaOH溶液的作用是吸收挥发的溴蒸气;
(6)反应过程中用冷水冷却装置E不能过度冷却(如用冰水),其原因是过渡冷却1,2-二溴乙烷易凝结成固体而发生堵塞.
(7)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多,如果装置的气密性没有问题,试分析可能的原因:①浓硫酸将部分乙醇氧化②发生副反应生成乙醚③乙醇挥发④乙烯流速过快,未完全发生加成反应;(写出两条即可)
(8)除去产物中少量未反应的Br2后,还含有的主要杂质为乙醚,要进一步提纯,下列操作中必须用到的是D(填入正确选项前的字母);
A.重结晶 B.过滤 C.萃取 D.蒸馏.

已知:
CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O
CH3CH2OH$→_{140℃}^{浓硫酸}$CH3CH2OCH2CH3+H2O
相关数据列表如表:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 | 红棕色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 | 3.10 |
| 沸点/℃ | 78.5 | 132 | 34.6 | 58.8 |
| 熔点/℃ | -l30 | 9 | -1l6 | -7.2 |
| 水溶性 | 混溶 | 难溶 | 微溶 | 可溶 |
(1)实验中应迅速将温度升高到170℃左右的原因是减少副产物乙醚生成.
(2)气体发生装置使用连通滴液漏斗的原因使连通滴液漏斗里的溶液容易滴下.
(3)安全瓶B在实验中有多重作用,其一可以检查实验进行中B后面的装置中导管是否发生堵塞,请写出发生堵塞时瓶B中的现象B中长直玻璃管内有一段液柱上升;
(4)装置D中品红溶液的作用是验证二氧化硫是否被除尽;
(5)容器C、F中都盛有NaOH溶液,F中NaOH溶液的作用是吸收挥发的溴蒸气;
(6)反应过程中用冷水冷却装置E不能过度冷却(如用冰水),其原因是过渡冷却1,2-二溴乙烷易凝结成固体而发生堵塞.
(7)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多,如果装置的气密性没有问题,试分析可能的原因:①浓硫酸将部分乙醇氧化②发生副反应生成乙醚③乙醇挥发④乙烯流速过快,未完全发生加成反应;(写出两条即可)
(8)除去产物中少量未反应的Br2后,还含有的主要杂质为乙醚,要进一步提纯,下列操作中必须用到的是D(填入正确选项前的字母);
A.重结晶 B.过滤 C.萃取 D.蒸馏.
12.将amolCO2气体缓缓通入含bmolCa(OH)2的饱和石灰水中,已知a>b,下列判断正确的是( )
| A. | 形成amolCaCO3 | |
| B. | 形成bmolCaCO3 | |
| C. | 可能得到CaCO3沉淀,但沉淀量小于bmol | |
| D. | 可能最终得到澄清溶液,其中含$\frac{a}{2}$molCa2+ |
11.下列说法正确的是( )
0 161433 161441 161447 161451 161457 161459 161463 161469 161471 161477 161483 161487 161489 161493 161499 161501 161507 161511 161513 161517 161519 161523 161525 161527 161528 161529 161531 161532 161533 161535 161537 161541 161543 161547 161549 161553 161559 161561 161567 161571 161573 161577 161583 161589 161591 161597 161601 161603 161609 161613 161619 161627 203614
| A. | 离子化合物的熔点一定比共价化合物熔点高 | |
| B. | 甲烷的标准燃烧热为890.3KJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| C. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照条件和点燃条件下的△H相同 |



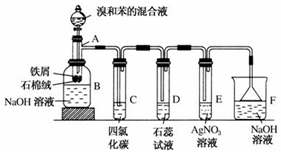 苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑.
苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑.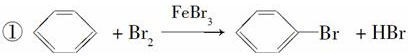 .
. 氯化铝可制备无机高分子混凝剂,在有机合成中有广泛的用途.完成下列填空:
氯化铝可制备无机高分子混凝剂,在有机合成中有广泛的用途.完成下列填空: